| Фосфорилаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
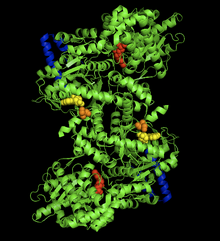 Кристаллическая структура комплекса гликогенфосфорилазы мышц кролика-АМФ. Аллостерический сайт AMP (желтый), фосфорилированный Ser14 (оранжевый), сайт связывания гликогена (синий), каталитический сайт (красный). Кристаллическая структура комплекса гликогенфосфорилазы мышц кролика-АМФ. Аллостерический сайт AMP (желтый), фосфорилированный Ser14 (оранжевый), сайт связывания гликогена (синий), каталитический сайт (красный). | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 2.4.1.1 | ||||||||
| Номер CAS | 9035 -74-9 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология генов | AmiGO / QuickGO | ||||||||
| |||||||||
Гликогенфосфорилаза является одной из фосфорилазы ферменты (EC 2.4.1.1 ). Гликогенфосфорилаза катализирует лимитирующую стадию гликогенолиза у животных, высвобождая глюкозо-1-фосфат из концевой альфа-1,4-гликозидной связи. Гликогенфосфорилаза также изучается как модельный белок, регулируемый как обратимым фосфорилированием, так и аллостерическим эффектами.
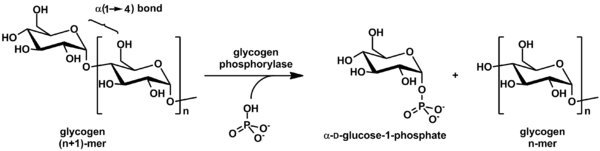
Гликогенфосфорилаза расщепляет гликоген на глюкозу субъединицы (см. Также рисунок ниже):
(цепь α-1,4-гликогена) n+ Pi ⇌ (цепь α-1,4-гликогена) n-1 + α-D-глюкозо-1-фосфат.
В гликогене остается на одну молекулу глюкозы меньше, а свободная молекула глюкозы находится в форме глюкозо-1-фосфата. Чтобы его можно было использовать для метаболизма, он должен быть преобразован в глюкозо-6-фосфат с помощью фермента фосфоглюкомутазы.
, хотя реакция обратима in vitro., внутри клетки фермент работает только в прямом направлении, как показано ниже, потому что концентрация неорганического фосфата намного выше, чем концентрация глюкозо-1-фосфата.
Гликогенфосфорилаза может действовать только на линейных цепях гликогена (α1-4 гликозидная связь). Его работа немедленно прекращается через четыре остатка от α1-6 ветви (которые чрезвычайно распространены в гликогене). В этих ситуациях необходим фермент разветвления, который выпрямляет цепь в этой области. Кроме того, фермент трансфераза сдвигает блок из 3 остатков глюкозила с внешней ветви на другой конец, и затем требуется фермент α1-6 глюкозидаза фермент для разрушения оставшейся (одиночной глюкоза) остаток α1-6, который остается в новой линейной цепи. После того, как все это будет сделано, гликогенфосфорилаза может продолжаться. Фермент специфичен для α1-4 цепей, так как молекула содержит щель длиной 30 ангстрем с таким же радиусом, что и спираль, образованная цепью гликогена; это вмещает 4-5 глюкозильных остатков, но слишком мало для разветвлений. Эта щель соединяет сайт хранения гликогена с активным каталитическим сайтом.
Гликогенфосфорилаза имеет пиридоксальфосфат (PLP, полученный из витамина B 6 ) на каждом каталитическом сайте. Пиридоксальфосфат связывается с основными остатками (в данном случае Lys680) и ковалентно образует основание Шиффа. После образования связи основания Шиффа, удерживающего молекулу PLP в активном центре, фосфатная группа на PLP легко отдает протон молекуле неорганического фосфата, позволяя неорганическому фосфату, в свою очередь, депротонироваться кислородом, образующим α-1, 4 гликозидная связь. PLP легко депротонируется, потому что его отрицательный заряд не только стабилизируется внутри фосфатной группы, но также в пиридиновом кольце, таким образом, основание конъюгата, образующееся в результате депротонирования PLP, довольно стабильно. Протонированный кислород теперь представляет собой хорошую уходящую группу , а цепь гликогена отделена от концевого гликогена способом SN1, что приводит к образованию молекулы глюкозы со вторичным карбокатионом в положении 1. Наконец, депротонированный неорганический фосфат действует как нуклеофил и связывается с карбокатионом, что приводит к образованию глюкозо-1-фосфата и цепи гликогена, укороченной на одну молекулу глюкозы.
Существует также альтернативный предложенный механизм, включающий положительно заряженный кислород в конформации полукресла.

Мономер гликогенфосфорилазы представляет собой большой белок, состоящий из 842 аминокислот с масса 97,434 кДа в мышечных клетках. Хотя фермент может существовать в виде неактивного мономера или тетрамера, он биологически активен как димер двух идентичных субъединиц.
 R- и T-состояния гликогенфосфорилазы b Tower Helices, слева и справа соответственно. Обратите внимание на относительное расположение спиралей центральной башни, а также на усиление взаимодействий между субъединицами в состоянии R. PDB3CEH, PDB3E3O
R- и T-состояния гликогенфосфорилазы b Tower Helices, слева и справа соответственно. Обратите внимание на относительное расположение спиралей центральной башни, а также на усиление взаимодействий между субъединицами в состоянии R. PDB3CEH, PDB3E3O У млекопитающих основные изоферменты гликогенфосфорилазы обнаруживаются в мышцах, печени и головном мозге. Тип мозга преобладает в головном мозге и эмбриональных тканях взрослого человека, тогда как типы печени и мышц преобладают в печени и скелетных мышцах взрослых, соответственно.
Димер гликогенфосфорилазы имеет много областей биологического значения, включая каталитические сайты, сайты связывания гликогена, аллостерические сайты и обратимо фосфорилированный сериновый остаток. Во-первых, каталитические центры относительно скрыты, на расстоянии 15 Å от поверхности белка и от границы раздела субъединиц. Это отсутствие легкого доступа каталитического сайта к поверхности является значительным, поскольку оно делает активность белка очень чувствительной к регулированию, поскольку небольшие аллостерические эффекты могут значительно увеличить относительный доступ гликогена к сайту.
Возможно, наиболее важным регуляторным сайтом является Ser14, сайт обратимого фосфорилирования, очень близкий к границе раздела субъединиц. Структурное изменение, связанное с фосфорилированием и превращением фосфорилазы b в фосфорилазу a, представляет собой расположение первоначально неупорядоченных остатков с 10 по 22 в α-спирали. Это изменение увеличивает активность фосфорилазы до 25% даже в отсутствие AMP и дополнительно усиливает активацию AMP.
Аллостерический сайт связывания AMP на мышечных изоформах гликогенфосфорилазы близок к интерфейс субблока такой же, как у Ser14. Связывание AMP на этом сайте, соответствующее изменению из состояния T фермента в состояние R, приводит к небольшим изменениям в третичной структуре на границе раздела субъединиц, что приводит к большим изменениям в четвертичной структуре. Связывание AMP поворачивает башни-спирали (остатки 262-278) двух субъединиц на 50 ° относительно друг друга за счет большей организации и межсубъединичных взаимодействий. Это вращение башенных спиралей приводит к повороту двух субъединиц на 10 ° относительно друг друга и, что более важно, нарушает остатки 282-286 (петля 280s), которые блокируют доступ к каталитическому сайту в Т-состоянии, но не в состояние R.
Последний, возможно, самый любопытный сайт в белке гликогенфосфорилазы - это так называемый сайт хранения гликогена. Остатки 397-437 образуют эту структуру, которая позволяет белку ковалентно связываться с цепью гликогена на полных 30 Å от каталитического сайта. Этот сайт, скорее всего, является сайтом, в котором фермент связывается с гранулами гликогена перед инициацией расщепления концевых молекул глюкозы. Фактически, 70% димерной фосфорилазы в клетке существует как связанная с гранулами гликогена, а не свободно плавающая.
| фосфорилаза, гликоген; мышца (синдром Макардла, болезнь накопления гликогена V) | |
|---|---|
| Идентификаторы | |
| Символ | PYGM |
| Ген NCBI | 5837 |
| HGNC | 9726 |
| OMIM | 608455 |
| RefSeq | NM_005609 |
| UniProt | P11217 |
| Другие данные | |
| Номер EC | 2.4.1.1 |
| Locus | Chr. 11 q12-q13.2 |
| фосфорилаза, гликоген; печень (болезнь Hers, болезнь накопления гликогена, тип VI) | |
|---|---|
| Идентификаторы | |
| Символ | PYGL |
| Ген NCBI | 5836 |
| HGNC | 9725 |
| OMIM | 232700 |
| RefSeq | NM_002863 |
| UniProt | P06737 |
| Прочие данные | |
| Номер EC | 2.4.1.1 |
| Locus | Chr. 14 q11.2-24.3 |
| фосфорилаза, гликоген; мозг | |
|---|---|
| Идентификаторы | |
| Символ | PYGB |
| Ген NCBI | 5834 |
| HGNC | 9723 |
| OMIM | 138550 |
| RefSeq | NM_002862 |
| UniProt | P11216 |
| Прочие данные | |
| Номер EC | 2.4.1.1 |
| Locus | Chr. 20 p11.2-p11.1 |
Ингибирование гликогенфосфорилазы было предложено в качестве одного метода лечения диабета 2 типа. Поскольку производство глюкозы в печени, как было показано, увеличивается у пациентов с диабетом 2 типа, ингибирование высвобождения глюкозы из запасов гликогена в печени представляется действенным подходом. Клонирование гликогенфосфорилазы печени человека (HLGP) выявило новый аллостерический сайт связывания рядом с интерфейсом субъединиц, который не присутствует в гликогенфосфорилазе мышц кролика (RMGP), обычно используемой в исследованиях. Этот сайт не был чувствителен к тем же ингибиторам, что и в аллостерическом сайте AMP, и наибольший успех был достигнут при синтезе новых ингибиторов, имитирующих структуру глюкозы, поскольку глюкозо-6-фосфат является известным ингибитором HLGP и стабилизирует менее активное Т-состояние. Эти производные глюкозы продемонстрировали некоторый успех в ингибировании HLGP с прогнозируемыми значениями Ki всего 0,016 мМ.
Мутации в мышечной изоформе гликогенфосфорилазы (PYGM) связаны с болезнью накопления гликогена типа V (GSD V, болезнь Макардла). На сегодняшний день идентифицировано более 65 мутаций в гене PYGM, которые приводят к болезни Макардла. Симптомы болезни Макардла включают мышечную слабость, миалгию и недостаток выносливости, все из-за низкого уровня глюкозы в мышечной ткани.
Мутации в изоформе гликогенфосфорилазы (PYGL) печени связаны с болезнью Херса (болезнь накопления гликогена тип VI ). Болезнь у нее часто связана с легкими симптомами, обычно ограниченными гипогликемией, и иногда ее трудно диагностировать из-за остаточной активности ферментов.
Была предложена изоформа гликогенфосфорилазы (PYGB) мозга как биомаркер для рака желудка.
Гликогенфосфорилаза регулируется посредством аллостерического контроля и посредством фосфорилирования. Каждая из фосфорилазы а и фосфорилазы b существует в двух формах: Т (напряженное) неактивное состояние и R (расслабленное) состояние. Фосфорилаза b обычно находится в состоянии T, неактивна из-за физиологического присутствия АТФ и глюкозо-6 фосфата, а фосфорилаза a обычно находится в состоянии R (активна). Изофермент гликогенфосфорилазы существует в печени, чувствительной к концентрации глюкозы, поскольку печень действует как экспортер глюкозы. По сути, фосфорилаза печени реагирует на глюкозу, что вызывает очень чувствительный переход от R к T-форме, инактивируя ее; кроме того, фосфорилаза печени нечувствительна к АМФ.
Гормоны, такие как адреналин, инсулин и глюкагон, регулируют гликогенфосфорилазу с помощью систем амплификации второго мессенджера, связанных с G-белками. Глюкагон активирует аденилатциклазу через G-белок-связанный рецептор (GPCR), связанный с Gs, который, в свою очередь, активирует аденилатциклазу для увеличения внутриклеточных концентраций цАМФ. цАМФ связывается с протеинкиназой A (PKA) и активирует их. PKA фосфорилирует киназу фосфорилазы, которая, в свою очередь, фосфорилирует гликогенфосфорилазу b по Ser14, превращая ее в активную гликогенфосфорилазу a.
В печени глюкагон также активирует другой GPCR, который запускает другой каскад, что приводит к активации фосфолипазы C (PLC). PLC косвенно вызывает высвобождение кальция из эндоплазматического ретикулума гепатоцитов в цитозоль. Повышенная доступность кальция связывается с субъединицей кальмодулина и активирует киназу гликогенфосфорилазы. Киназа гликогенфосфорилазы активирует гликогенфосфорилазу таким же образом, как упоминалось ранее.
Гликогенфосфорилаза b не всегда неактивна в мышцах, поскольку она может аллостерически активироваться AMP. Повышение концентрации АМФ во время физических упражнений сигнализирует о потребности в энергии. АМФ активирует гликогенфосфорилазу b, изменяя ее конформацию с напряженной на расслабленную. Эта расслабленная форма имеет такие же ферментативные свойства, что и фосфорилированный фермент. Увеличение концентрации АТФ противодействует этой активации, вытесняя АМФ из сайта связывания нуклеотидов, что указывает на наличие достаточных запасов энергии.
После приема пищи происходит высвобождение инсулина, сигнализирующего о наличии глюкозы в крови. Инсулин косвенно активирует протеинфосфатазу 1 (PP1) и фосфодиэстеразу через каскад передачи сигнала. PP1 дефосфорилирует гликогенфосфорилазу a, реформируя неактивную гликогенфосфорилазу b. Фосфодиэстераза превращает цАМФ в АМФ. Вместе они снижают концентрацию цАМФ и ингибируют ПКА. В результате PKA больше не может инициировать каскад фосфорилирования, который заканчивается образованием (активной) гликогенфосфорилазы a. В целом, передача сигналов инсулина снижает гликогенолиз для сохранения запасов гликогена в клетке и запускает гликогенез.
Гликогенфосфорилаза была первым обнаруженным аллостерическим ферментом. Он был изолирован, и его активность подробно охарактеризована Карлом Ф. Кори и Герти Т. Кори. Арда Грин и Герти Кори кристаллизовал его впервые в 1943 году и проиллюстрировал, что гликогенфосфорилаза существует либо в форме a, либо в форме b в зависимости от ее состояния фосфорилирования, а также в состояниях R или T в зависимости от присутствия AMP.
| На Wikimedia Commons есть материалы, связанные с гликогенфосфорилазой. |