Глоссарий химических терминов
редактировать
Список определений терминов и понятий, обычно используемых при изучении химии
Этот глоссарий химических терминов - это список терминов и определений, относящихся к химии, включая химические законы, диаграммы и формулы, лабораторные инструменты, посуду и оборудование. Химия - это физическая наука, изучающая состав, структуру и свойства материи, а также изменения, которым она претерпевает во время химических реакций ; он отличается обширным словарным запасом и значительным количеством жаргона.
Примечание: Все ссылки на периодическую таблицу относятся к стилю IUPAC Периодической таблицы.
Содержание:
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
A
- абсолютный ноль
- Теоретическое условие, относящееся к системе при нижнем пределе термодинамической температуры Шкала или ноль кельвина, при которой система не излучает и не поглощает энергию (т. Е. Все атомы находятся в состоянии покоя). Путем экстраполяции закона идеального газа, международно согласованное значение для абсолютного нуля было определено как -273,15 ° C (-459,67 ° F; 0,00 K).
- поглощение
- поглощение
- 1. Физический или химический процесс, при котором вещество в одном состоянии включается и удерживается другим веществом в другом состоянии. Абсорбция отличается от адсорбции тем, что первое вещество проникает через весь объем второго вещества, а не просто прилипает к поверхности.
- 2. процесс, с помощью которого материя (обычно электроны связанные в атомах) принимает энергию электромагнитного излучения и преобразует ее в любой из различных типов внутренней энергии, например как тепловая энергия. Этот тип поглощения является принципом, на котором основана спектрофотометрия.
- изобилие
- точность
- Насколько близко измеренное значение к фактическому или истинному значению. Сравните прецизионность.
- кислота
- Соединение, которое при растворении в воде дает pH менее 7,0 или отдает ион водорода.
- ангидрид кислоты
- Соединение с двумя ацильными группами, связанными с одним атомом кислорода.
- константа диссоциации кислоты (Ka)
- Количественная мера силы кислоты в раствор, выраженный как константа равновесия для химической диссоциации реакции в контексте кислотно-основных реакций. Его часто называют его одекологарифмом по основанию 10, pK a.
- актинидов
- периодическая серия металлических элементов с атомными номерами от 89 до 103, от актиний до Лоуренсий.
- активированный комплекс
- Структура, которая образуется из-за столкновения между молекулами при образовании новых связей.
- энергия активации
- Минимальная энергия, которая должна быть доступна химической системе с потенциальными реагентами, чтобы вызвать химическую реакцию.
- ряд активности
- См. ряд реактивности.
- фактический выход
- ациклический
- Содержащий только линейные структуры атомов (в частности, в углеводородах).
- реакции присоединения
- В органической химии, когда две или более молекулы объединяются, чтобы образовать большую.
- адгезия
- Тенденция разнородных частиц или поверхностей прилипать к друг друга в результате межмолекулярных сил. Контраст когезия.
- адсорбция
- Химическая адгезия атомов, ионы или молекулы одного вещества (либо газ, жидкость, или растворенное твердое вещество) на поверхность другого вещества, в результате чего образуется пленка из первого вещество слабо связано с границей раздела между двумя веществами. Адсорбция отличается от абсорбции тем, что она является исключительно поверхностным явлением, в то время как абсорбция включает целые объемы материалов.
- аэрация
- Смешивание воздуха с жидкостью или твердый.
- спирт
- Любое органическое соединение, состоящее из гидроксильной функциональной группы, присоединенной к насыщенному атому углерода.
- альдегид
- Любое органическое соединение, состоящее из карбонильной группы, присоединенной к атому водорода, и любого другого R-группы.
- щелочного металла
- Любого из металлов элементы, принадлежащие группе 1 таблицы Менделеева : литий (Li), натрий (Na), калий (K), рубидий (Rb), цезий (Cs) и франций (Fr).
- щелочноземельный металл
- Любой из металлических элементов, относящихся к группе 2 периодической таблицы : бериллий (Be), магний (Mg), кальций (Ca), s тронций (Sr), барий (Ba) и радий (Ra).
- алкан
- Любой насыщенный ациклический углеводород.
- алкен
- Ненасыщенный углеводород, содержащий по меньшей мере одну пару атомов углерода с двойной связью.
- Алкильная группа
- Функциональная группа, состоящая из алкана, отсутствует атом водорода.
- алкин
- Ненасыщенный углеводород, содержащий по крайней мере одну пару углеродов с тройной связью.
- алломер
- Вещество, которое отличается по химическому составу состав, но имеет ту же кристаллическую структуру, что и другое вещество.
- аллотроп
- Элементы, которые могут иметь разные структуры (и, следовательно, разные формы), такие как углерод (алмазы, графит и фуллерен ).
- сплав
- A смесь из металлов или металла и другого элемента которые в сочетании демонстрируют характер металлического соединения. Общие примеры включают бронзу, латунь и оловянную.
- амальгаму
- Любой сплав из ртути с другим металл.
- количество вещества
- Количество дискретных частиц (например, молекул, атомов, ионов, электронов или любой другой объект атомарного масштаба) в данном образце материи, деленный на константу Авогадро. СИ базовой единицей количества вещества является моль (моль).
- аналит
- аналитическая химия
- Раздел химии, изучающий и использующий инструменты и методы разделения, количественного определения и идентификации химических веществ, как с помощью классических методов влажной химии, таких как осаждение, экстракция, дистилляция, и наблюдательный анализ, а также с помощью современных инструментальных методов, таких как хроматография, спектроскопия и электрохимия.
- анион
- Отрицательно заряженный ион. Т.е. атом, у которого больше электронов по сравнению с протонами.
- анод
- 1. Электрод, через который обычный электрический ток (поток положительных зарядов) входит в поляризованную электрическую цепь.
- 2. Проволока или пластина электрохимического элемента, имеющая избыточный положительный заряд. Отрицательно заряженные анионы всегда движутся к аноду. Контрастный катодный.
- водный раствор
- A раствор, в котором растворитель представляет собой воду. В химических уравнениях он обозначается добавлением (aq) к химической формуле.
- ароматичность
- Химическое свойство сопряженных колец атомов, например бензол, что приводит к необычно высокой стабильности.. Такие кольца называются ароматическими.
- стрелка, указывающая на
- арил
- Любая функциональная группа или заместитель, производный от ароматического кольца, например как фенил или нафтил. Символ Ar часто используется в качестве заполнителя для общей арильной группы на структурных схемах.
- атом
- Химический элемент в его наименьшей форме, состоящий из протонов и нейтронов внутри ядра и электроны, вращающиеся вокруг ядра.
 атом с протонами, нейтронами и электронами помечено
атом с протонами, нейтронами и электронами помечено - атомная масса
- масса атома, обычно выражаемая в унифицированных атомных единицах массы и почти эквивалентная массовое число.
- атомная единица массы
- См. унифицированную атомную единицу массы.
- атомный номер (Z)
- Число протонов, обнаруженных в ядре атома данного химического элемента. Он идентичен зарядному числу ядра и используется в периодической таблице для однозначной идентификации каждого химического элемента.
- атомная орбиталь
- Любая область, в которой один или больше электронов можно найти в отдельном атоме (в отличие от молекулы).
- атомный радиус
- атомная масса
- средняя атомная масса
- Закон Авогадро
- Число Авогадро
- Количество отдельных составляющих частиц (например, молекул, атомов или ионов) в одном моль вещества, определяемого как точно 6,02214076 × 10 таких частиц.
- азеотроп
- A смесь жидкостей, состав которых не изменяется при дистилляции.
Содержание:
- Top
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
B
- барометр
- Устройство, используемое для измерения атмосферного давления.
- base
- Вещество, которое принимает протон и имеет pH выше 7,0. Типичный пример - sodiu м. гидроксид (NaOH).
- базовый ангидрид
- Оксиды металлических элементов I и II групп.
- стакан
- Цилиндрический сосуд или контейнер с плоским дном, чаще всего тип стеклянная посуда, широко используемая в лабораториях для различных целей, таких как подготовка, хранение, хранение, сбор или объемное измерение химических веществ, образцов или растворов, или как камера, в которой химическая реакция происходит. Стаканы отличаются от колб тем, что у них прямые, а не наклонные стороны; у большинства мензурок также есть небольшой носик на ободке для облегчения разливания.
- Закон Бера – Ламберта
- биохимия
- Исследование химии биологических систем и организмов.
- Модель Бора
- кипение
- См. испарение.
- точка кипения
- Температура, при которой вещество меняет состояние с жидкости на газ (или пар). Это зависит от давления и обычно указывается для данного вещества при стандартных условиях.
- повышение точки кипения
- процесс, при котором температура кипения повышается путем добавления вещества
- связки.
- Любое постоянное притяжение между атомами, ионами или молекулами, которое делает возможным образование химических соединений. Связи создаются в результате широкого спектра электрохимических сил, сила которых может значительно различаться; они разрушаются, когда эти силы преодолеваются другими силами. Типы, прочность и количество связей, удерживающих вместе химические вещества, определяют структуру и объемные свойства материи.
- закон Бойля
- Для данной массы газа при постоянной температуре объем изменяется обратно пропорционально давлению.
- Закон Брэгга
- Броуновское движение
- Кислота Бренстеда – Лоури
- Любые химические соединения, которые легко отдают протон.
- реакция кислоты – основания Бренстеда – Лоури
- Основание Бренстеда – Лоури
- Любые химические соединения, которые легко принимают протон.
- колба Бюхнера
- буферный раствор
- водный раствор, состоящий из слабой кислоты и ее конъюгат основания или слабого основания и его конъюгированной кислоты, который сопротивляется изменениям pH при добавлении сильных кислот или оснований.
- bumping
- Явление, при котором гомогенная жидкость, повышенная до своей точки кипения, становится перегретой и после зародышеобразования быстро переходит в газовую фазу, что приводит к сильному выбросу ион жидкости из емкости; в крайнем случае может треснуть сама тара. Частое перемешивание, использование подходящей емкости и использование кипяченой стружки может помочь предотвратить удары.
- пробка
- бюретка
- Стеклянная посуда, используемая для выдачи определенного количества жидкости, когда необходима точность (например, во время титрования и зависимых от ресурсов реакций).
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Литература
- Внешние ссылки
C
- калориметр
- Устройство, используемое для измерения тепла.
- карбанион
- карбокатион
- катализатор
- Любой элемент или соединение, которое способствует увеличению скорости химическая реакция, но которая не расходуется и не разрушается во время реакции. Считается как реагентом, так и продуктом реакции.
- катод
- An электрод, от которого обычный электрический ток (поток положительных зарядов) выходит из поляризованной электрической цепи. Положительно заряженные катионы всегда движутся в сторону катод, хотя катод Полярность оды может быть положительной или отрицательной, в зависимости от типа электрического устройства и способа его эксплуатации. Контраст анод.
- катион
- Положительно заряженный ион.
- центрифугирование
- Лабораторный метод, который включает приложение центробежной силы для отделения частиц от раствора в соответствии с их размер, форма и плотность. Более крупные и / или более плотные вещества мигрируют от оси центрифуги, в то время как более мелкие и / или менее плотные вещества мигрируют к оси.
- центрифуга
- Устройство, используемое для разделения веществ в зависимости от размера, форма и плотность посредством центрифугирования или вращения сосудов, содержащих вещества, вокруг центрированной оси с чрезвычайно высокими скоростями.
- потенциал ячейки
- Сила в гальваническом элементе, который притягивает электроны через восстановитель к окислителю.
- цепная реакция
- число заряда
- A квантованное значение электрического заряда, рассчитанное как электрический заряд в кулонах деленное на константу элементарного заряда, или z = q / e. Зарядные числа для ионов обозначены в верхнем индексе (например, Na обозначает ион натрия с положительным числом зарядов). Атомные номера представляют собой зарядовые числа атомных ядер.
- Закон Чарльза
- Когда давление на образец сухого газа поддерживается постоянным, температура Кельвина прямо пропорциональна его объему.
- хелатирующий агент
- хелатирование
- Тип связывания, включающий образование двух отдельных координационных ковалентных связей между полидентатным лигандом и единственный центральный металлический ион. Лиганд обычно представляет собой органическое соединение, называемое хелатирующим агентом или хелатирующим агентом.
- химический состав
- Идентичность и относительное количество элементов, составляющих химическое соединение, которое часто можно выразить с помощью химической формулы.
- химическое разложение
- Разрушение отдельной частицы или объекта (например, молекулы или реакционноспособный промежуточный продукт) на два или более фрагмента, или химическая реакция, в которой два или более продукта образуются из одного реагента. Контраст химический синтез.
- химическая формула
- Любой из различных способов краткого отображения информации о химическом составе соединения или молекулы с использованием буквы, цифры и / или типографские символы. Химические формулы, такие как эмпирические и молекулярные формулы, могут указывать только на идентичность и числовые пропорции атомов в соединении и поэтому имеют более ограниченную описательную силу, чем химические названия и структурные формулы.
- химический закон
- A закон природы, относящийся к химии, например, закон сохранения массы.
- химическая номенклатура
- химический процесс
- 1. Любой метод или средство изменения одного или нескольких химических веществ или химических соединений любым способом, естественным или искусственным, спонтанно или под действием внешних сил.
- 2. В химической инженерии - любой метод, используемый в промышленном масштабе (особенно в производстве ) для изменения состава одного или нескольких химических веществ или материалов.
- химическая реакция
- Изменение из одного или нескольких веществ в одно или несколько разных веществ.
- химические соединения
- A химические вещества или совокупность веществ, состоящих из химически идентичных молекулярных объектов, которые можно исследовать один и тот же набор уровней молекулярной энергии в характерной или обозначенной шкале времени.
- химическое вещество
- Форма вещества, имеющая постоянный химический состав и характерные свойства и которые нельзя разделить на более простые компоненты чисто физическими методами (т.е. без разрыва химических связей). Его часто называют чистым веществом, чтобы отличить его от смеси.
- химический синтез
- Искусственное выполнение одной или нескольких химических реакций с целью получения одного или нескольких продуктов.. В современных лабораторных условиях конкретные химические синтезы надежны и воспроизводимы.
- химия
- Научная дисциплина, изучающая химические вещества, соединения и молекулы состоящий из атомов различных химических элементов, а также их состава, структур, свойств, поведения и изменений, которым они претерпевают во время реакций с другими веществами.
- хиральность
- хроматография
- цис-транс-изомерия
- закрытая система
- кластер
- когезия
- Тенденция одинаковых частиц или поверхностей прилипать друг к другу, как результат межмолекулярных сил. Контраст адгезия.
- коллигативное свойство
- Любое свойство раствора, которое зависит от отношения количества растворенных частиц к количеству растворителя частиц в растворе, а не от природы присутствующих химических соединений.
- коллоидная
- A смесь равномерно диспергированных веществ, таких как многие молоко.
- горение
- экзотермическая реакция между окислителем и топливом, которое выделяет большое количество тепла и часто света.
 Пример горение
Пример горение - Комиссия по изотопному содержанию и атомному весу (CIAAW)
- сжатие
- Область в продольной волне, где частицы приближаются и вдавливаются внутрь.
- соединение
- A вещество который состоит из двух или более химически связанных элементов.
- концентрация
- Содержание компонента смеси, деленное на общий объем смеси. В химии широко используются несколько различных определений концентрации, включая массовая концентрация, объемная концентрация и молярная концентрация.
- конденсация
- Фазовый переход вещества из газа в жидкость.
- condosity
- Определено сравнительное измерение электрической проводимости раствора раствора. как молярная концентрация раствора хлорида натрия (NaCl), который имеет такую же удельную электрическую проводимость, что и тестируемый раствор. Обычно он выражается в единицах моль на литр (или на какую-либо другую единицу объема).
- проводник
- Любой объект или материал, который позволяет течь электрический ток в одном или нескольких направлениях. Контраст изолятор.
- конформация
- Пространственное расположение атомов, дающее различие между стереоизомерами, которые могут быть взаимно преобразованы вращениями вокруг формально одинарных связей.
- сопряженная кислота
- сопряженное основание
- сопряженная система
- кривая охлаждения
- координированная химия
- координационная ковалентная связь
- координационный комплекс
- коррозия
- Необратимая межфазная химическая реакция материала с окружающей средой что приводит к расходу материала или растворению в материале внешнего компонента окружающей среды.
- кулон
- Единица SI электрического заряда (символ: C), определяемый как заряд, переносимый постоянным током в один ампер за одну секунду.
- ковалентной связью
- A связью, которая включает разделение электронных пар между атомами. Стабильный баланс сил притяжения и отталкивания, возникающий между атомами, когда они разделяют электроны, известен как ковалентная связь.
 Двухатомная молекула водорода, H 2 (справа), образована ковалентной связь, когда два одиночных атома водорода разделяют два электрона
Двухатомная молекула водорода, H 2 (справа), образована ковалентной связь, когда два одиночных атома водорода разделяют два электрона - критическая точка
- Конечная точка фазы кривой равновесия или давление - температура кривая, при которой условия таковы, что границы фаз исчезают и различные фазы вещества, такие как жидкость и пар, могут сосуществовать. Критическая точка определяется пересечением критической температуры T c и критического давления p c ; выше этой температуры и давления все различия между фазами исчезают, и вещество становится сверхкритическим флюидом.
- кристаллом
- A твердым телом, составляющие частицы которого (такие как атомы, ионы или молекулы) расположены упорядоченно периодическая микроскопическая структура, образующая решетку, которая простирается во всех направлениях. Такие материалы часто называют кристаллическими.
- кристаллография
- Раздел химии, связанный с определением расположения атомов в кристаллических твердых телах.
- кювета
- Тип стеклянной посуды, использованной в спектроскопических экспериментах. Обычно он сделан из пластика, стекла или кварца и должен быть как можно более чистым и прозрачным.
Содержание:
- Вверху
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
D
- d-блок
- деионизация парциальных давлений Дальтона
- деионизация
- Удаление первой, а в случае воды, минеральных наиболее, таких как натрий, железо и закон кальций.
- расплывчатость
- Сродство вещества к воде, часто характеризующееся его тенденцией поглощать влагу из атмосферы с образованием водных водных растворов. Наиболее сильно расплывающиеся вещества - это соли, такие как хлорид кальция и карбонат калия.
- делокализованный электрон
- Любой электрон в молекуле, ион, или твердый металл, не соединение с атомом или ковалентной связью. Термин может относиться к электронам, участвующим в резонансе в сопряженных системах или ароматических соединенийх; к свободным электронам, которые способствуют электропроводности ; или электронам внутри делокализованных молекулярных орбиталей, охватывающих несколько соседних элементов.
- плотность
- интенсивное свойство вещества, определяемое как масса на единицу объем и выражается уравнением d = m / V
- дентальность
- Количество донорных групп в одном лиганде, связываются с центральным атомом в сочетании комплекс.
- зависимая переменная
- отложение
- Оседание частиц в растворе или смеси.
- колба Дьюара
- см. вакуумная колба.
- двухатомная
- Состоит из двух элементов, из одинаковых или разных элементов. Контрастная одноная и многоатомная.
- двухатомная молекула
- Любая молекула, состоящая только из двух элементов, одинаковых или разных элементов.
- диффузия
- Суммарное перемещение элементами или молекул из области более высокой концентрации в области более низкой концентрации. Диффузия обусловлена градиентом химического диффундирующих частиц и зависит от случайного блуждания частиц; Следовательно, это приводит к смешиванию или переносу массы без необходимого направленного объемного движения.
- димер
- олигомер, состоящий из двух мономеров, соединенных химическими связями, которые могут быть в разной степени сильными или слабыми, ковалентный или межмолекулярный. Гомодимер состоит из двух идентичных молекул; гетеродимер состоит из двух разных молекул.
- диполярная связь
- диполь
- электрическое или магнитное разделение зарядов.
- дипольный момент
- полярность полярной ковалентной связи.
- дисперсия
- Система, в которой частицы одного материала распределены в непрерывной фазе другого материала; две фазы могут находиться в одном и том же или в разных состояниях материи. Дисперсии частиц, достаточно большие для седиментации, называются суспензиями, более мелкие частицы называются коллоидами или растворами.
- диссоциацией
- растворением
- Взаимодействие растворителя с молекулами или ионами растворенного вещества, включая образование связи, водородную связь и силы Ван-дер-Ваальса.
 Ион натрия ( Na) образует сольватационный комплекс с молекулами воды при растворении в водном растворе
Ион натрия ( Na) образует сольватационный комплекс с молекулами воды при растворении в водном растворе - дистилляция
- Процесс разделения компонентов жидкости смесь путем использования различных в относительной летучести компонентов посредством смесей избирательного кипячения и предыдущей конденсации. Аппарат, использованное для перегонки вещества, называется дистилляцией, повторно конденсированное вещество, полученное в процессе, называется дистиллятом.
- двойная связь
- A связь, включающая ковалентное совместное использование двух пары электронов.
- реакция двойного за ущерб
- пластичность
- Мера способности материала претерпевать значительную пластическую деформацию перед разрывом, обычно проявляется как процент удлинения или процент уменьшения площади при испытании на растяжение и обычно проявляется способностью вытягивания материала в проволоку.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. также
- Ссылки
- Внешние ссылки
E
- заземленный металл
- См. щелочноземельный металл.
- электрический заряд
- Измеренное свойство (кулоны), определяющее которое электромагнитное взаимодействие.
- раствор электролита
- A, проводит определенное количество электрического тока и может быть категорически разделен на слабые и сильные электролиты.
- электрохимическая ячейка
- Usi При токе химической реакции создается электродвижущая сила.
- электромагнитное излучение
- Тип волны, которая может проходить через вакуум, а также через материал, и классифицируется как самораспространяющаяся волна.
- электромагнитный спектр
- электромагнетизм
- Поля с электрическим зарядом и электрическими свойствами, которые изменяют свойства движения и частиц частиц.
- электродвижущая сила (ЭДС)
- электрон
- Тип субатомная частица с отрицательным суммарным зарядом.
- электронная конфигурация
- Распределение электронов в атоме или молекуле в пределах атомных или молекулярных орбиталей. Обширная система обозначений используется для краткого и однозначного представления информации об электронной конфигурации каждого вида элементов. Знание специфического расположения электронов в различных атомах для понимания химические связи и организации периодической таблицы элементов.
- дефицит электронов
- пары электронов
- Два электронов, которые занимают ту же самую молекулярную орбиталь, но имеют противоположные спины . Электронные пары образуют химические связи или встречаются как неподеленные пары из валентных электронов ; также возможно, чтобы электроны возникли индивидуально как неспаренные электроны.
- электронная оболочка
- орбиталь вокруг ядра атома, который содержит фиксированное количество электронов (обычно два или восемь).
- электроотрицательность (χ )
- Химическое свойство, которое является тенденцию атома притягивать общую пару из электронов (или плотность электронов) к себе. На электроотрицательность атома влияет как его заряд ядра (который пропорционален количеству протонов в его ядре), так и количество и расположение присутствующих электронов. в его атомных оболочках (что влияет на ядро от валентных электронов). Чем выше электроотрицательность атома или заместителя, тем больше он притягивает к себе электроны. Как обычно рассчитывают, электроотрицательность не только атома, но, скорее, атома внутри молекулы ; поэтому он меняется в зависимости от химического окружения элемента, хотя обычно считается передаваемым своим.
- электрофилом
- Любой атом или молекула, которые могут принимать электронные пару. Большинство электрофилов несут чистый положительный заряд, включая атом, несущий частичный положительный заряд, или включает нейтральный атом, который не имеет полного октета электронов, и поэтому они притягивают электроны. богатые регионы других видов; электрофил с вакантными орбиталями может принимать электронную пару, подаренную нуклеофилом, создавая химическую связь между двумя видами. Они принимают электроны, электрофилы по определению являются кислотами Льюиса.
- электросинтез
- элемент
- Вид элементы, имеющие такое же количество протонов в своих атомных ядрах и, следовательно, тот же атомный номер. Химические элементы составляют всю обычную материю вселенной; 118 элементов были идентифицированы и сгруппированы по их различным химическим свойствам в периодической таблице элементов.
- элементарная реакция
- Любая химическая реакция, в которой один или несколько химических соединений непосредственно непосредственно реагируют с образованием продуктов на одной стадии реакции и с одним переходным состоянием, то есть без каких-либо промежуточных соединений. Контраст ступенчатая реакция.
- энантиомер
- энантиоморф
- эндотермический процесс
- энергия
- Способность системы выполнять работу.
- энплетия
- См. количество вещества.
- энтальпия
- Мера общей внутренней энергии термодинамической системы, обычно обозначаемая H.
- энтальпия плавления
- энтропия
- Количество энергии, недоступное для работа в замкнутой термодинамической системе, обычно обозначаемой S.
- химия окружающей среды
- фермент
- Биологический белок катализатор, который ускоряет химическую реакцию.
- эмпирическая формула
- Дает простейшее целочисленное отношение атомов каждого элемента, присутствующего в соединении.
- равновесие
- В целом, это состояние системы, в которой все конкурирующие влияния уравновешены. Химическое равновесие - это состояние, при котором концентрации реагентов и продуктов перестали изменяться во времени.
- Пробирка Эппендорфа
- Обобщенное и зарегистрированное название, используемое для обозначения пробирки для микроцентрифуги.
- колба Эрленмейера
 500-миллилитровая колба Эрленмейера
500-миллилитровая колба Эрленмейера - экзотермический процесс
- обширное свойство
- A физическая величина, значение которой пропорционально размеру описываемой системы или количеству материи в системе. Примеры включают массу, объем, энтальпию и энтропию. Контраст интенсивное свойство.
- извлечение
- внешнее свойство
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
F
- f-блок
- замерзание
- фазовый переход вещества из жидкости в твердое тело.
- постоянная Фарадея
- единица электрического заряда, широко используемый в электрохимии, который представляет 1 моль из электронов : 6,022 × 10 электронов. Он равен примерно 96 500 кулонам (F = 96 485,339 9 (24) Кл / моль).
- Законы электролиза Фарадея
- Набор двух законов, относящихся к электролизу которые утверждают, что: а) масса вещества, измененного на электроде во время электролиза, прямо пропорциональна количеству электричества, переданного на этом электроде; и б) масса элементарного материала, измененного на электроде, прямо пропорциональна эквивалентному весу элемента.
- Законы диффузии Фика
- фильтрация
- Любая физическая, биологическая или химическая операция, которая разделяет крупные частицы (часто твердое вещество вещество) из более мелких частиц (часто жидкость) путем пропускания смеси через сложную решетчатую структуру, через которую могут проходить только частицы достаточно малого размера, называемую фильтром. Жидкость и мелкие частицы, которые успешно проходят через фильтр, называются фильтратом.
- реакция первого порядка
- колба
- Сосуд или контейнер, чаще всего тип стеклянной посуды, широко используемый в лабораториях для различных целей, таких как подготовка, хранение, хранение, сбор или объемное измерение химикатов, образцов или растворов, или в качестве камеры, в которой протекает химическая реакция. Колбы бывают разных форм и размеров, но обычно характеризуются более широким «корпусом» сосуда и одной или несколькими более узкими трубчатыми секциями с отверстием вверху.
- формальный заряд (FC)
- электрический заряд, присвоенный атому в молекуле, при условии, что все электроны во всех связях равномерно распределены между атомов, независимо от относительной электроотрицательности каждого атома. Формальный заряд любого атома, входящего в состав молекулы, можно рассчитать по уравнению
 , где
, где  - количество валентных электронов нейтрального атома в его основном состоянии;
- количество валентных электронов нейтрального атома в его основном состоянии;  - количество валентных электронов атома, не участвующих в связях в молекуле; и
- количество валентных электронов атома, не участвующих в связях в молекуле; и  - количество электронов, связанных с другими атомами в молекуле.
- количество электронов, связанных с другими атомами в молекуле. - фракционная дистилляция
- свободный радикал
- См. радикал.
- депрессия точки замерзания
- точка замерзания
- Температура температуры, при которой вещество меняет состояние с жидкости на твердое вещество. Поскольку замерзание противоположно плавлению, точка замерзания вещества идентична его точке плавления, но по соглашению только точка плавления называется характеристическое свойство вещества.
- частота
- Измерение количества циклов данного процесса в единицу времени. Блок SI для м Частота измерения - герц (Гц), с 1 Гц = 1 цикл в секунду.
- функциональная группа
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. также
- Ссылки
- Внешние ссылки
G
- гальванический элемент
- Тип батареи, состоящей из электрохимических веществ с двумя разными металлами, соединенными солевым мостиком.
- газом
- Один из четырех основных состояний вещества, характеризующихся высокоэнергетическими частями, которые заполняют свой контейнер, но не имеют формы или объема.
- газовая хроматография
- Тип хроматографии обычно используется в аналитической химии для выделения и анализа химических соединений, которые могут быть испарены без разложения. Газовая хроматография часто используется для проверки чистоты веществ, идентификации неизвестных веществ и измерений различных компонентов компонентов смесей.
- закон Гей-Люссака
- Химический закон, используемый для каждого из двух отношений, выведенных французским химиком Жозефом Луи Гей-Люссаком и имеющими свойства газов, хотя это название чаще используется к его закону территории области.
- геохимия
- Изучение геохимии химия и химический состав Земли и геологические процессы.
- энергиябса
- Значение, указывающее на спонтанность Гибкости. Обычно обозначается как G.
- стекло
- грамм-атом
- Один грамм-атом составляет как совокупность 6,023X10 ^ 23 атомов.
- Реакция Гриньяра
- соединение матового стекла
- Устройство, предназначенное для быстрой и простой сборки двух частей герметичной стеклянной посуды вместе, с поверхностью матового стекла и, как правило, с коническим конусом на заказ.
- группа
- Вертикальный столбец периодической таблицы элементы и элементы, которые разделяют его. Контраст период.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
H
- галоген
- Любой из пяти не- металлические элементы из Группы 17 таблицы Менделеева : фтор (F), хлор (Cl), бром (Br), йод (I) и астатин (У).
- адрон
- Субатомные части типа, включая барионы и мезоны, которые могут принимать участие в сильном взаимодействии.
- тепло
- Энергия, передаваемая от одной системы к другому посредством теплового взаимодействия.
- теплота плавления
- См. энтальпия плавления.
- закон Генри
- Гесса постоянного суммирования тепла
- Закон физической химии, который гласит, что общий закон энтальпия изменение в ходе одинаково, независимо от того, завершается ли реакция в одну или несколько стадий.
- Правила Хунда
- гидрат
- Любое вещество, содержащее воду или ее составляющие элементы или любое соединение, образованное добавление воды или ее элементов в другую молекуле.
- реакция гидратации
- водород
- водородная связь
- Форма электростатического взаимодействия между электроотрицательным атомом и атомом водорода, проигрывает со вторым электроотрицательным атомом. Водородная связь уникальна, потому что небольшой размер водорода допускает близость взаимодействующих электрических зарядов и может возникать как межмолекулярная или внутримолекулярная сила.
- гидрирование
- гидролиз
- Разрыв химической связи добавлением воды.
- гигроскопия
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
I
- идеальный газ
- постоянная идеального газа
- Константа пропорциональности в законе идеального газа, определенная как 0,08206 L·атм /(K·моль).
- закон идеального газа
- A химический закон, который гласит, что объем газа пропорционален количеству газа и его Кельвину температура и обратно пропорциональна его.
- идеальный раствор
- A раствор, для которого газовая фаза проявляет термодинамические свойства, аналогичные свойстваам смеси идеальных газов.
- независимая переменная
- показатель
- К раствору добавлено специальное соединение, меняющее цвет в зависимости от кислотности раствора. Различные индикаторы имеют разный цвет и эффективны в разных диапазонах pH.
- индуцированная радиоактивность
- радиоактивность, вызванная бомбардировкой стабильного изотопа элементарными частями, образующими радиоактивный изотоп
- инертный
- неорганический соединение
- Любое химическое соединение, не содержащееся углерода, за исключением случаев. Контраст органическое соединение.
- неорганическая химия
- Раздел химии, касающийся химических свойств и свойств неорганических соединений. Контраст органическая химия.
- изолятор
- Любой материал, противодействующий прохождение электрическому току. Контраст проводник.
- интенсивное свойство
- A физическая величина, значение которого не зависит от размера системы или количества вещества, для которого оно измеряется. Примеры включают плотность, температуру и давление. Контраст обширное свойство.
- межмолекулярная сила
- Международная система единиц (SI)
- Международный союз теоретической и прикладной химии (IUPAC)
- Международная федерация химиков, признан мировым авторитетом в разработке стандартов химической номенклатуры и других методологий в химии.
- внутримолекулярная сила
- внутреннее свойство
- ион
- A молекула, которая приобрела или потеряла или более электронов из своего нейтрального состояния и, следовательно, его отрицательным или положительным электрический заряд.
- ионной связью
- Электростатическое притяжение между противоположно заряженными ионами.
 An ионная связь между атомом натрия (Na) и атомом фтора (F). Атом натрия теряет свой единственный валентный электрон (оставляя атом с положительным электрическим зарядом ), а атом фтора приобретает этот же электрон в результате экзотермического процесса ( придавая атому отрицательный электрический заряд). Противоположно заряженные ионы затем притягиваются друг к другу с образованием нового соединения, называемого фторидом натрия.
An ионная связь между атомом натрия (Na) и атомом фтора (F). Атом натрия теряет свой единственный валентный электрон (оставляя атом с положительным электрическим зарядом ), а атом фтора приобретает этот же электрон в результате экзотермического процесса ( придавая атому отрицательный электрический заряд). Противоположно заряженные ионы затем притягиваются друг к другу с образованием нового соединения, называемого фторидом натрия.- ионизация
- Распад химического соединения на отдельные ионы.
- изоэлектронность
- Явление двух или более химических соединений (атомов, молекул, ионов и т. Д.) состоящий из разных элементов, но имеющих одинаковое количество валентныхэлектронов и одинаковое структурное расположение (то есть одинаковое количество атомов с одинаковой связностью). Изоэлектронные частицы обычно демонстрируют полезную последовательность и предсказуемость своих химических свойств.
- изомеризация
- изомеры
- Ионы или молекулы с идентичными химическими формулами, но с разными структурами или пространственные договоренности. Изомеры не обязательно обладают схожими свойствами. Двумя основными типами изомеров являются структурные изомеры и стереоизомеры.
- изотоп
- Вариант определенного химического элемента, который отличается количеством нейтронов. присутствует в ядре. Все изотопы данного элемента имеют одинаковое количество протонов в каждом атоме.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
J
- джоуль (Дж)
- Единица СИ для энергии (символ: Дж). Один джоуль определяется как один Ньютон - метр.
K
- кельвин (K)
- Базовая единица СИ для температуры ( символ: K). Шкала Кельвина - это шкала абсолютной термодинамической температуры, в которой в качестве нулевой точки используется абсолютный ноль.
- кетон
- Органическое соединение с карбонильной группой между двумя атомами углерода.
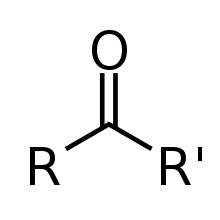 Формула скелета для общего кетона, где R и R 'обозначают переменные углеродсодержащие группы заместителей
Формула скелета для общего кетона, где R и R 'обозначают переменные углеродсодержащие группы заместителей - кинетика
- Подполе химия, специализирующаяся на скорости реакции.
- кинетическая энергия
- энергия объекта, обусловленная его движением.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
L
- lability
- лантаноиды
- периодические серии металлических элементов с атомными номерами от 57 до 71, из решетка от лантана до лютеция.
-
- Уникальное расположение атомов или молекул в кристаллической жидкости или твердом теле.
- энергия решетки
- закон сохранения энергии
- закон сохранения массы
- закон кратных пропорций
- законы термодинамики
- эффект выравнивания
- Влияние растворителя на химические свойства кислот или оснований, растворенных в растворителе. Сила сильной кислоты ограничивается или «выравнивается» основностью растворителя, и аналогично сила сильного основания ограничивается кислотностью растворителя, так что эффективное pH раствора выше или ниже, чем можно предположить с помощью константы диссоциации кислоты или основания.
- кислота Льюиса
- основание Льюиса
- структура Льюиса
- лиганд
- ион ион, функциональная группа или другая молекула, которая связывается с центральным атомом металла с образованием координационного комплекса. Такое связывание может варьироваться от ковалентного до ионного, но обычно включает формальное пожертвование одной или нескольких электронных пар лиганда металлу.
- свет
- Часть электромагнитного спектра, видимая невооруженным глазом.
- разжижение
- жидкость
- Одно из четырех основных состояний вещества, характеризуемых почти несжимаемыми частицами жидкости, которые сохраняют определенный объем, но не имеют фиксированной формы.
- locant
- Лондонские дисперсионные силы
- Тип слабой межмолекулярной силы.
Содержание:
- Top
- 0 –9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
M
- магнитное квантовое число
- пластичность
- См. пластичность.
- манометр
- Прибор, используемый для измерения давления изобретен Евангелистой Торричелли в 1643 году.
- масса
- A свойство физического материи, которое является мерой его сопротивления ускорению когда применяется чистая сила d. СИ базовой единицей массы является килограмм (кг).
- массовая концентрация
- массовая доля
- массовое число (A)
- общее количество протонов и нейтронов (вместе известных как нуклонов) в ядре атома атома. Он определяет атомную массу атома. Массовое число варьируется между разными изотопами одного и того же химического элемента и часто включается либо после названия элемента (как в углерод-12 ), либо в виде надстрочного индекса слева от элемента символ (как в C ) для идентификации конкретного изотопа.
- масс-спектрометрия (MS)
- Аналитический метод, который измеряет отношение массы к заряду ионов в химическом образце путем бомбардировки образца электронами до точки ионизации с последующим разделением заряженных фрагментов путем воздействия на них электрического или магнитного поля, обычно для определения элементарные или изотопные сигнатуры неизвестного вещества, массы составляющих его частиц и / или идентичности или структуры молекул внутри него. Результаты представлены в виде масс-спектра, графика интенсивности ионных сигналов как функции отношения массы к заряду.
- материя
- Любое вещество с массой и занимает место, имея объем.
- металл
- Любой химический элемент, который является хорошим проводником как электричества, так и тепла и который легко образует катионы и ионные связи с неметаллами.
- плавление
- фазовый переход вещества из твердое в жидкое.
- точка плавления
- Температура, при которой вещество меняет состояние с твердого на жидкость. Оно зависит от давления и обычно указывается для данного вещества в стандартных условиях. Температура плавления вещества идентична его точке замерзания.
- металлоиду
- Химический элемент или вещество, обладающее свойствами как металлов, так и неметаллов.
- метиленового синего.
- A гетероциклическое ароматическоесоединение с молекулярной формулой C16H18N3S Cl.
- микроцентрифужная пробирка
- Небольшой пластиковый герметичный контейнер, который используется для хранения небольших объемов жидкость, обычно менее 2 миллилитров.
 1,7-миллилитровая микроцентрифужная пробирка или пробирка Эппендорфа, содержащая кумасси синего раствор
1,7-миллилитровая микроцентрифужная пробирка или пробирка Эппендорфа, содержащая кумасси синего раствор - минерал
- смешиваемость
- смесь
- Материал, состоящий из двух или более различных веществ, которые физически смешаны, но не соединены химически (т.е. не произошла химическая реакция, которая превратила молекулы веществ в новые вещества).
- фрагмент
- Любая названная характеристическая группа, ветвь или другая часть большой молекулы, которая может быть идентифицирована в других типах m молекулы. Функциональные группы обычно меньше и более общие, чем фрагменты, тогда как заместители и боковые цепи часто можно классифицировать как фрагменты и наоборот.
- моляльность
- Мера концентрации растворенного вещества в растворе в единицах количества растворенного вещества на единицу массы из растворителя. Моляльность обычно выражается в единицах моль на килограмм (моль / кг); раствор с концентрацией ровно 1 моль / кг иногда называют 1 моль. Контраст молярность.
- молярный коэффициент ослабления
- молярная концентрация
- мера концентрации химического вещества, особенно растворенного вещества в растворе в единицах количества компонентов на единицу объема раствора. Молярность обычно выражается в единицах моль на литр (моль / л); раствор с концентрацией ровно 1 моль / л обычно считается 1 молярным, что обозначается как 1 М. Контраст молярность.
- молярная доля
- молярная масса
- моль (моль)
- Единица (обозначение: моль), которая измеряет количество вещества с точки зрения абсолютного количества частиц или объектов, составляющих вещество. Один моль содержит приблизительно 6,022 × 10 частиц или объектов.
- молекулярная формула
- молекулярная орбиталь (МО)
- Любая область, в которой один или несколько электронов можно найти в молекуле (в отличие от отдельного атома).
- молекулярной орбитальной диаграммы
- молекулы
- Ряд атомов, которые химически связаны вместе и в совокупности электрически нейтральны.
- одноатомный
- Имеет только один атом, в отличие от молекулы, состоящей более чем из одного. все элементы одноатомны в фазе газа при достаточно высоких температурах. Контраст двухатомный и многоатомный.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
N
- естественное содержание
- чистый
- Условия с жидким реагентом или газом, выполненные без добавления растворителя или сорастворителя.
- нейтрон
- Тип субатомная частица, которая электрически нейтральна, хавин g без чистого заряда.
- азот
- нуклон
- Либо протон, либо нейтрон, рассматриваемый в качестве компонента атомного ядра.
- нуклеофил
- Любой атом или молекула, которые могут передавать электронную пару другому атому или молекуле. Все молекулы или ионы со свободной парой электронов или, по меньшей мере, с одной пи-связью могут действовать как нуклеофилы, благодаря чему они притягиваются к электронно-дефицитным областям других видов; химическая реакция, в которой нуклеофил отдает электронную пару электрофилу, может быть названа нуклеофильной атакой. Поскольку они отдают электроны, нуклеофилы по определению являются основаниями Льюиса.
- ядром
- Центром атома, состоящего из нейтронов и протоны и обладающие чистым положительным электрическим зарядом.
- благородный газ
- Любой из шести неметаллических элементов из группы 18 периодической таблицы : гелий (He), неон (Ne), аргон (Ar), криптон (Kr), ксенон (Xe) и радон (Rn). Все благородные газы имеют внешние электронные оболочки, которые полностью заполнены в своем естественном состоянии, что придает им очень низкую химическую активность.
- неметалл
- Любой химический элемент, не являющийся металл.
- нормальность
- ядерное
- Относится к атомному ядру или относится к нему.
- ядерная химия
- Раздел химии, изучающий различные процессы и свойства, относящиеся к атомным ядрам, включая радиоактивность.
- спектроскопия ядерного магнитного резонанса
- Метод, который использует магнитные свойства определенных ядер, полезный для идентификации неизвестных соединений. Ядерный магнитный резонанс часто сокращенно обозначается как ЯМР.
- ядерная трансмутация
- нуклид
- Вид атома, характеризующийся его массовым числом, атомным номером и состояние ядерной энергии при условии, что средняя продолжительность жизни в этом состоянии достаточно велика, чтобы ее можно было наблюдать.
- числовая плотность
- Мера концентрации счетных объектов (атомов, молекул и т. д.) в пространстве, выраженное числом на единицу том.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. также
- Ссылки
- Внешние ссылки
O
- правило октетов
- Классическое правило описания электронной конфигурации атомов в определенных молекулах: максимальное количество электронных пар, которые могут быть размещены в валентной оболочке элемента в первой строке периодической таблицы равно четырем (или восьми электронам). Для элементов во второй и последующих строках есть много исключений из этого правила.
- олефин
- Тривиальное (не IUPAC) название для любого алкена.
- оптической активности
- орбиталь
- Любая область атома или молекулы, в которой можно найти один или несколько электронов. Термин может относиться к атомной орбитали или молекулярной орбитали.
- орбитальной гибридизации
- порядок реакции
- органическая кислота
- Любое органическое соединение с кислотными свойствами. Контраст органическое основание.
- органическое основание
- Любое органическое соединение с основными свойствами. Контрастная органическая кислота.
- органическое соединение
- Любое химическое соединение, которое содержит один или несколько атомов углерода. Контраст неорганическое соединение.
- органическая химия
- Раздел химии, изучающий химические свойства и реакции органических соединений. Контраст неорганическая химия.
- органическая окислительно-восстановительная реакция
- осмотическое давление
- другой металл
- Любой из металлических элементов в p-блоке, которые являются характеризуется сочетанием относительно низких точек плавления (все менее 950 K) и относительно высоких значений электроотрицательности (все более 1,6, пересмотренный Pauling).
- окисление
- степень окисления
- 1. Степень окисления отдельного атома в химическом соединении, измеряемая как уменьшение количества электронов по сравнению с естественным элементным состоянием атома.
- 2. Гипотетический электрический заряд (положительный, отрицательный или нулевой), который был бы у атома, если бы все связи с атомами различных элементов были 100% ионными, без ковалентными компонент.
- окислитель
- оксокислота
- 1. Любая кислота, имеющая кислород в кислотной группе.
- 2. Любое соединение, которое содержит кислород, по меньшей мере один другой элемент и по меньшей мере один атом водорода, связанный с кислородом, и которое дает сопряженное основание за счет потери положительных ионов водорода..
- кислород
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
P
- p-блок
- парафин
- 1. Тривиальное (не IUPAC) имя для любого алкана.
- 2. Другое название керосина.
- парциальное давление
- паскаль (Па)
- пассивация
- pH
- Логарифмическая шкала, используемая для указания кислотности или основности водного раствора. Шкала pH приблизительно соответствует отрицательному значению логарифма по основанию 10 молярной концентрации ионов водорода в растворе. При комнатной температуре чистая вода нейтральна (pH = 7); растворы с pH менее 7 являются кислыми, а растворы с pH более 7 - основными.
- фаза
- Область пространства, в которой все физические свойства вещества практически однородны, или область материала, которая является химически однородный, физически различный и часто механически разделяемый. Термин «фаза» может иметь несколько различных применений в химическом контексте; в просторечии он часто используется как синоним состояния вещества, но в одном состоянии вещества может существовать множество различных фаз.
- фазовый переход
- 1. Преобразование химического вещества между твердым, жидким и газообразным состояниями вещества и, в редких случаях, случаи, плазма.
- 2. Измеряемые значения внешних условий, при которых происходит такое превращение.
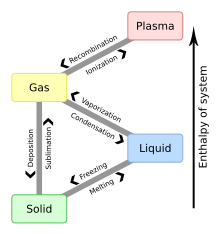 На этой диаграмме показана номенклатура, обычно используемая для каждого из различных фазовых переходов
На этой диаграмме показана номенклатура, обычно используемая для каждого из различных фазовых переходов - фи-связь
- физическая химия
- химия, изучающая химические системы с точки зрения принципов, методов и концепций физики, таких как движение, энергия, сила, время, термодинамика, химическое равновесие, статистическая механика и др. В отличие от химической физики, физическая химия - это преимущественно (хотя и не полностью) макроскопическая наука, изучающая физические и химические взаимодействия объемных количеств вещества.
- пи-связь
- пипетка
- A лабораторный инструмент, обычно используемый в химии, биологии и медицине для переноса и распределения точно измеренного объема жидкости.
- плазма
- Одно из четырех основных состояний вещества, в котором очень высокая энергия частицы частично или полностью ионизированы до такой степени, что они проявляют уникальные свойства и поведение в отличие от других трех состояний. Плазма не существует свободно на поверхности Земли в естественных условиях.
- период
- Горизонтальный ряд периодической таблицы элементов и элементов, которые разделяют ее. Контраст группа.
- периодическая таблица элементов
- Табличное расположение химических элементов, организованных по их атомному номеру, электронной конфигурации, и другие химические свойства, принятая структура которых показывает периодические тенденции и используется химиками для получения взаимосвязей между различными элементами, а также для прогнозирования свойств и поведения неоткрытых или вновь синтезированных элементов. Первая периодическая таблица элементов была опубликована русским химиком Дмитрием Менделеевым в 1869 году.
 Современная Периодическая таблица элементов. Горизонтальные строки называются периодами, а вертикальные столбцы называются группами или семействами.
Современная Периодическая таблица элементов. Горизонтальные строки называются периодами, а вертикальные столбцы называются группами или семействами. - полярность
- потенциальная энергия
- Накопленная энергия в теле или в системе из-за его положения в силовом поле или из-за его конфигурации.
- осадок
- Образование твердого вещества в растворе или внутри другого твердого вещества во время химической реакции или путем диффузии в твердом теле.
- точность
- Насколько близки друг к другу результаты нескольких экспериментальных испытаний или наблюдений. Сравните точность.
- давление
- Сила , приложенная перпендикулярно к поверхности объекта на единицу площади. Единица измерения давления СИ - это паскаль (Па), хотя многие другие единицы давления также широко используются в химии.
- фотон
- Носитель электромагнитное излучение всех длин волн (например, гамма-лучи и радиоволны ).
- многоатомные
- Состоит из двух или более атомов, одинаковых или разных элементов. Контраст одноатомный и двухатомный.
- многоатомный ион
- A молекула, состоящая из двух или более ковалентно связанных атомов, которые вместе несут общую электрическую заряжать и, следовательно, действовать как ион.
- защитная группа
- протон
- A субатомная частица с положительным электрическим зарядом, который находится в ядре атом. Часто обозначается символом H.
- протонирование
- Присоединение протона (H) к атому, молекуле или иону.
- чистое вещество
- См. химическое вещество.
- пиролиз
- термическое разложение материалов при e повышенные температуры в инертной атмосфере, такой как вакуумный газ.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. также
- Ссылки
- Внешние ссылки
Q
- квантовая механика
- изучение того, как атомы, молекулы, субатомные частицы и т. д. ведут себя и структурированы.
- кварк
- Элементарная частица и фундаментальный компонент материи.
- квант
Содержание:
- Наверх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
R
- рацемат
- Эквимолярная смесь пары энантиомеров который не проявляет оптической активности. Химическое название или формула рацемата отличается от энантиомеров префиксом (±) или символами RS и SR.
- излучение
- Энергия, выделяемая в форме волн или субатомных частиц при переходе от высокоэнергетического состояния к низкоэнергетическому.
- радикал
- Любой атом, молекула или ион, имеющий хотя бы один неспаренныйвалентный электрон. За некоторыми исключениями, такие неспаренные электроны делают радикалы очень химически реактивными, и поэтому органические радикалы обычно недолговечны.
- радиоактивный распад
- Процесс потери энергии нестабильным атомным ядром из-за испускания излучения.
- Закон Рауля
- Закон термодинамики, который гласит, что парциальное давление каждого газообразного компонента идеальной смеси из жидкостей равно давление пара чистого компонента, умноженное на его молярную долю в смеси.
- редкоземельный металл
- уравнение скорости
- реагент
- Любое вещество, которое потребляется в ходе химической реакции.
- механизм реакции
- Пошаговая последовательность элементарных реакций, в результате которых происходит большая химическая реакция или общее изменение имеет место. Полный механизм должен описывать и объяснять, какие связи разорваны и какие образуются (и в каком порядке), а также все реагенты, продукты и задействованы катализаторы ; суммы каждого; все промежуточные соединения, активированные комплексы и переходные состояния ; и стереохимия каждого химического вещества. Поскольку детальные процессы сложной реакции в большинстве случаев не наблюдаются, механизм реакции часто является теоретическим предположением, основанным на термодинамической осуществимости и той небольшой поддержке, которую можно получить из эксперимента.
- скорость реакции
- Скорость, с которой реагенты превращаются в продукты в химической реакции.
- константа скорости реакции
- реактивный промежуточный продукт
- реакционная способность
- ряд реактивности
- эмпирический расчет, и структурно-аналитическая последовательность ряда металлов, упорядоченная по их общей реакционной способности от наивысшей к самой низкой и используемая для обобщения информации об их реакциях с кислотами и водой. и методы, используемые для их извлечения из руд.
- реагент
- Тестируемое вещество, которое добавляется в систему, чтобы вызвать химическую реакцию или посмотреть, происходит ли реакция.
- редокс
- восстановитель
- восстановительный потенциал
- резонанс
- реторта
- Лабораторное устройство, используемое для дистилляции или сухой дистилляции химических веществ, традиционно состоящее из сферического сосуда с длинной направленной вниз горловиной, через которую проходят конденсированные пары, образующиеся при дистилляции. в отдельную емкость для сбора.
- колба с круглым дном
- ржавчина
Содержимое:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. также
- Ссылки
- Внешние ссылки
S
- s -block
- Общее название элементов 1 и 2 групп таблицы Менделеева (щелочные и щелочные металлы), а также водород и гелиевая.
- соль
- Любое ионное соединение, состоящее из одного или нескольких анионов и одного или нескольких катионов.
- солевой мостик
- Устройство, используемое для соединения восстановления с полуячейками окисления в электрохимической ячейке.
- солевой раствор
- Общий термин для раствора хлорида натрия (NaCl), растворенный в воде (H2O).
- Schrödinger equat ion
- Уравнение квантового состояния, которое представляет поведение электрона вокруг атома.
- реакция второго порядка
- полупроводник
- Электропроводящее твердое тело, степень проводимости находится где-то между проводник и проводник.
- последовательное разбавление
- боковая цепь
- Химическая группа заместителя, которая присоединена к основной части или " основная цепь "более крупной молекулы, особенно олигомерной или полимерной углеводородной цепи, которая ответвляется от более длинной первичная цепь макромолекулы , используемая в биохимии и органической химии.
- одинарная связь
- A связь, которая включает разделение одной пары электронов.
- скелетная формула
- золь
- A суспензия твердых частиц в жидкости. Искусственные примеры включают золь-гели.
- твердое тело
- Одно из четырех основных состояний вещества, характеризующееся относительно низкоэнергетическими частицами, плотно упакованными вместе в жесткие структуры сформа форма и объем. См. Модуль Юнга.
- растворимость
- Свойство твердого, жидкого или газообразногорастворенного вещества до растворить в твердом, жидком или газообразном растворителе. Обычно он выражается как доля растворенного вещества, растворенного в растворителе в насыщенном растворе.
- растворенное вещество
- Часть раствора, которая растворяется в растворителе. Например, хлорид натрия (NaCl) - это растворенное вещество в растворе солевой воды.
- раствор
- Гомогенная смесь, состоящая из нескольких веществ, обычно называемых растворенные вещества и растворители.
- сольватированный электрон
- сольватация
- См. растворение.
- сольватационная оболочка
- растворитель
- Часть раствора, который растворяет растворенное вещество. Например, вода (H 2 O) является растворителем в растворе солевой воды.
- спектрохимия
- спектрометрия
- См. масс-спектрометрия.
- спектроскопия
- исследование излучения и вещества, например, рентгеновской абсорбционной и эмиссионной спектроскопии.
- стандартный раствор
- стандартные условия температуры и давления (STP)
- Стандартизация окружающей температуры и давления, используемая для упрощения сравнения экспериментальных результатов. Стандартная температура составляет 25 градусов Цельсия (° C), а стандартное давление - 100 000 килопаскалей (кПа). Стандартные условия часто обозначаются аббревиатурой STP или SATP.
- состояние материи
- Состояние материи, существующей в отдельной, однородной, макроскопической форме. Твердое, жидкое, газ и плазма - четыре традиционных состояния вещества и наиболее известные. См. Также фаза.
- ступенчатая реакция
- стереохимия
- стереоизомер
- изомер, который имеет идентичный химический состав, но отличается пространственным расположением его атомы.
- стехиометрия
- Расчет количества реагентов и продуктов в химических реакциях. Стехиометрия основана на законе сохранения массы и наблюдении, что количества реагентов и продуктов обычно существуют в соотношении положительных целых чисел, подразумевая, что если количества отдельных реагентов известны, то количества реагентов продукты могут быть вычислены.
- сильная кислота
- сильное основание
- структурная формула
- структурный изомер
- субатомная частица
- Любая частица, которая меньше, чем атом. Примеры включают протоны, нейтроны и электроны.
- сублимацию
- фазовый переход вещества из твердого тела на известковую воду топливо или газ без очевидного промежуточного перехода в жидкость в процессе.
- вещество
- См. химическое вещество.
- заместитель
- суспензия
- Гетерогенная смесь, содержащая твердые частицы, достаточно большие для седиментации, посредством которой такие частицы разделяются из жидкости и оседать со временем, если ее не беспокоить. В суспензии растворенное вещество не растворяется, но остается диспергированным или взвешенным в текучем растворителе только временно и при механическом перемешивании. Контраст коллоид и раствор.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
T
- потускнение
- температура
- Пропорциональная мера средней кинетической энергии случайных движений составляющих микроскопических частиц системы. СИ базовой единицей температуры является кельвин.
- теоретический выход
- См. выход.
- теплопроводность
- Свойство материала, которое позволяет ему проводить термическую энергия или тепло (величина, часто обозначаемая
 ).
). - термохимия
- Изучение поглощения или выделения тепла в течение химическая реакция.
- термодинамика
- Изучение эффектов изменения температуры, объема или давления (или работы, тепла и энергии) в макроскопическом масштабе.
- термодинамическая стабильность
- Состояние системы, находящейся в наиболее
- термометр
- Прибор, используемый для измерения температуры.
- титрование
- лабораторный метод используется количественного химический анализ, используемый для определения концентрации идентифицированного аналита. Процедура включает приготовление конкретного реагента в виде стандартного раствора стандартным объемом (называемым титрантом или титратором) и предоставлением ему возможностей реагировать с помощью аналит (называемый титраном) для определения последнего.
- торр
- Единица измерения давления, эквивалентная 133,322 Па или 1,3158 × 10 атм..
- переходный металл
- Элемент, атомы которого естественным образом встречаются с не полностью заполненными суб-оболочками "d". Эти элементы сгруппированы как так называемые элементы d-блока в периодической таблицы.
- трансурановый элемент
- Любой элемент с атомным номером больше 92 (т.е. происходит после урана в периодической таблицы). Ни один из трансурановых элементов не является стабильным в естественных условиях.
- тройная связь
- A связь, которая включает ковалентное разделение трех пар электронов (например, молекула двухатомного азота N 2 состоит из двух атомов азота, связанной тройной связью).
- тройная точка
- Место, где температура и давление из трех фаз одинаковы. Вода имеет особую фазовую диаграмму.
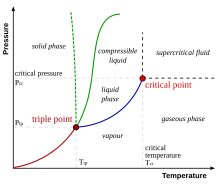 Фазовая диаграмма, показывающая тройную точку и критическую точку вещества
Фазовая диаграмма, показывающая тройную точку и критическую точку вещества - эффект Тиндаля
- эффект рассеяния света коллоидными или взвешенными частицами.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
U
- Номер ООН
- Четырехзначный код, используемый для обозначения опасных и легковоспламеняющихся веществ.
- неопределенность
- Представление о том, что любое измерение, включающее любое количество, не может быть точно воспроизводимым.
- принцип неопределенности
- Знание местоположения частиц делает ее импульс неопределенным, тогда как знание моментов делает ее местоположение неопределенным.
- единица атомной единица массы (u)
- Единица массы приблизительно равна массе одного протона или нейтрона. Иногда его приравнивают к технически отличной и устаревшей атомной единице массы и сокращенно а.е.м.
- элементарная ячейка
- Наименьшая повторяющаяся единица кристаллической решетки.
- коэффициент единицы
- Утверждения, используемые для преобразования единиц.
- неспаренный электрон
Содержание:
- Наверх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
V
- термос
- Сосуд для хранения, состоящий из двух колбы или другие емкости, помещенные одна в другую и соединенные горлышком, и пространство между ними, в котором частично откачивается воздух, создавая почти вакуум, который снижает тепло между внутренней частью судна и окружающей средой. Вакуумные колбы могут значительно увеличить время, в течение которого их содержимое остается или холоднее, чем окружающая среда.
- валентный электрон
- Любой из внешних электронов атома, находящегося в электронной оболочке.
- теория валентных связей
- теория, объясняющая химические связи внутри молекул путем обсуждения валентностей, числа химических связей, образованных атомом.
- валентность
- объединяющая способность элемент.
- сила Ван-дер-Ваальса
- Одна из сил (притяжение / отталкивание) между молекулами.
- фактор Ван 'т Гоффа
- Отношение моль частиценного в раствор к молям раствор вещества раствор.
- пар
- Когда температура вещества ниже критической, в то время как газ фаза.
- давление пара
- Давление, оказываемое паром, которое находится в термодинамическом равновесии с его конденсированными фазами (твердым или жидким) при заданной температуре в закрытая система. Это обычно описывается как показатель скорости испарения жидкости.
- испарение
- фазовый переход вещество из жидкости в газ.
- вязкость
- Мера сопротивление жидкости течению.
- летучесть
- Качество материала, этим, насколько легко вещество испаряется. При данном давлении и давлении материала с высокой вероятностью будет существовать в виде газа, в то время как вещество с низкой летучестью с большей вероятностью будет существовать в виде жидкости или сплошной ; эквивалентно, менее летучие вещества будут легче конденсироваться из газообразного состояния, чем высоколетучие.
- вольт (В)
- Производная единица электрического потенциала, разность электрических потенциалов и электродвижущая сила, определяемая как один джоуль из работы на кулон.
- вольтметр
- Прибор, измеряющий электрический потенциал ячейки.
- объем
- Количество трехмерного пространства, окруженного замкнутой поверхностью, или пространство, в котором вещество (твердое тело, жидкость, газ или плазма) или форма занимает или содержит. СИ единица куба измерения - счётчик (м).
- объемный анализ
- См. титрование.
- мерная колба
Содержимое:
- Наверх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
W
- стекло для часов
- Круглый вогнутый кусок стекла, обычно используется в химических лабораториях в качестве рабочей поверхности для целей. например, испарение жидкостей, удерживание твердых веществ при их взвешивании, нагревание количества веществ или в качестве покрытия стакана.
- воды
- A полярноенеорганическое соединение с химической формула H 2 O, которая представляет собой жидкость без вкуса, запаха и обычно бесцветную при стандартной температуре и давлении, хотя она также встречается в природе как твердое тело и газ на поверхности Земли. Это самое распространенное вещество на Земле, и поэтому он является неотъемлемым компонентом биологических химических и химических систем. Воду часто «универсальным растворителем » из-за присущей ей способности растворять многие вещества.
- волновая функция
- Математическая функция, описывающее положение электрон в трехмерном пространстве.
- слабая кислота
- слабое основание
- влажная химия
- Форма аналитической химии, в которой используются классические лабораторные методы, такие как простое наблюдение и элементарные химические тесты для изучения химических веществ и химических тестов, то есть без использования сложных инструментов или автоматизированного или компьютерного анализа. Его часто используют в школах для обучения студентов принципам химии.
- работа
- работа
- Серия манипуляций, необходимых для выделения и очистки желаемого продукта или продуктов химическая реакция.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См.
- Ссылки
- Внешние ссылки
X
- Рентгеновское Также излучение
- Форма ионизирующего излучения между гамма и УФ лучами в электромагнитном спектре.
- Дифракция рентгеновских лучей
- метод классических структур твердых тел с использованием рентгеновских лучей с одной длиной волны и наблюдения на дифрактограмме.
- Рентгеновская фотоэлектронная спектроскопия
- A спектроскопия метод, использование для измерения материала.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
Y
- yield
- Поддающееся количественной оценке количества продукта, полученного в ходе реакции.
Z
- зонной плавки
- Способ удаления примесей из элемента расплавив я t и медленно движется вниз по слитку (литью).
- цвиттерион
- Химическое соединение, чистый заряд которого равен нулю и, следовательно, электрически нейтрален. Но в нем есть положительные и отрицательные заряды из-за формального заряда из-за частичных зарядов составляющих его элементы.
- цинк
- Металлический химический элемент с атомным номером 30 и символ Zn.
Содержание:
- Верх
- 0–9
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- См. Также
- Ссылки
- Внешние ссылки
См. Также
Внешние ссылки
 | В Викиучебниках есть книга по теме: Химия |
 атом с протонами, нейтронами и электронами помечено
атом с протонами, нейтронами и электронами помечено  Пример горение
Пример горение  Двухатомная молекула водорода, H 2 (справа), образована ковалентной связь, когда два одиночных атома водорода разделяют два электрона
Двухатомная молекула водорода, H 2 (справа), образована ковалентной связь, когда два одиночных атома водорода разделяют два электрона  Ион натрия ( Na) образует сольватационный комплекс с молекулами воды при растворении в водном растворе
Ион натрия ( Na) образует сольватационный комплекс с молекулами воды при растворении в водном растворе  500-миллилитровая колба Эрленмейера
500-миллилитровая колба Эрленмейера  , где
, где  - количество валентных электронов нейтрального атома в его основном состоянии;
- количество валентных электронов нейтрального атома в его основном состоянии;  - количество валентных электронов атома, не участвующих в связях в молекуле; и
- количество валентных электронов атома, не участвующих в связях в молекуле; и  - количество электронов, связанных с другими атомами в молекуле.
- количество электронов, связанных с другими атомами в молекуле. An ионная связь между атомом натрия (Na) и атомом фтора (F). Атом натрия теряет свой единственный валентный электрон (оставляя атом с положительным электрическим зарядом ), а атом фтора приобретает этот же электрон в результате экзотермического процесса ( придавая атому отрицательный электрический заряд). Противоположно заряженные ионы затем притягиваются друг к другу с образованием нового соединения, называемого фторидом натрия.
An ионная связь между атомом натрия (Na) и атомом фтора (F). Атом натрия теряет свой единственный валентный электрон (оставляя атом с положительным электрическим зарядом ), а атом фтора приобретает этот же электрон в результате экзотермического процесса ( придавая атому отрицательный электрический заряд). Противоположно заряженные ионы затем притягиваются друг к другу с образованием нового соединения, называемого фторидом натрия. Формула скелета для общего кетона, где R и R 'обозначают переменные углеродсодержащие группы заместителей
Формула скелета для общего кетона, где R и R 'обозначают переменные углеродсодержащие группы заместителей  1,7-миллилитровая микроцентрифужная пробирка или пробирка Эппендорфа, содержащая кумасси синего раствор
1,7-миллилитровая микроцентрифужная пробирка или пробирка Эппендорфа, содержащая кумасси синего раствор  На этой диаграмме показана номенклатура, обычно используемая для каждого из различных фазовых переходов
На этой диаграмме показана номенклатура, обычно используемая для каждого из различных фазовых переходов  Современная Периодическая таблица элементов. Горизонтальные строки называются периодами, а вертикальные столбцы называются группами или семействами.
Современная Периодическая таблица элементов. Горизонтальные строки называются периодами, а вертикальные столбцы называются группами или семействами.  ).
). Фазовая диаграмма, показывающая тройную точку и критическую точку вещества
Фазовая диаграмма, показывающая тройную точку и критическую точку вещества