 Различные типы мутации indel. Панель C - это просто делеция, а не мутация со сдвигом рамки.
Различные типы мутации indel. Панель C - это просто делеция, а не мутация со сдвигом рамки. A Носится с Днепром RNA (также называемая ошибкой кадрирования или сдвигом рамки считывания ) - это генетическая мутация, вызванная инсерциями (вставками или делециями ) ряда нуклеотидов в последовательности ДНК, которая не делится на три. Из-за триплетной природы экспрессии гена с помощью кодонов вставка или удаление может изменить рамку считывания (группировку кодонов), что приведет к полностью отличается перевод от оригинала. Чем раньше в последовательности происходит делеция или вставка, тем больше изменяется белок. Мутация сдвига рамки считывания - это не то же самое, что однонуклеотидный полиморфизм, в котором нуклеотид заменен, а не вставлен или удален. Мутация сдвига рамки считывания обычно вызывает считывание кодонов после мутации для кодирования различных аминокислот. Мутация сдвига рамки также изменит первый стоп-кодон («UAA», «UGA» или «UAG»), встречающийся в последовательности. Создаваемый полипептид может быть ненормально коротким или ненормально длинным и, скорее всего, не будет функциональным.
Мутации сдвига рамки видны при тяжелых генетических заболеваниях, таких как болезнь Тея – Сакса ; они повышают восприимчивость к определенным видам рака и классам семейной гиперхолестеринемии ; в 1997 году мутация сдвига рамки считывания была связана с устойчивостью к инфекции ретровирусом ВИЧ. Мутации сдвиг рамки были предложены в качестве источника биологической новизны, так как с предполагаемым созданием nylonase, однако, эта интерпретация является спорной. Исследование, проведенное Негоро и др. (2006), показало, что мутация сдвига рамки считывания вряд ли была причиной, и что, скорее, в результате произошла замена двух аминокислот в активном сайте наследственной эстеразы. в нейлоназе.
Информация, содержащаяся в ДНК, определяет функцию белков в клетках всех организмов. Транскрипция и трансляция позволяют передавать эту информацию для создания белков. Однако ошибка при чтении этого сообщения может привести к неправильной функции белка и в конечном итоге вызвать заболевание, даже если клетка включает в себя различные корректирующие меры.
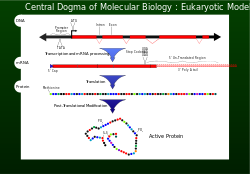 центральная догма модель
центральная догма модель В 1956 году Фрэнсис Крик описал поток генетической информации от ДНК к особое расположение аминокислот для создания белка в качестве центральной догмы. Для правильного функционирования клетки белки должны продуцироваться точно для структурной и каталитической активности. Неправильно полученный белок может оказывать пагубное воздействие на жизнеспособность клетки и в большинстве случаев вызывать нездоровье высшего организма из-за аномальных клеточных функций. Чтобы гарантировать, что геном успешно передает информацию, механизмы проверки, такие как экзонуклеазы и системы исправления несоответствий, включены в Репликация ДНК.
 Процесс трансляции
Процесс трансляции После репликации ДНК считывание выбранного участка генетической информации осуществляется с помощью транскрипции. Нуклеотиды, содержащие генетическую информацию, теперь находятся на одноцепочечной матрице мессенджера, называемой мРНК. МРНК встроена в субъединицу рибосомы и взаимодействует с рРНК. Генетическая информация, содержащаяся в кодонах мРНК, теперь считывается (декодируется) антикодонами тРНК. По мере считывания каждого кодона (триплета) аминокислоты соединяются вместе до тех пор, пока не будет достигнут стоп-кодон (UAG, UGA или UAA). На данный момент полипептид (белок) был синтезирован и высвобожден. На каждые 1000 аминокислот, включенных в белок, неверно не более одной. Эта точность распознавания кодонов, сохраняющая важность правильной рамки считывания, достигается за счет правильного спаривания оснований в сайте рибосомы A, GTP гидролизной активности EF-Tu формы кинетической стабильность и механизм корректуры при высвобождении EF-Tu.
Сдвиг рамки может также происходить во время трансляции профазы, продуцируя различные белки из перекрывающихся открытых рамок считывания, такие как gag-pol-env ретровирусные белки. Это довольно часто встречается у вирусов, а также у бактерий и дрожжей (Farabaugh, 1996). Обратная транскриптаза, в отличие от РНК-полимеразы II, считается более сильной причиной возникновения мутаций сдвига рамки считывания. В экспериментах только 3–13% всех мутаций сдвига рамки считывания происходили из-за РНК-полимеразы II. У прокариот частота ошибок, вызывающих мутации со сдвигом рамки считывания, находится где-то в диапазоне от 0,0001 до 0,00001.
Существует несколько биологических процессов, которые помогают предотвратить мутации со сдвигом рамки считывания. Происходят обратные мутации, которые изменяют мутированную последовательность обратно на исходную последовательность дикого типа. Другой возможностью коррекции мутации является использование мутации-супрессора . Это компенсирует эффект исходной мутации, создавая вторичную мутацию, сдвигая последовательность, чтобы можно было прочитать правильные аминокислоты. Направляющая РНК может также использоваться для вставки или удаления уридина в мРНК после транскрипции, это позволяет получить правильную рамку считывания.
 Трехбуквенный код, кодон
Трехбуквенный код, кодон A кодон представляет собой набор из трех нуклеотидов, триплет, который кодирует определенную аминокислоту. Первый кодон устанавливает рамку считывания, посредством чего начинается новый кодон. Аминокислотный скелет последовательность белка определяется смежными триплетами. Кодоны являются ключом к трансляции генетической информации для синтеза белков. Рамка считывания устанавливается, когда начинается трансляция мРНК, и сохраняется, когда она считывает один триплет за другим. Считывание генетического кода подчиняется трем правилам: отслеживание кодонов в мРНК. Сначала кодоны считываются в направлении от 5 'до 3'. Во-вторых, кодоны не перекрываются, и сообщение не имеет пробелов. Последнее правило, как указано выше, заключается в том, что сообщение транслируется в фиксированной рамке считывания.
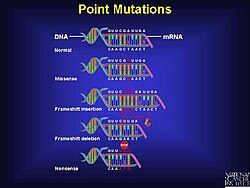 Пример различных типов точечных мутаций
Пример различных типов точечных мутаций Мутации со сдвигом рамки могут возникать случайным образом или быть вызваны внешним стимул. Обнаружение мутаций сдвига рамки считывания может происходить несколькими различными методами. Сдвиг рамки - это всего лишь один из типов мутаций, которые могут привести к неполным или неправильным белкам, но они составляют значительный процент ошибок в ДНК.
Это генетическая мутация на уровне нуклеотидных оснований. Почему и как происходят мутации со сдвигом рамки считывания, постоянно выясняется. Было проведено экологическое исследование, в частности продуцирование индуцированных УФ мутаций сдвига рамки считывания ДНК-полимеразами, дефицитными по 3 '→ 5' экзонуклеазной активности. Нормальная последовательность 5 'GTC GTT TTA CAA 3' была изменена на GTC GTT T TTA CAA (MIDT) из GTC GTT C TTA CAA (MIDC) для изучения сдвигов кадров. Э. coli pol I Kf и мутантная ДНК-полимераза T7 ферменты, лишенные 3 '→ 5' экзонуклеазной активности, продуцируют УФ-индуцированные ревертанты с большей частотой, чем их эффективные аналоги экзонуклеазы. Данные показывают, что потеря корректирующей активности увеличивает частоту сдвига рамки, вызванного УФ-излучением.
Влияние соседних оснований и вторичной структуры для обнаружения частоты Мутации сдвига рамки считывания были подробно изучены с использованием флуоресценции. Флуоресцентно меченая ДНК с помощью аналогов основания позволяет изучать локальные изменения последовательности ДНК. Исследования влияния длины праймерной цепи показывают, что равновесная смесь четырех конформаций гибридизации наблюдалась, когда основания матрицы выходили петлей в виде выпуклости, то есть структуры, фланкированной с обеих сторон дуплексной ДНК. Напротив, двойная петлевая структура с необычной конформацией разнесенной ДНК на ее нижнем крае наблюдалась, когда экструдированные основания располагались на стыке праймер-матрица, показывая, что смещения могут быть изменены соседней вторичной структурой ДНК.
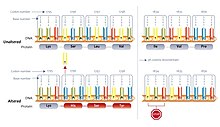 Делеционная мутация изменяет каждый следующий за ней кодон и может преждевременно остановить синтез белка за счет образования стоп-кодона.
Делеционная мутация изменяет каждый следующий за ней кодон и может преждевременно остановить синтез белка за счет образования стоп-кодона.секвенирование по Сэнгеру и пиросеквенирование - это два метода, которые имеют использовался для обнаружения мутаций сдвига рамки считывания, однако вероятно, что полученные данные будут не самого высокого качества. Тем не менее, с помощью секвенирования по Сэнгеру было идентифицировано 1,96 миллиона инделей, которые не перекрываются с другими базами данных. Когда наблюдается мутация со сдвигом рамки считывания, ее сравнивают с базой данных мутаций генома человека (HGMD), чтобы определить, оказывает ли мутация повреждающий эффект. Это делается путем изучения четырех функций. Во-первых, соотношение между пораженной и консервативной ДНК, во-вторых, расположение мутации относительно транскрипта, в-третьих, соотношение консервативных и затронутых аминокислот и, наконец, расстояние от инделя до конца экзона.
Массивно параллельное секвенирование - это новый метод, который можно использовать для обнаружения мутаций. Используя этот метод, можно одновременно секвенировать до 17 гигабаз, в отличие от ограниченных диапазонов для секвенирования по Сэнгеру только около 1 килобаз. Для проведения этого теста доступно несколько технологий, и сейчас рассматривается возможность его использования в клинических применениях. При тестировании на различные карциномы современные методы позволяют рассматривать только один ген за раз. Массивно параллельное секвенирование позволяет одновременно выявить множество мутаций, вызывающих рак, в отличие от нескольких конкретных тестов. Эксперимент по определению точности этого нового метода секвенирования, проверенный на 21 гене, не дал ложноположительных вызовов мутаций сдвига рамки считывания.
Патент США (5,958,684) в 1999 г. Leeuwen подробно описывает методы и реагенты для диагностики заболеваний, вызванных или связанных с геном, имеющим соматическую мутацию, приводящую к мутации сдвига рамки считывания. Способы включают в себя получение образца ткани или жидкости и проведение анализа гена на мутацию сдвига рамки считывания или белок из этого типа мутации. Нуклеотидная последовательность подозреваемого гена обеспечивается из опубликованных последовательностей генов или из клонирования и секвенирования подозрительного гена. Затем прогнозируется аминокислотная последовательность, кодируемая геном.
Несмотря на правила, которые регулируют генетический код и различные механизмы, присутствующие в клетке, чтобы гарантировать правильную передачу генетической информации во время в процессе репликации ДНК, а также при трансляции мутации действительно происходят; Мутация сдвига рамки считывания - не единственный тип. Есть по крайней мере два других типа распознаваемых точечных мутаций, а именно миссенс-мутация и бессмысленная мутация. Мутация со сдвигом рамки может кардинально изменить кодирующую способность (генетическую информацию) сообщения. Небольшие вставки или делеции (менее 20 пар оснований) составляют 24% мутаций, которые проявляются при признанном в настоящее время генетическом заболевании.
Мутации со сдвигом рамки считываются более распространенными в повторяющихся областях ДНК. Причиной этого является проскальзывание фермента полимеразы в повторяющихся областях, что позволяет мутациям войти в последовательность . Эксперименты можно запустить для определения частоты мутации сдвига рамки считывания, добавив или удаление заранее установленного количества нуклеотидов. Эксперименты проводились путем добавления четырех пар оснований, называемых экспериментами +4, но команда из Университета Эмори изучила разницу в частоте мутации как при добавлении, так и при удалении пары оснований. Было показано, что не было никакой разницы в частоте добавления и удаления пары оснований. Однако есть разница в конечном результате этого белка.
Болезнь Хантингтона является одним из девяти нарушений повторения кодонов, вызванных мутациями распространения полиглутамина, которые включают спино-мозжечковую атаксию (SCA) 1, 2, 6, 7 и 3, спинобульбарная мышечная атрофия и дентаторубально-паллидолизианатрофия. Может существовать связь между заболеваниями, вызванными мутациями экспансии полиглутамина и полиаланина, например сдвиг рамки считывания исходного продукта гена SCA3, кодирующего CAG / полиглутамины, на GCA / полиаланины. Рибосомное проскальзывание во время трансляции белка SCA3 было предложено как механизм, приводящий к переходу от полиглутамина к кодирующей полиаланин рамке. Динуклеотидная делеция или вставка одного нуклеотида в полиглутаминовый тракт экзона 1 хантингтина будет сдвигать CAG, кодирующую рамку полиглутамина на +1 (сдвиг рамки +1) к GCA, рамки, кодирующей полиаланин, и вводить новый эпитоп на С-конец Экзон 1 Htt (APAAAPAATRPGCG).
Некоторые заболевания имеют мутации сдвига рамки считывания, по крайней мере, как часть причины. Знание распространенных мутаций также может помочь в диагностике заболевания. В настоящее время делаются попытки использовать мутации сдвига рамки считывания с пользой для лечения заболеваний, изменяя рамку считывания аминокислот.
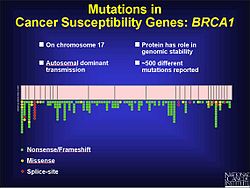 Частота мутаций гена BRCA1 на хромосоме 17
Частота мутаций гена BRCA1 на хромосоме 17  Частота мутаций гена BRCA2 на хромосоме 13
Частота мутаций гена BRCA2 на хромосоме 13 Известно, что мутации сдвига рамки считывания являются фактором колоректального поражения рак, а также другие виды рака с микросателлитной нестабильностью. Как указывалось ранее, мутации сдвига рамки считывания более вероятны в области повторяющейся последовательности. Когда репарация ошибочного спаривания ДНК не фиксирует добавление или удаление оснований, эти мутации с большей вероятностью будут патогенными. Это может быть отчасти потому, что опухоли не говорят перестать расти. Эксперименты на дрожжах и бактериях помогают выявить характеристики микросателлитов, которые могут способствовать исправлению дефектных несоответствий ДНК. К ним относятся длина микросателлита, состав генетического материала и чистота повторов. На основании экспериментальных результатов более длинные микросателлиты имеют более высокий уровень мутаций сдвига рамки считывания. Фланкирующая ДНК также может вносить вклад в мутации сдвига рамки считывания. При раке простаты мутация сдвига рамки считывания изменяет открытую рамку считывания (ORF) и предотвращает возникновение апоптоза. Это приводит к нерегулируемому росту опухоли. Хотя существуют факторы окружающей среды, которые способствуют прогрессированию рака простаты, существует также генетический компонент. Во время тестирования кодирующих областей для выявления мутаций было обнаружено 116 генетических вариантов, в том числе 61 мутация сдвига рамки считывания. На хромосоме 17 имеется более 500 мутаций, которые, по-видимому, играют роль в развитии рака груди и яичников в гене BRCA1, многие из которых связаны со сдвигом рамки считывания.
Болезнь Крона имеет ассоциация с геном NOD2. Мутация представляет собой вставку цитозина в положение 3020. Это приводит к преждевременному стоп-кодону, укорачивающему белок, который должен транскрибироваться. Когда белок способен нормально образовываться, он реагирует на бактериальные липосахариды, при этом мутация 3020insC не позволяет белку реагировать.
Муковисцидоз (CF) - заболевание, основанное на мутации в гене CF трансмембранного регулятора проводимости (CFTR). Выявлено более 1500 мутаций, но не все вызывают заболевание. Большинство случаев кистозного фиброза является результатом мутации ∆F508, которая удаляет всю аминокислоту. Две мутации сдвига рамки считывания представляют интерес для диагностики CF, CF1213delT и CF1154-insTC. Обе эти мутации обычно возникают вместе, по крайней мере, с одной другой мутацией. Оба они приводят к небольшому снижению функции легких и встречаются примерно у 1% обследованных пациентов. Эти мутации были идентифицированы с помощью секвенирования по Сэнгеру.
CCR5 - один из кофакторов проникновения в клетки, связанный с ВИЧ, наиболее часто участвующий в штаммах, не индуцирующих синцитий, наиболее очевиден у пациентов с ВИЧ. в отличие от больных СПИДом. Делеция 32 пары оснований в CCR5 была идентифицирована как мутация, которая сводит на нет вероятность ВИЧ-инфекции. Эта область на открытой рамке считывания ORF содержит мутацию сдвига рамки считывания, приводящую к преждевременному стоп-кодону. Это приводит к потере функции корецепторов ВИЧ in vitro. CCR5-1 считается диким типом, а CCR5-2 - мутантным аллелем. Те, у кого была гетерозиготная мутация CCR5, были менее восприимчивы к развитию ВИЧ. В исследовании, несмотря на высокую подверженность вирусу ВИЧ, не было ни одного гомозиготного по мутации CCR5, который дал бы положительный результат на ВИЧ.
Болезнь Тея – Сакса смертельна. заболевание, поражающее центральную нервную систему. Чаще всего встречается у младенцев и маленьких детей. Прогрессирование заболевания начинается в матке, но симптомы не проявляются примерно до 6-месячного возраста. От болезни нет лекарства. Известно, что мутации в гене β-гексозаминидазы A (Hex A) влияют на возникновение болезни Тея-Сакса; описано 78 мутаций различных типов, 67 из которых, как известно, вызывают заболевание. Большинство наблюдаемых мутаций (65/78) представляют собой замены одного основания или SNP, 11 делеций, 1 большую и 10 малых и 2 вставки. 8 из наблюдаемых мутаций - это сдвиг рамки считывания, 6 делеций и 2 вставки. Вставка из 4 пар оснований в экзон 11 наблюдается в 80% случаев болезни Тея-Сакса у ашкенази еврейского населения. Мутации сдвига рамки считывания приводят к раннему стоп-кодону, который, как известно, играет роль в заболевании у младенцев. Заболевание с отсроченным началом, по-видимому, вызвано 4 различными мутациями, одна из которых представляет собой делецию из 3 пар оснований.
Синдром Смита – Магениса (SMS) является сложным синдромом включая умственную отсталость, нарушение сна, поведенческие проблемы и различные черепно-лицевые, скелетные и висцеральные аномалии. В большинстве случаев SMS имеется общая делеция размером ~ 3,5 млн п.н., которая включает ген-1, индуцированный ретиноевой кислотой (RAI1). Другие случаи иллюстрируют изменчивость фенотипа SMS , ранее не показанную для мутации RAI1, включая потерю слуха, отсутствие самоуничижительного поведения и умеренные глобальные задержки. Секвенирование RAI1 выявило мутацию гептамерного тракта (ССКСС) в экзоне 3, приводящую к мутациям сдвига рамки считывания. Из семи сообщенных мутаций сдвига рамки считывания, встречающихся в поли C-трактах в RAI1, четыре случая (~ 57%) встречаются в этом гептамерном C-тракте. Результаты показывают, что этот гептамерный C-тракт является предпочтительной горячей точкой рекомбинации вставкой / удалением (SNindels) и, следовательно, основной целью для анализа у пациентов с подозрением на мутации в RAI1.
Гипертрофическая кардиомиопатия является наиболее частой причиной внезапной смерти у молодых людей, включая тренированных спортсменов, и вызывается мутациями в генах, кодирующих белки сердечного саркомера. Мутации в гене тропонина C (TNNC1) - редкая генетическая причина гипертрофической кардиомиопатии. Недавнее исследование показало, что мутация сдвига рамки считывания (c.363dupG или p.Gln122AlafsX30) в тропонине C была причиной гипертрофической кардиомиопатии (и внезапной сердечной смерти) у 19-летнего мужчины.
Лекарство от болезней, вызванных мутациями сдвига рамки считывания, - редкость. Исследования по этому поводу продолжаются. Одним из примеров является первичный иммунодефицит (ВЗОМТ), наследственное заболевание, которое может привести к увеличению числа инфекций. Есть 120 генов и 150 мутаций, которые играют роль в первичных иммунодефицитах. Стандартным лечением в настоящее время является генная терапия, но это лечение очень рискованно и часто может привести к другим заболеваниям, таким как лейкемия. Процедуры генной терапии включают изменение слитого белка с нуклеазой цинкового пальца, отщепление обоих концов мутации, что, в свою очередь, удаляет его из последовательности. Опосредованный антисмысловыми олигонуклеотидами пропуск экзона является еще одной возможностью для мышечной дистрофии Дюшенна . Этот процесс позволяет обойти мутацию, так что остальная часть последовательности остается в рамке, а функция белка остается неизменной. Это, однако, не излечивает болезнь, а только лечит симптомы и применимо только к структурным белкам или другим повторяющимся генам. Третьей формой репарации является ревертантный мозаицизм, который возникает в природе путем создания обратной мутации или мутации во втором сайте, который корректирует рамку считывания. Эта реверсия может происходить в результате внутригенной рекомбинации, митотической генной конверсии, сдвига ДНК второго сайта или сайт-специфической реверсии. Это возможно при нескольких заболеваниях, таких как Х-связанный тяжелый комбинированный иммунодефицит (ТКИД), синдром Вискотта – Олдрича и синдром Блума. Не существует лекарств или других фармакогеномных методов, которые помогают при ВЗОМТ.
В европейском патенте (EP1369126A1) от 2003 г., выданном Bork, описан метод, используемый для профилактики рака и для лечения рака и предраковых заболеваний, таких как ДНК- Спорадические опухоли с дефицитом репарации несоответствия (MMR) и опухоли, связанные с HNPCC. Идея состоит в том, чтобы использовать иммунотерапию с комбинаторными смесями опухолеспецифических пептидов, происходящих из мутации сдвига рамки считывания, чтобы вызвать цитотоксический Т-клеточный ответ, специфически направленный против опухолевых клеток.
| Викискладе есть медиафайлы, связанные с мутацией сдвига фреймов. |