 Образец спектра ЯМР 19F простого органического соединения. Интеграции показаны под каждым пиком.
Образец спектра ЯМР 19F простого органического соединения. Интеграции показаны под каждым пиком. 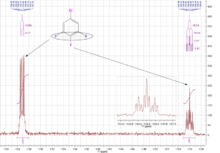 Спектр ЯМР 19F 1-бром-3,4,5-трифторбензола. В расширении показана схема спин-спинового взаимодействия, возникающая в результате взаимодействия пара-фтора с ядрами 2 метафтора и 2 орто-протонов.
Спектр ЯМР 19F 1-бром-3,4,5-трифторбензола. В расширении показана схема спин-спинового взаимодействия, возникающая в результате взаимодействия пара-фтора с ядрами 2 метафтора и 2 орто-протонов. Спектроскопия ядерного магнитного резонанса фтора-19 (ЯМР фтора или F ЯМР ) - это аналитический метод, используемый для обнаружения и идентификации фторсодержащих соединений. F является важным ядром для ЯМР-спектроскопии из-за его восприимчивости и большого химического сдвига дисперсии, которая больше, чем для протонной спектроскопии ядерного магнитного резонанса.
F имеет ядерный спин (I), равный 1/2, и высокое гиромагнитное отношение. Следовательно, этот изотоп очень чувствителен к измерениям ЯМР. Кроме того, F содержит 100% встречающегося в природе фтора. Единственные другие высокочувствительные ЯМР-активные ядра со спином 1/2, которые являются моноизотопными (или почти таковыми), - это H и P. Действительно, ядро F является третьим наиболее восприимчивым ядром ЯМР после ядра H и ядра H.
Химические сдвиги F ЯМР охватывают диапазон прибл. 800 частей на миллион. Для фторорганических соединений диапазон уже, составляя прибл. От -50 до -70 ppm (для групп CF 3) до -200 до -220 ppm (для групп CH 2 F). Очень широкий спектральный диапазон может вызвать проблемы при записи спектров, такие как плохое разрешение данных и неточная интеграция.
Также можно записывать разделенные спектры F {H} и H {F} и корреляции множественных связей F-C HMBC и космические спектры HOESY.
Химические сдвиги F ЯМР в литературе сильно различаются, обычно более чем на 1 ppm, даже в пределах одного и того же растворителя. Хотя эталонное соединение для спектроскопии F ЯМР, чистый CFCl 3 (0 ppm), использовалось с 1950-х годов, четких инструкций о том, как его измерять и использовать в обычных измерениях, не было до недавнего времени. Исследование факторов, влияющих на химический сдвиг в спектроскопии ЯМР фтора, показало, что растворитель имеет наибольшее влияние (Δδ = ± 2 ppm или более). Была подготовлена справочная таблица для конкретных растворителей с 5 внутренними справочными соединениями (CFCl 3, C6H5F, PhCF 3, C6F6 и CF3CO2H ), чтобы обеспечить воспроизводимое сопоставление с точностью Δδ = ± 30 частей на миллиард. Поскольку на химический сдвиг CFCl 3 также влияет растворитель, необходимо соблюдать осторожность при использовании растворенного CFCl 3 в качестве эталонного соединения в отношении химического сдвига чистого CFCl 3 (0 частей на миллион). Пример химических сдвигов, определенных для чистого CFCl 3 :
| CFCl 3 | C6H5F | PhCF 3 | C6F6 | CF3CO2H | |
|---|---|---|---|---|---|
| Растворитель | [ ppm] | [ppm] | [ppm] | [ppm] | [ppm] |
| CDCl 3 | 0,65 | -112,96 | -62,61 | -161,64 | -75,39 |
| CD2Cl2 | 0,02 | -113,78 | -62,93 | -162,61 | -75,76 |
| C6D6 | -0,19 | -113,11 | -62,74 | -163,16 | - 75,87 |
| Ацетон-d 6 | -1,09 | -114,72 | -63,22 | -164,67 | -76,87 |
Для полного Перечислите химические сдвиги эталонных соединений в 11 дейтерированных растворителях. Читатель отсылается к цитированной литературе.
Также недавно был предоставлен краткий список соответствующих ссылок на химические сдвиги более 240 фторированных химических веществ.
Химические сдвиги F ЯМР предсказать труднее, чем сдвиги H ЯМР. В частности, сдвиги F ЯМР сильно зависят от вкладов электронных возбужденных состояний, тогда как сдвиги H ЯМР преобладают за счет диамагнитных вкладов.
| -R | δ (м.д.) |
|---|---|
| H | -78 |
| CH3 | -62 |
| CH2CH3 | -70 |
| CH2NH2 | -72 |
| CH2OH | -78 |
| CH = CH 2 | -67 |
| C=CH | -56 |
| CF3 | -89 |
| CF2CF3 | -83 |
| F | -63 |
| Cl | -29 |
| Br | -18 |
| I | -5 |
| OH | -55 |
| NH2 | -49 |
| SH | -32 |
| C (= O) Ph | -58 |
| C (= O) CF 3 | -85 |
| C (= O) OH | -77 |
| C (= O) F | -76 |
| C (= O) OCH 2CH3 | -74 |
| -R | δ (м.д.) |
|---|---|
| H | -144 |
| CH3 | -110 |
| CH2CH3 | -120 |
| CF3 | -141 |
| CF2CF3 | -138 |
| C (= O) OH | -127 |
| -R | δ (м.д.) |
|---|---|
| H | -268 |
| CH3 | -212 |
| CH2CH3 | -212 |
| CH2OH | -226 |
| CF3 | -241 |
| CF2CF3 | -243 |
| C (= O) OH | -229 |
Для винилового фтора su b, следующая формула позволяет оценить химические соответствия F:
 где Z - статистический химический сдвиг заместителя (SSCS) для заместителя в указанном положении, а S - фактор взаимодействия. Некоторые типичные значения для использования в этом уравнении представлены в таблице ниже:
где Z - статистический химический сдвиг заместителя (SSCS) для заместителя в указанном положении, а S - фактор взаимодействия. Некоторые типичные значения для использования в этом уравнении представлены в таблице ниже: | Заместитель R | Zцис | Zтранс | Zгем |
|---|---|---|---|
| -H | -7,4 | -31,3 | 49,9 |
| -CH 3 | -6,0 | -43,0 | 9,5 |
| - CH = CH 2 | --- | --- | 47,7 |
| -Ph | -15,7 | -35,1 | 38,7 |
| -CF 3 | -25,3 | -40,7 | 54,3 |
| -F | 0 | 0 | 0 |
| -Cl | -16,5 | -29,4 | --- |
| -Br | -17,7 | -40,0 | --- |
| -I | -21,3 | -46,3 | 17,4 |
| -OCH 2CH3 | -77,5 | --- | 84,2 |
| Заместитель | Заместитель | Sцис / транс | Sцис / гем | Sтранс / гем |
|---|---|---|---|---|
| -H | -H | -26,6 | --- | 2,8 |
| -H | -CF 3 | -21,3 | --- | --- |
| -H | -CH 3 | --- | 11,4 | --- |
| -H | -OCH 2CH3 | -47.0 | --- | --- |
| -H | -Ph | -4.8 | --- | 5,2 |
| -CF 3 | -H | -7,5 | -10,6 | 12,5 |
| -CF 3 | -CF 3 | -5.9 | -5.3 | -4.7 |
| -CF 3 | -CH 3 | 17.0 | --- | --- |
| -CF 3 | -Ph | -15.6 | --- | -23.4 |
| -CH 3 | -H | --- | -12.2 | --- |
| -CH 3 | -CF 3 | --- | -13.8 | -8,9 |
| -CH 3 | -Ph | --- | -19,5 | -19,5 |
| -OCH 2CH3 | - H | -5.1 | --- | --- |
| -Ph | -H | --- | --- | 20,1 |
| -Ph | -CF 3 | -23.2 | --- | - - |
При определении химических сдвигов F ароматических атомов фтора, в частности фенилфторидов, существует другое уравнение, которое позволяет приблизительное значение. Заимствовано из «Определения структуры органических соединений», это уравнение:
 где Z - значение SSCS для заместителя в данном положении относительно атома фтора. Некоторые типичные значения для использования в этом уравнении представлены в таблице ниже:
где Z - значение SSCS для заместителя в данном положении относительно атома фтора. Некоторые типичные значения для использования в этом уравнении представлены в таблице ниже: | Заместитель | Zорто | Zмета | Zпара |
|---|---|---|---|
| -CH 3 | -3,9 | -0,4 | -3,6 |
| -CH = CH 2 | -4,4 | 0,7 | -0,6 |
| -F | -23,2 | 2,0 | -6,6 |
| -Cl | -0,3 | 3,5 | - 0,7 |
| -Br | 7,6 | 3,5 | 0,1 |
| -I | 19,9 | 3,6 | 1,4 |
| -OH | -23,5 | 0 | -13,3 |
| -OCH 3 | -18,9 | -0,8 | -9,0 |
| -NH 2 | -22,9 | -1,3 | -17,4 |
| -NO 2 | -5,6 | 3,8 | 9,6 |
| -CN | 6,9 | 4,1 | 10,1 |
| -SH | 10,0 | 0,9 | -3,5 |
| -CH (= O) | -7,4 | 2,1 | 10,3 |
| -C (= O) CH 3 | 2,5 | 1,8 | 7,6 |
| -C (= O) OH | 2,3 | 1,1 | 6,5 |
| -C (= O) NH 2 | 0,5 | -0,8 | 3,4 |
| -C (= O) OCH 3 | 3,3 | 3,8 | 7,1 |
| -C (= O) Cl | 3,4 | 3,5 | 12,9 |
Приведенные выше данные представляют только некоторые тенденции и молекулы. Для получения более полного списка тенденций в F-химических сдвигах можно обратиться к другим источникам и таблицам данных. Следует отметить, что исторически большинство литературных источников изменили соглашение об использовании негативов. Поэтому будьте осторожны со знаком значений, указанных в других источниках.
Константы взаимодействия F-F обычно больше, чем константы взаимодействия H-H. Обычно наблюдается связь F-F на большом расстоянии (J, J, J или даже J). Как правило, чем больше диапазон муфты, тем меньше значение. Водород соединяется с фтором, что очень характерно для спектра F. С геминальным водородом константы взаимодействия могут достигать 50 Гц. Другие ядра могут связываться с фтором, однако этого можно избежать, проведя эксперименты с независимой связью. Обычно ЯМР фтора проводят с развязкой как от углерода, так и от протона. Атомы фтора также могут соединяться друг с другом. Между атомами фтора константы гомоядерного взаимодействия намного больше, чем с атомами водорода. Геминальный фтор обычно имеет J-значение 250-300 Гц. Есть много хороших ссылок на значения констант связи. Цитаты включены ниже.
Чаще всего спектроскопию ЯМР F используют для анализа структуры фторорганических соединений. Репрезентативными целями этого метода являются многие фармацевтические препараты, содержащие связи C-F. Этот метод также используется для анализа фторидных солей.