 Проекция Фишера D- глицеральдегида
Проекция Фишера D- глицеральдегида 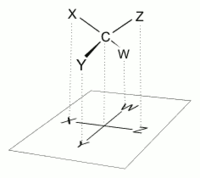 Проекция тетраэдрической молекулы на плоскую поверхность.
Проекция тетраэдрической молекулы на плоскую поверхность.  Визуализация проекции Фишера.
Визуализация проекции Фишера. проекция Фишера, разработанная Эмилем Фишером в 1891 году, представляет собой двумерное представление трехмерного органического молекула по проекции. Проекции Фишера были первоначально предложены для описания углеводов и использовались химиками, особенно в органической химии и биохимии. Не рекомендуется использовать проекции Фишера для неуглеводных диаграмм, поскольку такие рисунки неоднозначны, если их путают с рисунками других типов.
 Проекция Фишера с атомами углерода
Проекция Фишера с атомами углерода 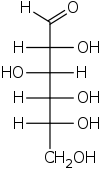 Проекция Фишера без атомов углерода
Проекция Фишера без атомов углерода  Проекция Натта Три разных проекции одной и той же молекулы (D- глюкоза )
Проекция Натта Три разных проекции одной и той же молекулы (D- глюкоза )Все нетонцевые связи изображены горизонтальными или вертикальными линиями. углеродная цепь изображена вертикально, причем атомы углерода иногда не показаны и представлены в центре пересекающихся линий (см. рисунок ниже). Ориентация углеродной цепи такова, что первый углерод (C1) находится наверху. В альдозе, C1 является углеродом альдегида ; в группе кетозы C1 представляет собой углерод, ближайший к группе кетона, которая обычно находится в группе C2.
В проекции Фишера все горизонтальные облигации предназначены для использования направлен к зрителю. Молекулы с простой тетраэдрической геометрией можно легко вращать в пространстве, так что это условие выполняется (см. Рисунки). Например, моносахарид с тремя атомами углерода (триоза ), такой как D- глицеральдегид, изображенный выше, имеет тетраэдрическую геометрию с C2 в его центре и может вращаться в пространстве. так что углеродная цепь расположена вертикально с C1 вверху, а горизонтальные связи, соединяющие C2 с -H и -OH, обе наклонены к зрителю.
Однако при создании проекции Фишера для моносахарида с более чем тремя атомами углерода нет способа ориентировать молекулу в пространстве так, чтобы все горизонтальные связи были наклонены к наблюдателю. После поворота молекулы так, чтобы обе горизонтальные связи с C2 были наклонены к наблюдателю, горизонтальные связи с C3 обычно будут наклонены в сторону. Итак, после построения связей с C2, перед тем, как нарисовать связи с C3, молекула должна быть повернута в пространстве на 180 ° вокруг своей вертикальной оси. Для завершения чертежа могут потребоваться другие подобные повороты.
Это означает, что в большинстве случаев проекция Фишера не является точным представлением реальной трехмерной конфигурации молекулы. Его можно рассматривать как проекцию модифицированной версии молекулы, идеально скрученной на нескольких уровнях вдоль ее основной цепи. Например, молекула с открытой цепью D- глюкозы, повернутая так, что горизонтальные связи с C2 наклонены к наблюдателю, будет иметь связи с C3 и C5, наклоненные от зритель, и, следовательно, его точная проекция не будет совпадать с проекцией Фишера. Для более точного представления молекулы с открытой цепью можно использовать проекцию Натта.
Согласно правилам IUPAC, все атомы водорода предпочтительно должны быть нарисованы явно; в частности, должны присутствовать атомы водорода концевой группы углеводов. В этом отношении проекция Фишера отличается от скелетных формул.
Проекции Фишера чаще всего используются в биохимии и органической химии для представления моносахаридов. Их также можно использовать для аминокислот или других органических молекул, хотя это не одобряется рекомендациями IUPAC 2006 года.
Проекция Фишера может использоваться для различения L- и D-молекулы. Например, по определению в проекции Фишера предпоследний (предпоследний) углерод D-сахаров изображен с водородом слева и гидроксилом <38.>справа. L-сахара будут показаны с водородом справа и гидроксилом слева.
проекции Хаворта - это родственные химические обозначения, используемые для представления сахаров в кольцевой форме. Группы в правой части проекции Фишера эквивалентны группам, расположенным ниже плоскости кольца в проекциях Хаворта. Проекции Фишера не следует путать с структурами Льюиса, которые не содержат никакой информации о трехмерной геометрии. Знаки клина и тире используются для представления стереохимии большинства классов органических соединений, а проекции Ньюмана используются для изображения конкретных конформаций вращающихся связей органических молекул (включая, но не ограничивается углеводами).
| Викискладе есть материалы, связанные с проекцией Фишера. |