| Синтаза жирных кислот | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 2.3.1.85 | ||||||||
| Номер CAS | 9045-77-6 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология гена | AmiGO / QuickGO | ||||||||
| |||||||||
| FASN | |||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||
| Псевдонимы | FASN, синтаза жирных кислот, Fasn, A630082H08Rik, FAS, OA-519, SDR27X1, синтаза жирных кислот | ||||||||||||||||||||||||
| Внешние идентификаторы | OMIM: 600212 MGI: 95485 HomoloGene: 55800 GeneCard: FASN | ||||||||||||||||||||||||
| Номер EC | 2.3.1.85 | ||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| |||||||||||||||||||||||||
| Ортологи | |||||||||||||||||||||||||
| Виды | Человек | Мышь | |||||||||||||||||||||||
| Entrez | |||||||||||||||||||||||||
| Ensembl | |||||||||||||||||||||||||
| UniProt |
| ||||||||||||||||||||||||
| RefSeq (мРНК) | |||||||||||||||||||||||||
| RefSeq (белок) н / д | |||||||||||||||||||||||||
| Просмотр / Edit Human | View / Edit Mouse |
Синтаза жирных кислот (FAS ) - это фермент, который у человека кодируется геном FASN .
Синтаза жирных кислот представляет собой мультифермент белок, который катализирует синтез жирных кислот. Это не один фермент, а целая ферментная система, состоящая из двух идентичных 272 кДа многофункциональных полипептидов, в которых субстраты передаются от одного функционального домена к другому..
Его основная функция - катализировать синтез пальмитата (C16: 0, длинноцепочечная насыщенная жирная кислота ) из ацетил-CoA и малонил-КоА, в присутствии НАДФН.
Жирные кислоты синтезируются серией реакций декарбоксилирования конденсации Клайзена из ацетил-КоА и малонил-КоА. После каждого раунда элонгации бета-кетогруппа восстанавливается до полностью насыщенной углеродной цепи за счет последовательного действия кеторедуктазы (KR), дегидратазы (DH) и еноила. редуктаза (ER). Растущая цепь жирных кислот переносится между этими активными центрами, будучи ковалентно присоединенной к фосфопантетеиновой простетической группе ацильного белка-носителя (ACP), и высвобождается под действием тиоэстеразы ( TE) при достижении длины углеродной цепи 16 (пальмитиновая кислота).
Есть два основных класса синтаз жирных кислот.
Механизм удлинения и восстановления FAS I и FAS II такой же, поскольку домены ферментов FAS II в значительной степени гомологичны их аналогам в домене в Мультиферментные полипептиды FAS I. Однако различия в организации ферментов - интегрированных в FAS I и дискретных в FAS II - порождают множество важных биохимических различий.
История эволюции синтаз жирных кислот очень тесно связана с историей поликетидсинтазы (PKS). Поликетидсинтазы используют аналогичный механизм и гомологичные домены для производства липидов вторичных метаболитов. Кроме того, поликетидсинтазы также демонстрируют организацию типа I и типа II. Считается, что FAS I у животных возник в результате модификации PKS I у грибов, тогда как FAS I у грибов и группы бактерий CMN, по-видимому, возник отдельно в результате слияния генов FAS II.
FAS млекопитающих состоит из гомодимера двух идентичных белковых субъединиц, в которых три каталитических домена в N-концевой секции (-кетоацилсинтаза (KS), малонил / ацетилтрансфераза (MAT) и дегидраза (DH)) разделены центральной областью из 600 остатков от четырех C-концевых доменов (еноилредуктаза (ER), -кетоацилредуктаза (KR), белок-носитель ацила ( ACP) и тиоэстераза (TE)).
Традиционная модель организации FAS (см. Модель «голова к хвосту» справа) в значительной степени основана на наблюдениях, что бифункциональный реагент 1,3 -дибромпропанон (DBP) способен сшивать активный центр цистеин тиол домена KS в одном мономере FAS с простетической группой фосфопантетеин ACP домен в другом мономере. Анализ комплементации димеров FAS, несущих различные мутации на каждом мономере, показал, что домены KS и MAT могут взаимодействовать с ACP любого мономера. и повторное исследование экспериментов по сшиванию DBP показало, что тиол Cys161 активного центра KS может быть сшит с тиолом ACP 4'- фосфопантетеин любого мономера. Кроме того, недавно сообщалось, что гетеродимерный FAS, содержащий только один компетентный мономер, способен к синтезу пальмитата.
Вышеупомянутые наблюдения кажутся несовместимыми с классическим принципом «голова к хвосту». модель для организации FAS, и была предложена альтернативная модель, предсказывающая, что домены KS и MAT обоих мономеров расположены ближе к центру димера FAS, где они могут получить доступ к ACP любой субъединицы (см. рисунок вверху справа).
Была решена структура рентгеновской кристаллографии с низким разрешением как FAS свиньи (гомодимер), так и дрожжевого FAS (гетерододекамер), а также структура FAS дрожжей с разрешением ~ 6 Å с разрешением ~ 6 Å (крио-ЭМ).
Решенные структуры дрожжевого FAS и FAS млекопитающих показывают две различные организации высококонсервативных каталитических доменов / ферментов в этой мультиферментной клеточной машине. Дрожжевой FAS имеет высокоэффективную жесткую бочкообразную структуру с 6 реакционными камерами, которые синтезируют жирные кислоты независимо, в то время как FAS млекопитающих имеет открытую гибкую структуру всего с двумя реакционными камерами. Однако в обоих случаях консервативный АСР действует как мобильный домен, ответственный за транспортировку промежуточных субстратов жирных кислот к различным каталитическим сайтам. Первое прямое структурное понимание этого механизма челночного перемещения субстрата было получено с помощью крио-ЭМ-анализа, при котором наблюдается связывание АСР с различными каталитическими доменами в бочкообразной синтазе жирных кислот дрожжей. Результаты крио-ЭМ предполагают, что связывание ACP с различными сайтами является асимметричным и стохастическим, на что также указывают исследования с компьютерным моделированием
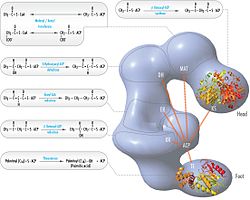 пересмотренная модель FAS с положениями полипептидов, трех каталитических доменов и их соответствующих реакции, визуализация Коси Граматикофф. Обратите внимание, что FAS активен только как гомодимер, а не как изображенный мономер. пересмотренная модель FAS с положениями полипептидов, трех каталитических доменов и их соответствующих реакции, визуализация Коси Граматикофф. Обратите внимание, что FAS активен только как гомодимер, а не как изображенный мономер. | 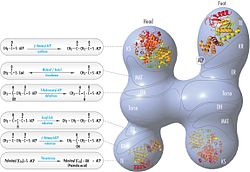 Модель FAS «голова-к-хвосту» с положениями полипептидов, тремя каталитическими доменами и их соответствующими реакциями, визуализация Коси Граматикофф. Модель FAS «голова-к-хвосту» с положениями полипептидов, тремя каталитическими доменами и их соответствующими реакциями, визуализация Коси Граматикофф. |
Метаболизм и гомеостаз синтазы жирных кислот транскрипционно регулируется вышестоящими стимулирующими факторами (USF1 и USF2 ) и белок, связывающий регуляторный элемент стерола -1c (SREBP-1c) в ответ на кормление / инсулин у живых животных.
Хотя рецептор Х печени (LXR) модулирует экспрессию белок, связывающий регуляторный элемент стерола -1c (SREBP-1c) при кормлении, регуляция FAS с помощью SREBP-1c зависит от USF.
Ацил флороглюцинолы, выделенные из папоротник Dryopteris crassirhizoma проявляет ингибирующую активность в отношении синтазы жирных кислот.
Ген, кодирующий FAS, был исследован как возможный онко ген. ФАС активируется при раке груди и желудка, а также является индикатором плохого прогноза и может быть полезной в качестве химиотерапевтической мишени. Следовательно, ингибиторы FAS являются активной областью исследований по открытию лекарств.
FAS также может участвовать в производстве эндогенного лиганда для ядерный рецептор PPARalpha, мишень фибратных препаратов для лечения гиперлипидемии, и исследуется как возможная мишень для лечения метаболического синдрома. Орлистат, который является Ингибитор желудочно-кишечной липазы также ингибирует FAS и имеет потенциал в качестве лекарства от рака.
В некоторых линиях раковых клеток этот белок был слит с рецептором эстрогена альфа (ER-альфа), в котором N-конец FAS слит в рамке с C-концом ER-альфа.
Ассоциация с лейомиомами матки.