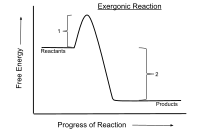
 Экзергоническая реакция (например, клеточное дыхание) - это реакция, которая высвобождает свободную энергию в процесс реакции. Ход реакции показан линией. Энергия активации (1) замедляет реакцию. Изменение свободной энергии Гиббса (ΔG) в экзергонической реакции (которая происходит при постоянном давлении и температуре) отрицательно, поскольку теряется энергия (2).
Экзергоническая реакция (например, клеточное дыхание) - это реакция, которая высвобождает свободную энергию в процесс реакции. Ход реакции показан линией. Энергия активации (1) замедляет реакцию. Изменение свободной энергии Гиббса (ΔG) в экзергонической реакции (которая происходит при постоянном давлении и температуре) отрицательно, поскольку теряется энергия (2). экзергоническая реакция - это химическая реакция, при которой изменение свободной энергии отрицательно (есть чистое высвобождение свободной энергии). Это указывает на спонтанную реакцию, если система закрыта и начальная и конечная температуры совпадают. Для процессов, которые происходят в замкнутой системе при постоянном давлении и температуре, используется свободная энергия Гиббса, тогда как энергия Гельмгольца актуальна для процессов, которые происходят при постоянном объеме и температуре.. Согласно второму закону термодинамики, любая реакция, протекающая при постоянной температуре без ввода электрической или фотонной энергии, является экергонической. Примером может служить клеточное дыхание.
Условно, выделение свободной энергии G в экзергонической реакции (при постоянном давлении и температуре) обозначается как

Хотя говорят, что экзэргонические реакции происходят спонтанно, это не означает, что реакция будет протекать с наблюдаемой скоростью. Например, диспропорционирование пероксида водорода высвобождает свободную энергию, но происходит очень медленно в отсутствие подходящего катализатора. Было высказано предположение, что нетерпеливый был бы более интуитивным термином в этом контексте.
В более общем плане термины экзэргонический и эндергонический относятся к свободной энергии изменение любого процесса, а не только химических реакций. Напротив, термины экзотермический и эндотермический относятся к изменению энтальпии в закрытой системе во время процесса, обычно связанного с обменом тепла.