 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Балверса |
| Другие названия | JNJ- 42756493 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a619031 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы введения. | Пероральный |
| Класс препарата | Азоторганические соединения |
| Законные статус | |
| Юридический статус |
|
| Идентификаторы | |
Название IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| PubChem SID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBEMBL <16845> | |
| ECHA InfoCard | 100.235.008 |
| Химические и физические данные | |
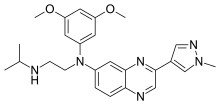
| Формула | C25H30N6O2 |
| Молярная масса | 446,555 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Эрдафитиниб представляет собой низкомолекулярный ингибитор рецептора фактора роста фибробластов (FGFR), одобренный для лечения рака и продаваемый под имя Бальверса . FGFR являются субпопуляцией тирозинкиназ, которые не регулируются в некоторых опухолях и влияют на дифференцировку клеток, пролиферацию, ангиогенез и выживаемость клеток. Astex Pharmaceuticals. обнаружил препарат и передал его Janssen Pharmaceuticals для дальнейшей разработки.
Исследователи изучили безопасность и эффективность эрдафитиниба при лечении рака желчных протоков., рак желудка, немелкоклеточный рак легкого и рак пищевода.
В марте 2018 года эрдафитиниб получил новейшую терапию обозначение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США для лечения уротелиального рака.
В апреле 2019 года эрдафитиниб получил одобрение FDA для лечения метастатического или местнораспространенного мочевого пузыря рак с изменением FGFR3 или FGFR2, который вышел за рамки традиционных методов лечения на основе платины и подлежит подтверждающему исследованию. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) считает его первым в своем классе.
Эрдафитиниб - это таблетка, которую принимают один раз в день с общей дозой 8 мг. Во время лечения доза эрдафитиниба может быть увеличена до 9 мг, если необходимо.
Общие побочные эффекты включают повышение уровня фосфатов, язвы во рту, чувство усталости, изменение функции почек, диарею, сухость во рту, отрыв ногтей от ложа или плохое формирование ногтя, изменение функции печени, низкий уровень соли (натрия), снижение аппетита, изменение вкусовых ощущений, низкий уровень эритроцитов (анемия), сухость кожи, сухость глаз и потеря волос. Другие побочные эффекты включают покраснение, отек, шелушение или болезненность на руках или ногах (синдром кистей и стоп), запор, боль в животе, тошноту и боль в мышцах.
Эрдафитиниб может вызвать серьезные проблемы с глазами, в том числе воспаление глаз, воспаление роговица (передняя часть глаза) и нарушения сетчатки, внутренней части глаза. Пациентам рекомендуется периодически проходить обследование глаз и сразу же сообщать своему лечащему врачу, если у них появятся нечеткое зрение, потеря зрения или другие визуальные изменения.
Эффективность эрдафитиниба изучалась в клиническом испытании (NCT02365597), в котором участвовали 87 взрослых с местнораспространенным или метастатическим раком мочевого пузыря, с генетическими изменениями FGFR3 или FGFR2, которые прогрессировали после лечения химиотерапией. Общий процент ответов у этих взрослых составил 32,2%, из которых 2,3% имели полный ответ и почти 30% имели частичный ответ. Ответ длился в среднем около пяти с половиной месяцев. Испытание проводилось в Азии, Европе и США.
Эрдафитиниб получил ускоренное одобрение. Для подтверждения клинической пользы эрдафитиниба требуются дальнейшие клинические испытания, и спонсор проводит или планирует провести эти исследования. Эрдафитинибу также был присвоен статус прорыв в терапии.
FDA предоставило Janssen Pharmaceutical разрешение на использование Balversa. FDA также одобрило набор Therascreen FGFR RGQ RT-PCR Kit, разработанный Qiagen Manchester, Ltd., для использования в качестве сопутствующей диагностики с Balversa для этого терапевтического показания.