 | |||
| |||
| Названия | |||
|---|---|---|---|
| Предпочтительное название IUPAC 2- (Хлорметил) оксиран | |||
| Другие названия (Хлорметил) оксиран. Эпихлоргидрин. 1-Хлор-2,3-эпоксипропан. γ-Оксид хлорпропилена. Глицидилхлорид | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 79785 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.003.128 | ||
| Номер EC |
| ||
| Справочник Гмелина | 164180 | ||
| KEGG | |||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Номер ООН | 2023 | ||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C3H5ClO | ||
| Молярная масса | 92,52 г / моль | ||
| Внешний вид | бесцветная жидкость | ||
| Запах | чеснок или хлороформ -подобный | ||
| Плотность | 1,1812 г / см | ||
| Температура плавления | -25,6 ° C (-14,1 ° F; 247,6 K) | ||
| Температура кипения | 117,9 ° C (244,2 ° F; 391,0 K) | ||
| Растворимость в воде | 7% (20 ° C) | ||
| Давление пара | 13 мм рт. ° C) | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| Пиктограммы GHS |      | ||
| Сигнальное слово GHS | Опасно | ||
| Предупреждения об опасности GHS | H226, H301, H311, H314, H317, H331, H350 | ||
| Меры предосторожности GHS | P201, P202, P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P271, P272, P280, P281, P301 + 310, P301 + 330 + 331, P302 + 352, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P308 + 313, P310, P311 | ||
| NFPA 704 (огненный алмаз) |  3 3 2 3 3 2 | ||
| Температура вспышки | 32 ° C (90 ° F; 305 K) | ||
| Пределы взрываемости | 3,8–21% | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LC50(me концентрация диана ) | 3617 частей на миллион (крыса, 1 час). 2165 частей на миллион (крыса, 1 час). 250 частей на миллион (крыса, 8 часов). 244 частей на миллион (крыса, 8 часов). 360 ppm (крыса, 6 часов) | ||
| LCLo(самый низкий опубликованный ) | 250 ppm (крыса, 4 часа) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимый) | TWA 5 ppm (19 мг / м3) [кожа] | ||
| REL (рекомендуется) | Канцероген | ||
| IDLH (непосредственная опасность) | Ca [75 ppm] | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки ink | |||
Эпихлоргидрин (сокращенно ECH ) представляет собой хлорорганическое соединение и эпоксид. Несмотря на свое название, это не галогидрин. Это бесцветная жидкость с резким запахом чеснока, умеренно растворимая в воде, но смешивающаяся с большинством полярных органических растворителей. Это хиральная молекула, обычно существующая в виде рацемической смеси правых и левых энантиомеров. Эпихлоргидрин представляет собой высокореактивное электрофильное соединение, которое используется в производстве глицерина, пластиков, эпоксидных клеев и смол, эпоксидных разбавителей и эластомеры.
Эпихлоргидрин традиционно производят из аллилхлорида в два этапа, начиная с добавления хлорноватистой кислоты, что дает смесь двух изомерных спиртов:
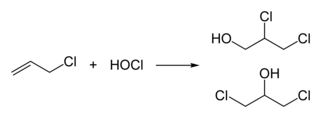
На втором этапе эту смесь обрабатывают основанием с получением эпоксида :

. Таким образом, более 800000 тонн (1997 г.) эпихлоргидрина производятся ежегодно.
Эпихлоргидрин был впервые описан в 1848 году Марселлином Бертело. Соединение было выделено во время исследований реакций между глицерином и газообразным хлористым водородом.
. Напоминая эксперимент Бертло, растения, производящие глицерин-эпихлоргидрин (GTE), были коммерциализированы. Эта технология использует дешевый глицерин, получаемый в результате переработки биотоплива. В процессе, разработанном Dow Chemical, глицерин претерпевает две реакции замещения при обработке хлороводородом в присутствии катализатора карбоновой кислоты . Это тот же промежуточный продукт, который образуется в процессе аллилхлорида / хлорноватистой кислоты, который затем аналогичным образом обрабатывается основанием с образованием эпихлоргидрина.

Способы, в которых задействовано меньшее количество хлорированных промежуточных продуктов, продолжают вызывать интерес. Один из таких процессов включает эпоксидирование аллилхлорида.
Эпихлоргидрин в основном превращается в бисфенол A диглицидил эфир, строительный блок при производстве эпоксидных смол. Он также является предшественником мономеров для других смол и полимеров. Другое использование - преобразование в синтетический глицерин. Однако быстрое увеличение производства биодизеля, где глицерин является побочным продуктом, привело к избытку глицерина на рынке, что сделало этот процесс неэкономичным. Синтетический глицерин сейчас используется только в чувствительных фармацевтических и биотехнологических приложениях, где стандарты качества очень высоки.
Эпихлоргидрин - универсальный прекурсор в синтезе многих органических соединений. Например, он превращается в энергетическое связующее, используемое во взрывчатых и метательных композициях. Эпихлоргидрин реагирует с нитратом щелочного металла, таким как нитрат натрия, с образованием глицидилнитрата и хлорида щелочного металла. Он используется в качестве растворителя для целлюлозы, смол и красок, и он нашел применение в качестве фумиганта от насекомых.
Используются полимеры, изготовленные из эпихлоргидрина, например, полиамид-эпихлоргидриновые смолы в бумажной арматуре и в пищевой промышленности для производства чайных пакетов, фильтров для кофе и оболочек для колбас / салями, а также при очистке воды.
Важное биохимическое применение эпихлоргидрин - это его использование в качестве сшивающего агента для производства сефадексных хроматографических смол с эксклюзионной хроматографией из декстранов.
Эпихлоргидрин классифицируется несколькими международными исследовательскими организациями и группами в области здравоохранения как вероятный или вероятный канцероген в людях. Длительное пероральное употребление высоких уровней эпихлоргидрина может привести к проблемам с желудком и повышенному риску рака. Воздействие эпихлоргидрина на рабочем месте при вдыхании может привести к раздражению легких и повышению риска рака легких.