| ELISA | |
|---|---|
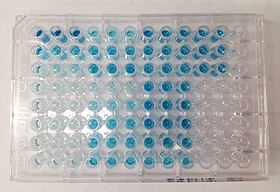 ELISA, разрабатываемый с TMB ELISA, разрабатываемый с TMB | |
| MeSH | D004797 |
| [редактировать в Викиданных ] | |
иммуноферментный анализ (ELISA ) (, ) - широко используемый аналитический биохимический анализ, впервые описанный Энгваллом и Перлманном в 1971 году. В этом анализе используется твердофазный иммуноферментный анализ . (EIA) для обнаружения присутствия лиганда (обычно белка) в жидком образце с использованием антител, направленных против измеряемого белка. ELISA использовался в качестве диагностического инструмента в медицине, патологии растений и биотехнологии, а также в качестве контроля качества в различных отрасли.
В наиболее простой форме ELISA антигены из исследуемого образца прикрепляются к поверхности. Затем соответствующее антитело наносится на поверхность, чтобы оно могло связывать антиген. Это антитело связывается с ферментом, а затем все несвязанные антитела удаляются. На заключительном этапе добавляется вещество, содержащее субстрат фермента. Если связывание имело место, последующая реакция дает детектируемый сигнал, чаще всего изменение цвета.
В проведении ELISA участвует по крайней мере одно антитело со специфичностью к конкретному антигену. Образец с неизвестным количеством антигена иммобилизован на твердой подложке (обычно полистирол микротитровальный планшет ) либо неспецифично (посредством адсорбции на поверхности) или конкретно (путем захвата другим антителом, специфичным к тому же антигену, в «сэндвич-методе ELISA»). После иммобилизации антигена добавляется детектирующее антитело, образующее комплекс с антигеном. Детектирующее антитело может быть ковалентно связано с ферментом или само может быть обнаружено вторичным антителом, которое связано с ферментом посредством биоконъюгирования. Между каждым этапом планшет обычно промывают мягким раствором детергента для удаления любых белков или антител, которые не связываются специфически. После последней стадии промывки планшет проявляют путем добавления ферментативного субстрата для получения видимого сигнала, который указывает количество антигена в образце.
Следует отметить, что ELISA может выполнять другие формы анализов связывания лиганда вместо строго «иммуно», хотя название носило исходное «иммуно» из-за общего использования и истории разработки. этого метода. По существу, для этого метода требуется любой лигирующий реагент, который может быть иммобилизован на твердой фазе, а также реагент обнаружения, который будет специфически связываться и использовать фермент для генерации сигнала, который может быть правильно определен количественно. В промежутках между промывками только лиганд и его специфические связывающие аналоги остаются специфически связанными или «иммуносорбированными» за счет взаимодействий антиген-антитело с твердой фазой, в то время как неспецифические или несвязанные компоненты вымываются. В отличие от других форматов спектрофотометрических лабораторных анализов, где одна и та же реакционная лунка (например, кювета) может быть повторно использована после промывки, в планшетах для ELISA продукты реакции иммуно сорбированы на твердой фазе, которая является частью планшета, поэтому их нелегко использовать.
В качестве аналитического биохимического анализа и метода «влажной лаборатории» ИФА включает обнаружение аналита (т. е. конкретного вещества, присутствие которого анализируется количественно или качественно) в жидкой пробе методом, продолжающим использовать жидкие реагенты во время анализа (т. е. контролируемая последовательность биохимических реакций, которая будет генерировать сигнал, который может быть легко определен количественно и интерпретирован как мера количества аналита в образце), который остается жидким и остается внутри реакционной камеры или колодца, необходимого для удержания реагентов. Это контрастирует с методами «сухой лаборатории», в которых используются сухие полоски. Даже если образец является жидким (например, измеренная маленькая капля), заключительный этап обнаружения в «сухом» анализе включает считывание высушенной полоски такими методами, как рефлектометрия, и не требует камеры сдерживания реакции для предотвращать перетекание или смешивание между образцами.
В качестве гетерогенного анализа ELISA разделяет некоторые компоненты аналитической реакционной смеси путем адсорбции определенных компонентов на твердой фазе, которая физически иммобилизована. В ELISA жидкий образец добавляется к неподвижной твердой фазе с особыми связывающими свойствами, за ним следует несколько жидких реагентов, которые последовательно добавляются, инкубируются и промываются с последующим некоторым оптическим изменением (например, проявлением окраски продуктом ферментативной реакции). реакция) в конечной жидкости в лунке, из которой измеряется количество аналита. Количественное «считывание» обычно основано на определении интенсивности прошедшего света с помощью спектрофотометрии, которая включает количественное определение пропускания света определенной длины волны через жидкость (а также прозрачное дно лунки в формат многолуночного планшета). Чувствительность обнаружения зависит от усиления сигнала во время аналитических реакций. Поскольку ферментативные реакции являются хорошо известными процессами амплификации, сигнал генерируется ферментами, которые связаны с реагентами обнаружения в фиксированных пропорциях, чтобы обеспечить точное количественное определение, и, следовательно, название «ферментно-связанный».
Аналитом является также называется лигандом, потому что он будет специфически связываться или лигировать с реагентом для обнаружения, таким образом, ELISA подпадает под большую категорию анализов связывания лиганда. Лиганд-специфический связывающий реагент «иммобилизован», то есть обычно наносится и сушится на прозрачном дне, а иногда и на боковой стенке лунки (здесь неподвижная «твердая фаза» / «твердая подложка», в отличие от твердых микрочастиц / гранул, которые может быть смыт), который обычно представляет собой многолуночный планшет, известный как «планшет для ELISA». Обычно, как и другие формы иммуноанализов, используется специфичность реакции типа антиген - антитело, потому что легко получить антитело, специфичное против антигена в массе. в качестве реагента. В качестве альтернативы, если сам аналит является антителом, его антиген-мишень может использоваться в качестве связывающего реагента.
До разработки ELISA единственным вариантом проведения иммуноанализа был радиоиммуноанализ, метод с использованием радиоактивно меченных антигенов или антител. В радиоиммуноанализе радиоактивность дает сигнал, который указывает, присутствует ли в образце конкретный антиген или антитело. Радиоиммуноанализ был впервые описан в научной статье Розалин Сассман Ялоу и Соломон Берсон, опубликованной в 1960 году.
Поскольку радиоактивность представляет потенциальную угрозу для здоровья, была предпринята попытка найти более безопасную альтернативу. Подходящая альтернатива радиоиммуноанализу могла бы заменить радиоактивный сигнал нерадиоактивным. Когда ферменты (такие как пероксидаза хрена ) реагируют с соответствующими субстратами (такими как ABTS или TMB ), происходит изменение цвета, которое используется как сигнал. Однако сигнал должен быть связан с присутствием антитела или антигена, поэтому фермент должен быть связан с подходящим антителом. Этот процесс связывания был независимо разработан Стратисом Аврамеасом и Г. Б. Пирсом. Поскольку необходимо удалить любое несвязанное антитело или антиген путем промывки, антитело или антиген необходимо зафиксировать на поверхности контейнера; т.е. должен быть приготовлен иммуносорбент. Методика достижения этого была опубликована Wide и Jerker Porath в 1966 году.
В 1971 году Питер Перлманн и Ева Энгвалл из Стокгольмского университета в Швеции и Антон Шуурс и Bauke van Weemen в Нидерландах независимо опубликовали статьи, в которых эти знания были синтезированы в методы для выполнения EIA / ELISA.
Традиционный ELISA обычно включает хромогенные репортеры и субстраты, которые вызывают заметное изменение цвета. для обозначения присутствия антигена или аналита. В более новых методах, подобных ELISA, используются репортеры флуорогенного, электрохемилюминесцентного и количественно-оппозиционной ПЦР для создания сигналов, поддающихся количественной оценке. Эти новые репортеры могут иметь различные преимущества, включая более высокую чувствительность и мультиплексирование. С технической точки зрения, новые анализы этого типа не являются строго ELISA, поскольку они не связаны с ферментом, а вместо этого связаны с некоторым неферментативным репортером. Однако, учитывая, что общие принципы этих анализов во многом схожи, их часто относят к той же категории, что и ELISA.
В 2012 году сверхчувствительный тест ELISA на основе ферментов с использованием наночастиц в качестве хромогенного репортера смог дать цветовой сигнал невооруженным глазом при обнаружении простых аттограмм аналита. Синий цвет отображается для положительных результатов, а красный - для отрицательных. Обратите внимание, что это обнаружение может подтвердить только присутствие или отсутствие аналита, но не фактическую концентрацию.
Существует множество тестов ELISA для определенных молекул, в которых используются соответствующие антитела. Тесты ELISA разбиты на несколько типов тестов в зависимости от того, как аналиты и антитела связаны и используются. Основные типы описаны здесь.
 Диаграмма прямого ИФА
Диаграмма прямого ИФА Этапы прямого ИФА следуют приведенному ниже механизму:
Фермент действует как усилитель; даже если остается связанным лишь несколько антител, связанных с ферментом, молекулы фермента будут производить много сигнальных молекул. В рамках здравого смысла фермент может производить цвет бесконечно долго, но чем больше антител связано, тем быстрее будет развиваться цвет. Основным недостатком прямого ELISA является то, что метод иммобилизации антигена не специфичен; когда в качестве источника тестируемого антигена используется сыворотка, все белки в образце могут прилипать к лунке микротитрационного планшета, поэтому небольшие концентрации аналита в сыворотке должны конкурировать с другими белками сыворотки при связывании с поверхностью лунки. Сэндвич-метод или непрямой ИФА обеспечивает решение этой проблемы за счет использования «захватывающего» антитела, специфичного для тестируемого антигена, для извлечения его из молекулярной смеси сыворотки.
ИФА может выполняться в качественном или количественном формате. Качественные результаты дают простой положительный или отрицательный результат (да или нет) для образца. Граница между положительным и отрицательным значениями определяется аналитиком и может быть статистической. Два или три раза стандартное отклонение (ошибка, присущая тесту) часто используется, чтобы отличить положительные образцы от отрицательных. В количественном ИФА оптическая плотность (ОП) образца сравнивается со стандартной кривой, которая обычно представляет собой серийное разведение раствора целевой молекулы с известной концентрацией. Например, если тестовая проба дает ОП, равную 1,0, точка на стандартной кривой, которая дает ОП = 1,0, должна иметь ту же концентрацию аналита, что и образец.
Использование и значение названия «косвенный ELISA »и« прямой ELISA »различаются в литературе и на веб-сайтах в зависимости от контекста эксперимента. Когда анализируется присутствие антигена, название «прямой ИФА» относится к ИФА, в котором используется только меченое первичное антитело, а термин «непрямой ИФА» относится к ИФА, в котором антиген связывается первичным антителом. который затем обнаруживается меченым вторичным антителом. В последнем случае сэндвич-ELISA четко отличается от непрямого ELISA. Когда представляет интерес «первичное» антитело, например в случае анализов иммунизации это антитело непосредственно выявляется вторичным антителом, и термин «непрямой ELISA» применяется к установке с двумя антителами.
 Сэндвич-ELISA . (1) Планшет покрыт захватывающим антителом; (2) добавляется образец, и любой присутствующий антиген связывается, захватывая антитело; (3) добавляется детектирующее антитело, которое связывается с антигеном; (4) добавляется связанное с ферментом вторичное антитело, которое связывается с детектирующим антителом; (5) добавляется субстрат, который ферментом превращается в детектируемую форму.
Сэндвич-ELISA . (1) Планшет покрыт захватывающим антителом; (2) добавляется образец, и любой присутствующий антиген связывается, захватывая антитело; (3) добавляется детектирующее антитело, которое связывается с антигеном; (4) добавляется связанное с ферментом вторичное антитело, которое связывается с детектирующим антителом; (5) добавляется субстрат, который ферментом превращается в детектируемую форму. "сэндвич" ELISA используется для обнаружения антигена в образце. Этапы следующие:
Изображение справа включает использование вторичного антитела, конъюгированного с ферментом, однако в с технической точки зрения в этом нет необходимости, если первичное антитело конъюгировано с ферментом (что могло бы быть прямым ELISA). Однако использование конъюгата вторичное антитело позволяет избежать дорогостоящего процесса создания ферментно-связанных антител для каждого антигена, который может потребоваться обнаружить. При использовании связанного с ферментом антитела, которое связывает Fc-область других антител, это же связанное с ферментом антитело можно использовать в различных ситуациях. Без первого слоя «захватывающего» антитела любые белки в образце (включая белки сыворотки) могут конкурентно адсорбироваться на поверхности планшета, снижая количество иммобилизованного антигена. Использование очищенного специфического антитела для прикрепления антигена к пластику устраняет необходимость очищать антиген от сложных смесей перед измерением, упрощая анализ и повышая специфичность и чувствительность анализа. Сэндвич-ELISA, используемый для исследований, часто требует подтверждения из-за риска получения ложноположительных результатов.
Третье использование ELISA - это конкурентное связывание. Этапы этого ELISA несколько отличаются от первых двух примеров:
Немеченое антитело инкубируют в присутствии его антигена (образца).
Некоторые конкурентные наборы ELISA включают в себя связанный с ферментом антиген, а не антитело, связанное с ферментом. Меченый антиген конкурирует за сайты связывания первичного антитела с антигеном образца (немеченым). Чем меньше антигена в образце, тем больше меченого антигена остается в лунке и тем сильнее сигнал.
Обычно антиген не помещается в лунку первым.
Для обнаружения антител к ВИЧ лунки микротитрационного планшета покрывают антигеном ВИЧ. Используются два специфических антитела: одно конъюгировано с ферментом, а другое присутствует в сыворотке (если сыворотка положительна на антитело). Кумулятивная конкуренция происходит между двумя антителами за один и тот же антиген, что приводит к появлению более сильного сигнала. В эти лунки добавляют анализируемую сыворотку и инкубируют при 37 ° C, а затем промывают. Если антитела присутствуют, происходит реакция антиген-антитело. Для специфических антител к ВИЧ, меченных ферментом, не остается антигена. Эти антитела остаются свободными при добавлении и смываются во время промывки. Субстрат добавлен, но на нем нет фермента, поэтому положительный результат не показывает изменения цвета.
Четвертый тест ELISA не использует традиционные лунки. Этот тест оставляет антигены суспендированными в тестовой жидкости.
Этот тест позволяет пометить и подсчитать несколько антигенов одновременно. Это позволяет идентифицировать определенные штаммы бактерий по двум (или более) разным цветным меткам. Если в ячейке присутствуют оба тега, то это конкретный штамм. Если присутствует только один, его нет.
Этот тест, как правило, выполняется по одному за раз и не может быть проведен с планшетом для микротитрования. Необходимое оборудование обычно менее сложное и может использоваться в полевых условиях.
В следующей таблице перечислены ферментные маркеры, обычно используемые в анализах ELISA, которые позволяют измерять результаты анализа по завершении.
 Человеческий анти-IgG, сэндвич-ELISA с двумя антителами
Человеческий анти-IgG, сэндвич-ELISA с двумя антителами Поскольку ELISA может быть выполнен для оценки либо наличия антигена, либо наличия антитела в образце, он является полезным инструментом для определения концентраций антител сыворотки (например, с тестом на ВИЧ или вирус Западного Нила ). Он также нашел применение в пищевой промышленности при обнаружении потенциальных пищевых аллергенов, таких как молоко, арахис, грецкие орехи, миндаль и яйца и в качестве серологического анализа крови на целиакию. ELISA может также использоваться в токсикологии как быстрый презумптивный скрининг определенных классов лекарств.
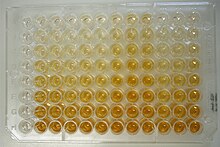
 Планшет для иммуноферментного анализа
Планшет для иммуноферментного анализа ELISA был первым скрининговым тестом, широко используемым на ВИЧ из-за его высокой чувствительности. В ELISA сыворотку человека разводят в 400 раз и наносят на планшет, к которому прикреплены антигены ВИЧ. Если в сыворотке крови присутствуют антитела к ВИЧ, они могут связываться с этими антигенами ВИЧ. Затем планшет промывают для удаления всех остальных компонентов сыворотки. Затем на планшет наносят специально подготовленное «вторичное антитело» - антитело, которое связывается с другими антителами, после чего проводят еще одну промывку. Это вторичное антитело заранее химически связано с ферментом.
Таким образом, планшет будет содержать фермент пропорционально количеству вторичного антитела, связанного с планшетом. Применяется субстрат для фермента, и катализ ферментом приводит к изменению цвета или флуоресценции. Результаты ELISA представлены в виде числа; Наиболее спорным аспектом этого теста является определение точки отсечения между положительным и отрицательным результатом.
Точка отсечения может быть определена путем сравнения ее с известным стандартом. Если тест ELISA используется для скрининга наркотиков на рабочем месте, устанавливается пороговая концентрация, например, 50 нг / мл, и будет подготовлен образец, содержащий стандартную концентрацию аналита. Неизвестные, которые генерируют более сильный сигнал, чем известный образец, являются «положительными». Те, которые генерируют более слабый сигнал, считаются «отрицательными».
Д-р Деннис Э. Бидвелл и Алистер Воллер создали тест ELISA для выявления различных заболеваний, таких как денге, малярия, болезнь Шагаса, болезнь Джона и другие. ELISA-тесты также используются в диагностике in vitro в медицинских лабораториях. Другие применения ELISA включают: