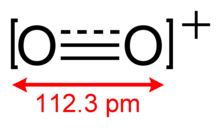
диоксигенилион, O. 2, является редко встречающимся оксикатионом, в котором оба атома кислорода имеют формальный степень окисления +1/2. Формально он получается из кислорода путем удаления электрона :
. Изменение энергии для этого процесса называется энергией ионизации молекулы кислорода. По сравнению с большинством молекул эта энергия ионизации очень высока и составляет 1175 кДж / моль. В результате область химии O. 2весьма ограничена, действуя в основном как одноэлектронный окислитель.
O. 2имеет порядок связи, равный 2,5, и длину связи , равную 112,3 мкм в твердом O 2 [AsF 6 ]. Он изоэлектронен с оксидом азота и является парамагнитным. Энергия связи составляет 625,1 кДж · моль, а частота растяжения составляет 1858 см, оба значения являются высокими по сравнению с большинством молекул.
Нил Бартлетт продемонстрировал, что диоксигенилгексафтороплатинат (O2PtF 6), содержащий диоксигенильный катион, может быть получен при комнатной температуре путем прямой реакции газообразный кислород (O 2) с гексафторидом платины (PtF 6):
Соединение также может быть приготовленным из смеси газов фтора и кислорода в присутствии платиновой губки при 450 ° C и из дифторида кислорода (OF. 2) выше 400 ° C:
При более низких температурах (около 350 ° C) вместо него получают тетрафторид платины диоксигенилгексафтороплатината. Диоксигенилгексафтороплатинат сыграл ключевую роль в открытии соединений благородных газов. Наблюдение за тем, что PtF 6 является достаточно мощным окислителем для окисления O 2 (который имеет первый потенциал ионизации 12,2 эВ ) привел Бартлетта к выводу, что он также должен быть способен окислять ксенон (первый потенциал ионизации 12,13 эВ). Его последующее исследование дало первое соединение благородного газа, гексафтороплатинат ксенона.
O. 2также обнаружен в аналогичных соединениях формы O 2MF6, где M - мышьяк (As), сурьма (Sb), золото (Au), ниобий (Nb), рутений (Ru), рений (Re), родий (Rh), ванадий (V) или фосфор (P). Также подтверждены другие формы, включая O 2 GeF 5 и (O 2)2SnF 6.
Тетрафторборатные и гексафторфосфатные соли могут быть получены реакцией дифторида диоксида с трифторидом бора или пентафторидом фосфора при -126 ° C:
Эти соединения быстро разлагаются при комнатной температуре:
Некоторые соединения, включая O 2Sn2F9, O 2Sn2F9· 0,9HF, O 2 GeF 5 · HF и O 2 [Hg ( HF)] 4 (SbF 6)9может быть получен ультрафиолетовым облучением кислорода и фтора, растворенного в безводном фтористом водороде, с оксидом металла.
Реакция из O 2BF4с ксеноном при 173 K (-100 ° C) дает белое твердое вещество, предположительно F – Xe – BF 2, содержащее необычную связь ксенон-бор:
Диоксигенил sa lts O 2BF4и O 2 AsF 6 реагируют с монооксидом углерода с образованием оксалилфторида, C 2O2F2с высоким содержанием yield.