 | |
 | |
| Названия | |
|---|---|
| Другие названия Диметилсульфат; Диметиловый эфир серной кислоты; Me 2SO4; ДМСО 4 ; Диметиловый эфир серной кислоты; Метил сульфат | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.000.963 |
| KEGG | |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
| Свойства | |
| Химическая формула | C2H6O4S |
| Молярная масса | 126,13 г / моль |
| Внешний вид | Бесцветная маслянистая жидкость |
| Запах | слабый, луковичный |
| Плотность | 1,33 г / мл, жидкость |
| Точка плавления | -32 ° C (-26 ° F; 241 K) |
| Температура кипения | 188 ° C (370 ° F; 461 K) (разлагается) |
| Растворимость в воде | Реагирует |
| Растворимость | Метанол, дихлорметан, ацетон |
| Давление пара | 0,1 мм рт. ст. (20 ° C) |
| Магнитная восприимчивость (χ) | -62,2 · 10 см / моль |
| Опасности | |
| Основные опасности | Чрезвычайно токсичный, контактный, опасность вдыхания, коррозия, опасность для окружающей среды, канцерогенный, мутагенный |
| R-фразы (устаревшие) | R45, R25, R26, R34,. R43, R68 |
| S-фразы (устаревшие) | S53, S45, S30, S60, S61 |
| NFPA 704 (огненный алмаз) |  2 4 1 2 4 1 |
| Температура вспышки | 83 ° C; 182 ° F; 356 K |
| Смертельная доза или концентрация (LD, LC): | |
| LC50(средняя концентрация ) | 8,6 ppm (крыса, 4 часа). 75 ppm (морская свинка, 20 мин). 53 ppm (мышь). 32 ppm (морская свинка, 1 час) |
| LCLo(самый низкий опубликованный ) | 97 ppm (человек, 10 мин) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 1 ppm (5 мг / м) [кожа] |
| REL (Рекомендуется) | Ca TWA 0,1 ppm (0,5 мг / м) [кожа] |
| IDLH (Непосредственная опасность) | Ca [7 ppm] |
| Родственные соединения | |
| Родственные соединения | Диэтилсульфат, метилтрифлат, диметилкарбонат |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
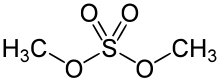
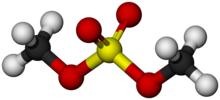
Диметилсульфат представляет собой химическое соединение с формулой (CH 3O)2SO2. Поскольку сложный диэфир из метанол и серная кислота, его формула часто записывается как (CH3 )2SO4 или Me 2SO4, где CH 3 или Me означает метил. Me 2SO4в основном используется d в качестве метилирующего агента в органическом синтезе.
Me2SO4представляет собой бесцветную маслянистую жидкость с легким луковичным запахом (хотя запах ее может свидетельствовать о значительном воздействии). Как все сильные алкилирующие агенты, Me 2SO4чрезвычайно токсичен. Его использование в качестве лабораторного реагента до некоторой степени заменено метилтрифлатом, CF 3SO3CH3, метиловым эфиром трифторметансульфоновой кислоты.
Диметилсульфат был обнаружен в начале 19 века в неочищенной форме. Позднее П. Клаессон подробно изучил его приготовление. Он использовался в химической войне в Первую мировую войну.
Диметилсульфат может быть синтезирован в лаборатории множеством различных методов, самым простым из которых является этерификация серной кислоты с помощью метанол :
Другой возможный синтез включает дистилляцию метилгидросульфата:
Метилнитрит и метилхлорсульфонат также приводят к диметилсульфату:
Me2SO4коммерчески производится с 1920-х годов. Обычным процессом является непрерывная реакция диметилового эфира с триоксид серы.
Диметилсульфат наиболее известен как реагент для метилирования фенолов, аминов и тиолов. Одна метильная группа переносится быстрее, чем вторая. Предполагается, что перенос метила происходит через S Реакция N 2. По сравнению по сравнению с другими метилирующими агентами, диметилсульфат предпочтительнее в промышленности из-за его низкой стоимости и высокой реакционной способности.
Чаще всего Me 2SO4используется для метилирования фенолов. Некоторые простые спирты также подходящим образом метилированы, как показано на примере превращения трет-бутанола в трет-бутилметиловый эфир :
Алкоксидные соли быстро метилируются:
Метилирование сахаров называется метилированием по Хаворту .
Me2SO4используется для получения обоих соли четвертичного аммония или третичные амины :
Кватернизованные жирные аммониевые соединения используются в качестве поверхностно-активного вещества или смягчителей тканей. Метилирование с образованием третичного амина показано как:
Аналогично метилированию спиртов, соли меркаптидов легко метилируются Me 2SO4:
Пример:
Этот метод был использован для получения сложных тиоэфиров:
Диметилсульфат (DMS) используется для определения вторичной структуры из РНК. При нейтральном pH DMS метилирует неспаренные остатки аденина и цитозина на их канонических лицевых сторонах Уотсона-Крика, но не может метилировать нуклеотиды, спаренные по основанию. Используя метод, известный как DMS-MaPseq, РНК инкубируют с DMS для метилирования неспаренных оснований. Затем РНК подвергается обратной транскрипции; обратная транскриптаза часто добавляет неправильное основание ДНК, когда встречается с метилированным основанием РНК. Эти мутации можно обнаружить с помощью секвенирования, и предполагается, что РНК является одноцепочечной по основаниям с частотой мутаций выше фоновой.
Диметилсульфат может влиять на специфическое для оснований расщепление ДНК, воздействуя на кольца имидазола, присутствующие в гуанине. Диметилсульфат также метилирует аденин в одноцепочечных частях ДНК (например, в тех, где белки, такие как РНК-полимераза, постепенно плавятся и повторно отжигают ДНК). При повторном отжиге эти метильные группы мешают образованию пары оснований аденин-гуанин. Нуклеазу S1 затем можно использовать для разрезания ДНК в одноцепочечных областях (в любом месте с метилированным аденином). Это важный метод анализа взаимодействий белок-ДНК.
Хотя диметилсульфат очень эффективен и доступен, его токсичность побуждает использовать другие метилирующие реагенты. Метилиодид представляет собой реагент, используемый для O-метилирования, как и диметилсульфат, но менее опасен и более дорогой. Диметилкарбонат, который менее реакционноспособен, имеет гораздо более низкую токсичность по сравнению с обоими диметилсульфат и метилиодид. Высокое давление можно использовать для ускорения метилирования диметилкарбонатом. В общем, токсичность метилирующих агентов коррелирует с их эффективностью в качестве реагентов переноса метила.
Диметилсульфат канцерогенный и мутагенный, очень ядовитый, коррозионный и экологически опасно. Диметилсульфат всасывается через кожу, слизистые оболочки и желудочно-кишечный тракт и может вызывать замедленную реакцию дыхательных путей со смертельным исходом. Часто встречается глазная реакция. Нет сильного запаха или немедленного раздражения, предупреждающих о смертельной концентрации в воздухе. LD50 (острая, пероральная) составляет 205 мг / кг (крыса) и 140 мг / кг (мышь), а LC50 (острая) составляет 45 частей на миллион / 4 часа (крыса). Давление пара 65 Па достаточно велико, чтобы создать смертельную концентрацию в воздухе за счет испарения при 20 ° C. Отсроченная токсичность позволяет произойти потенциально смертельному воздействию до появления каких-либо предупреждающих симптомов. Симптомы могут проявиться через 6–24 часа. Концентрированные растворы оснований (аммиак, щелочи) могут использоваться для гидролиза незначительных разливов и остатков на загрязненном оборудовании, но реакция может стать бурной с большим количеством диметилсульфата (см. ICSC). Хотя соединение гидролизуется, нельзя предполагать, что обработка водой обеззараживает диметилсульфат.