 | |
 | |
| Имена | |
|---|---|
| Название IUPAC гидрофосфат кальция | |
| Другие имена гидрофосфат кальция,. кальциевая соль фосфорной кислоты (1: 1) | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.028.933 |
| E number | E341 (ii) (антиоксиданты,...) |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
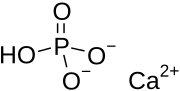
| Химическая формула | CaHPO 4 |
| Молярная масса | 136,06 г / моль (безводный). 172,09 (дигидрат) |
| Внешний вид | белый порошок |
| Запах | без запаха |
| Плотность | 2,929 г / см (безводный). 2,31 г / см (дигидрат) |
| Температура плавления | разлагается |
| Растворимость в воде | 0,02 г / 100 мл (безводный). 0,02 г / 100 мл (дигидрат) |
| Структура | |
| Кристаллическая структура | триклинная |
| Опасности | |
| NFPA 704 (огненный алмаз) |  0 1 0 0 1 0 |
| Температура вспышки | Невоспламеняющийся |
| Родственные соединения | |
| Другое анионы | пирофосфат кальция |
| другие катионы | фосфат магния. монокальцийфосфат. трикальцийфосфат. |
| Если не указано иное, данные для материалов приведены в их стандарте состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
Дикальцийфосфат - это фосфат кальция с формулой CaHPO 4 и его дигидрат. Префикс «ди» в общепринятом названии возникает потому, что образование аниона HPO 4 включает удаление двух протонов из фосфорной кислоты, H 3PO4. Он также известен как двухосновный фосфат кальция или моногидрофосфат кальция . Дикальцийфосфат используется как пищевая добавка, он содержится в некоторых зубных пастах как полировальный агент и является биоматериалом.
Двухосновный фосфат кальция получают нейтрализацией гидроксида кальция с помощью фосфорной кислоты, которая осаждает дигидрат в виде твердого вещества. При 60 ° C осаждается безводная форма:
Для предотвращения разложения, которое может привести к образованию гидроксиапатита, пирофосфата натрия или октагидрат тримагнийфосфата добавляются, когда, например, дигидрат двухосновного фосфата кальция должен использоваться в качестве полирующего агента в зубной пасте.
В непрерывном процессе CaCl 2 можно обработать (NH 4)2HPO 4 с образованием дигидрата:
Затем суспензию дигидрата нагревают примерно до 65–70 ° C с образованием безводного CaHPO 4 в виде кристаллического осадка, обычно в виде плоских кристаллов алмазоида, которые подходят для дальнейшей обработки.
Дигидрат двухосновного фосфата кальция образуется в кальций-фосфатных цементах «брушит» (CPC), которые имеют медицинское применение. Пример общей реакции схватывания при образовании «β-TCP / MCPM» (β- трикальцийфосфат / монокальцийфосфат ) фосфор кальция Фатные цементы:
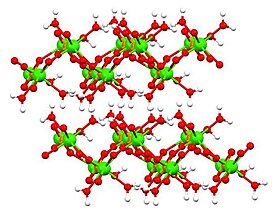
 Часть решетки дигидрата дикальцийфосфата, выделяя 8-скоординированный Ca-центр и расположение протонов на трех лигандах (зеленый = Ca, красный = кислород, оранжевый = фосфор, белый = водород)
Часть решетки дигидрата дикальцийфосфата, выделяя 8-скоординированный Ca-центр и расположение протонов на трех лигандах (зеленый = Ca, красный = кислород, оранжевый = фосфор, белый = водород) Известны три (3) формы дикальцийфосфата:
Структура безводных и дигидратированных форм была определена с помощью рентгеновской кристаллографии и Структура моногидрата была определена с помощью электронной кристаллографии. Дигидрат (показанный в таблице выше), а также моногидрат имеют слоистую структуру.
.
Двухосновный фосфат кальция в основном используется в качестве пищевой добавки в приготовленных сухих завтраках, лакомствах для собак, обогащенной муке и продуктах из лапши. Он также используется в качестве таблетирующего агента в некоторых фармацевтических препаратах, включая некоторые продукты, предназначенные для устранения запаха тела. Двухосновный фосфат кальция также содержится в некоторых пищевых добавках с кальцием (например, Bonexcin). Используется в кормах для птицы. Он также используется в некоторых зубных пастах в качестве средства для предотвращения образования зубного камня .
Нагревание дикальцийфосфата дает дифосфат дикальция, полезный полирующий агент:
В форме дигидрата (брушита) он обнаружен в некоторых камнях в почках и в зубных камнях.