
Группа диазопредставляет собой органический фрагмент, состоящий из двух связанные атомы азота (азо ) в концевом положении. С нейтральным зарядом органические соединения, содержащие диазогруппу, связанную с атомом углерода, называются диазосоединениями или диазоалканами и описываются общей структурной формулой R 2 C = N = N. Простейшим примером диазосоединения является диазометан, CH 2N2. Диазосоединения (R 2 C = N 2) не следует путать с азосоединениями типа RN = NR или с соединениями диазония типа RN 2.
Электронная структура диазосоединений характеризуется π-электронной плотностью, делокализованной по α- углерода и двух атомов азота, а также ортогональной π-системы с электронной плотностью, делокализованной только по концевым атомам азота. Поскольку все резонансные формы диазосоединений, удовлетворяющие правилу октетов, имеют формальные заряды, они являются членами класса соединений, известных как 1,3-диполи. Некоторые из наиболее стабильных диазосоединений представляют собой α-диазо-β-дикетоны и α-диазо-β-диэфиры, в которых электронная плотность дополнительно делокализована в электроноакцепторную карбонильную группу. Напротив, большинство диазоалканов без электроноакцепторных заместителей, включая сам диазометан, взрывоопасны. Коммерчески подходящим диазосоединением является этилдиазоацетат (N2CHCOOEt). Группа изомерных соединений, обладающих лишь несколькими подобными свойствами, представляет собой диазирины, в которых углерод и два атома азота связаны в виде кольца.
Можно выделить четыре резонансные структуры :

Соединения с диазогруппой следует отличать от соединений диазония, которые имеют ту же концевую азогруппу, но несут общий положительный заряд и азосоединения, в которых азогруппа связывает два органических заместителя.
Диазосоединения были впервые получены Питером Гриссом, который открыл новую универсальную химическую реакцию, как подробно описано в его статье 1858 года «Предварительное замечание о влиянии закиси азота. кислота на аминонитро- и аминодинитрофенол. "
Существует несколько методов получения диазосоединений.
Замещенные альфа-акцептором первичные алифатические амины R-CH 2 -NH 2 (R = COOR, CN, CHO, COR) реагируют с азотистой кислотой с образованием генерируют диазосоединение.
Примером электрофильного замещения с использованием диазометильного соединения является реакция между ацилгалогенидом и диазометан, например, первая стадия в синтезе Арндта-Эйстера.
В диазоперенос некоторые углеродные кислоты реагируют с тозилазидом в присутствии слабого основания, такого как триэтиламин или DBU. Побочным продуктом является соответствующий тозиламид (п-толуолсульфонамид). Эта реакция также называется диазопереносом Регица . Примерами являются синтез трет-бутилдиазоацетата и диазомалоната. Метилфенилдиазоацетат получают таким образом, обрабатывая метилфенилацетат п-ацетамидобензолсульфонилазидом в присутствии основания.
 Структура твердого состояния диазосоединения t-BuO 2 CC (N 2)C6H4NO2. Ключевые расстояния: CN = 1,329 Å, NN = 1,121 Å.
Структура твердого состояния диазосоединения t-BuO 2 CC (N 2)C6H4NO2. Ключевые расстояния: CN = 1,329 Å, NN = 1,121 Å. Механизм включает атаку енолята на концевом азоте, перенос протона и изгнание аниона сульфонамида.Использование β-карбонилальдегида приводит к деформилирующему варианту переноса Регитца, который полезен для получения диазосоединений, стабилизированных только одной карбонильной группой.

.
Диазосоединения могут быть получены реакцией элиминирования N-алкил-N-нитрозосоединений, например, при синтезе диазометана из Диазальда или MNNG :
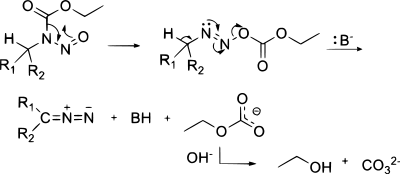
(Показанный здесь механизм является одной из возможных. Для альтернативного механизма аналогичного образования диазометта не из N-нитрозосульфонамида, см. страницу Диазальд.)
Гидразоны являются окисленными (дегидрированием ), например, с оксидом серебра или оксидом ртути, например, синтез 2-диазопропана из гидразона ацетона. Другими окисляющими реагентами являются тетраацетат свинца, диоксид марганца и реагент Сверна. Тозилгидразоны RRC = N-NHT реагируют с основанием, например, триэтиламином, в синтезе кротилдиазоацетата и в синтезе фенилдиазометана из PhCHNHT и метоксид натрия.
За реакцией карбонильной группы с гидразин 1,2-бис (трет-бутилдиметилсилил) гидразином с образованием гидразона следует реакция с иоданом. дифториодбензол дает диазосоединение:

1,3-дизамещенные алкиларил триазены могут быть фрагментированы с образованием диазосоединений. Эти триазены (ArN = NNH-CH 2 R) образуются в результате сочетания ароматических солей диазония с первичными аминами, но тип реакции встречается редко.
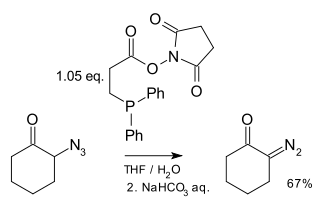
Описан один метод синтеза диазосоединений из азидов с использованием фосфинов :
Диазосоединения реагируют как 1,3-диполи в диазоалкан, 1,3-диполярные циклоприсоединения.
Диазосоединения используются в качестве предшественников карбенов, которые генерируются термолизом или фотолизом, например, в перегруппировке Вольфа. Как таковые, они используются в циклопропанировании, например, в реакции этилдиазоацетата с стиролом. Некоторые диазосоединения могут соединяться с образованием алкенов в формальной реакции димеризации карбена.
Диазосоединения являются промежуточными соединениями в реакции Бэмфорда-Стивенса тозилгидразонов до алкенов, опять же с карбеновым промежуточным соединением:

В Дойле-Кирмс реакция Некоторые диазосоединения реагируют с аллилсульфидами с образованием гомоаллилсульфида. Внутримолекулярные реакции диазокарбонильных соединений обеспечивают доступ к циклопропанам. В расширении цикла Бюхнера диазосоединения реагируют с ароматическими кольцами с расширением цикла.
Реакция Бюхнера-Курциуса-Шлоттербека дает кетоны из альдегидов и алифатических диазосоединений:

Тип реакции - нуклеофильное присоединение.
Диазогруппу присущи два семейства продуктов природного происхождения: кинамицин и. Эти молекулы являются интеркаляторами ДНК с диазофункциональностью в качестве «боеголовок». Потеря N 2, индуцированная восстановительно, приводит к образованию расщепляющего ДНК флуоренильного радикала.