| D-Ala-D-Ala карбоксипептидаза серинового типа | |||||||||
|---|---|---|---|---|---|---|---|---|---|
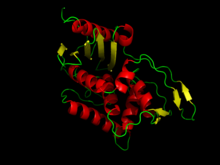 Структура DD-транспептидазы стрептомицетов K15 Структура DD-транспептидазы стрептомицетов K15 | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 3.4. 16.4 | ||||||||
| Номер CAS | 9077-67-2 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
DD-транспептидаза (EC 3.4.16.4, DD-пептидаза, DD-транспептидаза, DD-карбоксипептидаза, D-аланил-D-аланин карбоксипептидаза, D-аланил-D-аланин-расщепляющая пептидаза, D-аланинкарбоксипептидаза, D-аланилкарбоксипептидаза и D-Ala-D серинового типа -Ala карбоксипептидаза.) Представляет собой бактериальный фермент, который катализирует перенос RL-aca-D-аланила фрагмента доноров карбонила RL-aca-D-аланил-D-аланина к γ-OH их серин активного сайта и от него до конечного акцептора. Он участвует в биосинтезе бактериальной клеточной стенки, а именно в транспептидации, которая сшивает боковые пептидные цепи цепей пептидогликана.
антибиотик пенициллин необратимо связывается и ингибирует активность фермента транспептидазы за счет образования высокостабильного промежуточного пенициллоил-фермента. Из-за взаимодействия между пенициллином и транспептидазой этот фермент также известен как пенициллин-связывающий белок (PBP).
DD-транспептидаза механически аналогична протеолитическим реакциям семейства белков трипсина.
 Каталитический механизм DD-транспептидазы
Каталитический механизм DD-транспептидазы Сшивание пептидильных фрагментов соседних цепей гликана двухступенчатая реакция. Первая стадия включает расщепление связи D-аланил-D-аланин предшественника пептидной единицы, действующего как донор карбонила, высвобождение карбоксильного конца D-аланина и образование ацил-фермента. Второй этап включает разрушение промежуточного соединения ацил-фермент и образование новой пептидной связи между карбонилом D-аланильного фрагмента и аминогруппой другого пептидного элемента.
Большинство дискуссий о механизмах DD-пептидазы вращается вокруг катализаторов переноса протона. Во время образования промежуточного ацил-фермента протон должен быть удален из гидроксильной группы серина активного центра и один должен быть добавлен к уходящей группе амина. Подобное движение протонов должно облегчаться при деацилировании. Идентичность общих кислотных и основных катализаторов, участвующих в этих переносах протонов, еще не выяснена. Однако были предложены каталитическая триада тирозин, лизин и серин, а также серин, лизин, серин.
Транспептидазы являются членами суперсемейства пенициллоил-серинтрансфераз , имеющий сигнатуру SxxK, сохраняющуюся мотив. С обозначением «x» вариабельного аминокислотного остатка , транспептидазы этого суперсемейства демонстрируют тенденцию в форме трех мотивов: SxxK, SxN (или аналог) и KTG (или аналог). Эти мотивы встречаются в эквивалентных местах и примерно на равных расстояниях вдоль полипептидной цепи. Уложенный белок приближает эти мотивы друг к другу в каталитическом центре между доменом all-α и доменом α / β. Когда «x» обозначает вариабельный аминокислотный остаток аминокислотный, транспептидазы этого суперсемейства демонстрируют тенденцию в виде трех мотивов: SxxK, SxN (или аналог) и KTG (или аналог). Эти мотивы встречаются в эквивалентных местах и примерно на равных расстояниях вдоль полипептидной цепи. Уложенный белок сближает эти мотивы в каталитическом центре между доменом all-α и доменом α / β.
Структура стрептомицетов K15 DD-транспептидаза была изучена и состоит из одной полипептидной цепи, организованной в два домена. Один домен содержит в основном α-спирали, а второй - α / β-типа. Центр каталитической щели занят тетрадой Ser35-Thr36-Thr37-Lys38, которая включает нуклеофильный остаток Ser35 на аминоконцевом конце спирали α2. Одна сторона полости определяется петлей Ser96-Gly97-Cys98, соединяющей спирали α4 и α5. Триада Lys213-Thr214-Gly215 лежит на цепи β3 на противоположной стороне полости. NH-группа основной цепи основного остатка Ser35 и группа Ser216, расположенная ниже мотива Lys213-Thr214-Gly215, занимают положения, совместимые с функцией оксианионной дыры, необходимой для катализа.
Фермент классифицируется как DD-транспептидаза, поскольку восприимчивая пептидная связь донора карбонила простирается между двумя атомами углерода с D-конфигурацией.
Все бактерии обладают по крайней мере одним, чаще всего несколько монофункциональных сериновых DD-пептидаз.
 Структурное сходство между (A) D-Ala-D-Ala концом пептидогликанового конца и (B) пенициллинами. Транспептидазы неправильно распознают пенициллины для каталитической реакции TPase.
Структурное сходство между (A) D-Ala-D-Ala концом пептидогликанового конца и (B) пенициллинами. Транспептидазы неправильно распознают пенициллины для каталитической реакции TPase. Этот фермент является отличной мишенью для лекарств, поскольку он необходим, доступен из периплазмы и не имеет эквивалента в клетках млекопитающих. DD-транспептидаза является белком-мишенью для β-лактамных антибиотиков (например, пенициллина ). Это связано с тем, что структура β-лактама очень похожа на остаток D-ala-D-ala.
β-лактамы проявляют свое действие путем конкурентной инактивации каталитического сайта сериновой DD-транспептидазы. Пенициллин является циклическим аналогом доноров карбонила с концевыми D-Ala-D-Ala, поэтому в присутствии этого антибиотика реакция останавливается на уровне пенициллоильного фермента, связанного с сериновым эфиром. Таким образом, β-лактамные антибиотики заставляют эти ферменты вести себя как связывающие пенициллин белки..
Кинетически взаимодействие между DD-пептидазой и бета-лактамами представляет собой трехступенчатую реакцию:
Бета-иактамы могут образовывать аддукт EI * с высокой стабильностью с DD-транспептидазой. Период полураспада этого аддукта составляет около часов, тогда как период полураспада нормальной реакции составляет порядка миллисекунд.
Вмешательство в ферментные процессы, ответственные за формирование клеточной стенки, приводит к лизису и гибели клеток из-за к запуску автолитической системы у бактерий.