| Комплекс цитохрома b6f | |||||||||
|---|---|---|---|---|---|---|---|---|---|
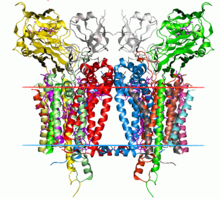 Кристаллическая структура комплекса цитохрома b6f из C. reinhardtii (1q90 ). Углеводородные границы липидного бислоя показаны красными и синими линиями (сторона тилакоидного пространства и сторона стромы соответственно). Кристаллическая структура комплекса цитохрома b6f из C. reinhardtii (1q90 ). Углеводородные границы липидного бислоя показаны красными и синими линиями (сторона тилакоидного пространства и сторона стромы соответственно). | |||||||||
| Идентификаторы | |||||||||
| Символ | B6F | ||||||||
| Pfam | PF05115 | ||||||||
| InterPro | IPR007802 | ||||||||
| TCDB | 3.D.3 | ||||||||
| суперсемейство OPM | 92 | ||||||||
| белок OPM | 4pv1 | ||||||||
| мембранома | 258 | ||||||||
| |||||||||
| Цитохром b 6 f комплекс | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| номер EC | 1.10.99.1 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
Комплекс цитохрома b 6f (пластохинол-пластоцианинредуктаза; EC 1.10.99.1 ) представляет собой фермент, обнаруженный в тилакоиде мембрана в хлоропластах растений, цианобактериях и зеленых водорослях, которая катализирует перенос электронов от пластохинола к пластоцианину. Реакция аналогична реакции, катализируемой цитохромом bc 1 (Комплекс III) митохондриальной цепи переноса электронов. Во время фотосинтеза комплекс цитохрома b 6 f представляет собой одну ступень в цепи, которая переносит электроны от Фотосистемы II к Фотосистеме. I, и в то же время закачивает протоны в тилакоидное пространство, что способствует созданию электрохимического (энергетического) градиента, который позже используется для синтеза АТФ из АДФ.
Комплекс цитохрома b 6 f представляет собой димер, каждый мономер состоит из восьми субъединиц. Они состоят из четырех больших субъединиц: цитохрома f 32 кДа с цитохромом c-типа, цитохрома b 6 25 кДа 6 с группой гема с низким и высоким потенциалом, группы гема 19 кДа железо-серный белок Риске, содержащий кластер [2Fe-2S] и субъединицу IV 17 кДа; вместе с четырьмя небольшими субъединицами (3-4 кДа): PetG, PetL, PetM и PetN. Общая молекулярная масса 217 кДа.
Кристаллическая структура комплексов цитохрома b 6 f из Chlamydomonas reinhardtii, Mastigocladus ламиносус и Nostoc sp. Был определен РСС 7120.
Ядро комплекса структурно аналогично ядру цитохрома bc 1. Цитохром b 6 и субъединица IV гомологичны цитохрому b, и белки железо-сера Риске этих двух комплексов гомологичны. Однако цитохром f и цитохром c 1 не гомологичны.
Цитохром b 6 f содержит семь простетических групп. Четыре обнаружены как в цитохроме b 6 f, так и в bc 1 : гем c-типа цитохрома c 1 и f, два гема b-типа ( b p и b n) в bc 1 и b 6 f, и кластер [2Fe-2S] белка Риске. В цитохроме b 6 f обнаружены три уникальные простетические группы: хлорофилл a, β-каротин и гем c n (также известный как гем x).
Межмономерное пространство в ядре димера комплекса цитохрома b6f занято липидами, которые обеспечивают направленность переноса электронов между гемом и гемом за счет модуляции диэлектрического окружения внутри белка. 73>
 Табак (Nicotiana tabacum ), мутант по цитохрому b 6 f (справа) рядом с нормальным растением. Растения используются в исследованиях фотосинтеза для изучения циклического фотофосфорилирования.
Табак (Nicotiana tabacum ), мутант по цитохрому b 6 f (справа) рядом с нормальным растением. Растения используются в исследованиях фотосинтеза для изучения циклического фотофосфорилирования. В фотосинтезе комплекс цитохрома b 6 f функционирует, опосредуя перенос электронов между двумя комплексами реакционных центров фотосинтеза., из Фотосистемы II в Фотосистемы I, при переносе протонов из стромы хлоропласта через тилакоидную мембрану в просвет. Транспорт электронов через цитохром b 6 f отвечает за создание протонного градиента, который управляет синтезом АТФ в хлоропластах.
В отдельной реакции комплекс цитохрома b 6 f играет центральную роль в циклическом фотофосфорилировании, когда НАДФ недоступен для приема электронов от восстановленного ферредоксин. Этот цикл приводит к созданию протонного градиента цитохромом b 6 f, который можно использовать для управления синтезом АТФ. Также было показано, что этот цикл важен для фотосинтеза, в котором предлагается поддерживать правильное соотношение выработки АТФ / НАДФН для фиксации углерода.
Реакции депротонирования-окисления p-стороны хинола в цитохроме. Комплекс b6f вовлечен в образование активных форм кислорода. Предполагается, что интегральная молекула хлорофилла, расположенная внутри участка окисления хинола, выполняет структурную, нефотохимическую функцию, увеличивая скорость образования активных форм кислорода, возможно, обеспечивая окислительно-восстановительный путь для внутриклеточной коммуникации.
Комплекс цитохрома b 6 f отвечает за «нециклический » (1) и «циклический "(2) перенос электрона между двумя мобильными окислительно-восстановительными носителями, пластохиноном (QH 2) и пластоцианином (Pc):
| H2O | → | фотосистема II | → | QH2 | → | Cyt b 6f | → | Pc | → | фотосистема I | → | NADPH | (1) |
| QH2 | → | Cyt b 6f | → | Pc | → | фотосистема I | → | Q | (2) | ||||
Цитохром b 6 f катализирует перенос электронов от пластохинола к пластоцианину, перекачивая два протона из стромы в просвет тилакоида:.
Эта реакция происходит через цикл Q, как в Комплексе III. Пластохинон действует s в качестве переносчика электронов, передавая два своих электрона в высоко- и низкопотенциальные электронные транспортные цепи (ETC) посредством механизма, называемого бифуркацией электронов. Комплекс содержит до трех природных молекул пластохинона (PQ), которые образуют сеть переноса электронов, которые отвечают за функционирование цикла Q и его окислительно-восстановительные и каталитические функции в фотосинтезе.
 Q-цикл цитохрома b 6f
Q-цикл цитохрома b 6fПервая половина Q-цикла
Вторая половина цикла Q
В отличие от Комплекса III, цитохром b 6 f катализирует другой перенос электрона r действие, которое является центральным для циклического фотофосфорилирования. Электрон от ферредоксина (Fd) переносится на пластохинон, а затем в комплекс цитохрома b 6 f для восстановления пластоцианина, который повторно окисляется P700 в Фотосистеме I. Точный механизм того, как пластохинон восстанавливается ферредоксином, все еще ведутся исследования. Одно из предположений состоит в том, что существует ферредоксин: пластохинонредуктаза или НАДФ-дегидрогеназа. Поскольку гем x, по-видимому, не требуется для цикла Q и не содержится в Комплексе III, было предложено использовать его для циклического фотофосфорилирования по следующему механизму: