| цистатионин-бета-лиаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
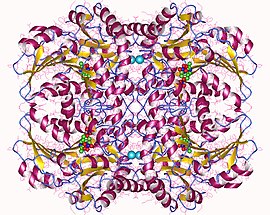 Тетрамер цистатионин-бета-лиазы, E.Coli Тетрамер цистатионин-бета-лиазы, E.Coli | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 4.4.1.8 | ||||||||
| Номер CAS | 9055-05-4 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология генов | AmiGO / QuickGO | ||||||||
| |||||||||
Цистатионин-бета-лиаза (EC 4.4.1.8 ), также часто упоминаемых как CBL или β-цистатионаза, представляет собой фермент, который в первую очередь катализирует следующее g α, β-элиминирование реакция

Таким образом, субстратом этого фермента является L-цистатионин, тогда как его 3 продукта составляют гомоцистеин, пируват и аммиак.
. Обнаружены в растениях, бактериях и дрожжах, цистатионин бета-лиаза является неотъемлемой частью пути биосинтеза метионина , поскольку гомоцистеин может быть напрямую преобразован в метионин с помощью метионинсинтазы. Фермент принадлежит к семейству PLP-зависимых ферментов из-за использования пиридоксаль-5'-фосфат (PLP) кофактора для расщепления цистатионина. Фермент также принадлежит к семейству лиаз, в частности к классу углерод-серных лиаз. систематическое название этого класса ферментов - L-цистатионин L-гомоцистеинлиаза (дезаминирующая; пируват-образующая) . Этот фермент участвует в 5 метаболических путях : метаболизм метионина, метаболизм цистеина, метаболизм азота и метаболизм серы.
Цистатионин-бета-лиаза - это тетрамер состоит из идентичных субъединиц и сконструирован как димер димеров, каждый из которых связан с одной молекулой PLP, связанной с каталитический центр остатком лизина . Димер образован двумя мономерами, связанными посредством нескольких электростатических, водородных связей и гидрофобных взаимодействий, тогда как тетрамер стабилизируется посредством взаимодействий между N-концевыми доменами и ключевыми α-спиралями.
Большинство остатков каталитических сайтов фермента законсервированы среди ферментов, участвующих в пути транссульфирования. К другим членам относятся цистатионин гамма-синтаза, цистатионин гамма-лиаза и метионин гамма-лиаза. Кроме того, эти структуры демонстрируют складку типа I и принадлежат к семейству аспартатаминотрансферазы (AAT), характеризующемуся гомодимерами с диэдральной симметрией и активными сайтами, состоящими из остатков. принадлежность к соседним субъединицам.
 Димер цистатионин-бета-лиазы. N-концевой домен показан зеленым, PLP-связывающий домен показан красным, а C-концевой домен показан голубым. Запись в PDB: 4ITX
Димер цистатионин-бета-лиазы. N-концевой домен показан зеленым, PLP-связывающий домен показан красным, а C-концевой домен показан голубым. Запись в PDB: 4ITX Мономер цистатионин-бета-лиазы состоит из трех функционально и структурно различных доменов:
Состоит из трех α- спиралей и одной бета-нити, которые способствуют формированию четвертичной структуры. Этот домен содержит остатки, которые взаимодействуют с активным сайтом соседней субъединицы для облегчения связывания субстрата и кофактора.
Содержит большую часть каталитически релевантных остатков на ферменте. Он состоит из α-спиралей и β-листов с четким параллельным семинитевым β-листом. Эти листы образуют изогнутую структуру вокруг спирали, связывающей PLP. PLP ковалентно присоединен к остатку лизина на С-конце листа.
Наименьший домен на ферменте, который присоединен к PLP-связывающий домен в виде длинной изогнутой α-спирали. Домен структурирован в четырехцепочечный антипараллельный β-лист с соседними спиралями.
Помимо связывания с остатком лизина, PLP фиксируется внутри сайт связывания субстрата фермента посредством различных взаимодействий с каталитическими остатками. Амин - и гидроксил -содержащие остатки расположены на расстоянии водородных связей с четырьмя фосфатными атомами кислорода. Считается, что эта фосфатная группа вносит основной вклад в защиту PLP в активном центре. Кроме того, остатки, соседствующие с пиридином азотом в PLP, помогают стабилизировать его положительный заряд, тем самым усиливая его электрофильный характер.
ароматическое кольцо в PLP фиксируется на месте почти копланарным тирозиновым остатком. Считается, что эта конфигурация увеличивает характер поглощения электронов кофактора. Эти стэкинг-взаимодействия между PLP и ароматическими боковыми цепями можно найти в большинстве PLP-зависимых ферментов, поскольку они играют важную роль в катализе реакции, облегчая трансальдиминирование.
 Остатки ключевых связывающих доменов, взаимодействующие с PLP. Остатки, принадлежащие соседней субъединице CBL Arabidopsis, показаны синим цветом. Запись в PDB: 1IBJ
Остатки ключевых связывающих доменов, взаимодействующие с PLP. Остатки, принадлежащие соседней субъединице CBL Arabidopsis, показаны синим цветом. Запись в PDB: 1IBJ Как показано в механизме ниже, цистатионин-бета-лиаза способствует расщеплению связи SC в цистатионине с использованием PLP. кофактор, связанный с каталитическим остатком лизина. Первоначально для проведения реакции трансальдиминирования необходима депротонированная аминогруппа. Учитывая, что оптимум pH для фермента составляет от 8,0 до 9,0, остаток тирозина в каталитическом кармане существует в виде фенолята, который отщепляет протон от α-аминогруппы субстрат. На следующем этапе депротонированный амин подвергается нуклеофильной атаке и замещает лизин с образованием основания Шиффа, образуя внутренний альдимин.
. Освободившийся лизин теперь может абстрагироваться. протон из C и образуют хиноид промежуточное соединение, чему способствует делокализация отрицательного заряда по конъюгированной p-системе PLP. Впоследствии протонирование S вызывает разрыв связи C-S, высвобождая тем самым гомоцистеин
Внешний альдимин замещается нуклеофильной атакой лизина, регенерируя каталитически активный внутренний альдимин и высвобождая дегидроаланин. Наконец, енамин таутомеризуется в имин, который подвергается гидролитическому дезаминированию с образованием пирувата и аммиака.
 Механизм, катализируемый цистатионин-бета-лиазой. Кофактор и каталитические остатки показаны синим цветом.
Механизм, катализируемый цистатионин-бета-лиазой. Кофактор и каталитические остатки показаны синим цветом. Растительные и бактериальные цистатионин-бета-лиазы ингибируются антимикробной аминокислотой, L-аминоэтоксибинилглицином (AVG) и антибактериальная аминокислота, ризобитоксин.
Цистатионин-бета-лиаза в растениях демонстрирует двухступенчатый процесс инактивации механизма с помощью AVG, в котором образуется обратимый комплекс фермент-ингибитор. образовались до необратимой инактивации фермента:

Избыточное добавление цистатионина предотвращало инактивацию фермента, предполагая, что AVG действует как конкурентный ингибитор по отношению к цистатионину. Кроме того, было показано, что фермент чувствителен к тиол -блокирующим ингибиторам, таким как N-этилмалеимид и идоацетамид.
В отличие от растений, цистатионин-бета-лиаза в бактериях проявляет одностадийный механизм ингибирования:
С помощью кинетических методов и рентгеновской кристаллографии было выявлено зависящее от времени ингибирование с медленным связыванием. наблюдаемый. Считается, что ингибитор связывается с ферментом так же, как и субстрат; однако после отщепления α-протона реакция продолжается с образованием неактивного производного PLP кетимина.
 AVG, связанный с каталитическим PLP в сайте связывания субстрата CBL E. coli. Запись в PDB: 1CL2
AVG, связанный с каталитическим PLP в сайте связывания субстрата CBL E. coli. Запись в PDB: 1CL2 Arabidopsis цистатионин-бета-лиаза обладает 22% гомологией с его аналогом Escherichia coli и даже более высокой гомологией (от 28% до 36%). %) с цистатионин-λ-синтазой из растительных и бактериальных источников и цистатионин-λ-лиазой из Saccharomyces cerevisiae. Все эти ферменты участвуют в пути биосинтеза Cys / Met и относятся к одному классу PLP-зависимых ферментов, что позволяет предположить, что эти ферменты произошли от общего предка.
Цистатионин-бета-лиаза катализирует выработку гомоцистеина, прямого предшественника метионина. Метионин является незаменимой аминокислотой для бактерий, которая необходима для синтеза белка и синтеза S-аденозилметионина ; таким образом, аминокислота напрямую связана с репликацией ДНК . Из-за необходимости в репликации ДНК ингибирование цистатионин-бета-лиазы является привлекательной мишенью для антибиотиков. Кроме того, этот фермент отсутствует у людей, что снижает вероятность вредных и нежелательных побочных эффектов.
. Исследования связывают противогрибковую активность некоторых противогрибковых агентов с ингибированием цистатионин-бета-лиазы; однако другие исследования не наблюдали ингибирования ферментов ими. Необходимы дальнейшие исследования, чтобы охарактеризовать полную степень ингибирования цистатионин-бета-лиазы на рост микробов и грибов.