| Просмотр / редактирование человека | Просмотр / редактирование мыши |
Простагландин-эндопероксид-синтаза 2 (простагландин-G / H-синтаза и циклооксигеназа) (официальный символ HUGO - PTGS2 ; HGNC ID, HGNC: 9605 ), также известный как циклооксигеназа-2 или COX-2, представляет собой фермент, который у человека кодируется геном PTGS2 . У человека это одна из двух циклооксигеназ. Он участвует в превращении арахидоновой кислоты в простагландин H2, важный предшественник простациклина, который выражается в воспалении.
PTGS2 (COX-2), превращает арахидоновую кислоту (AA) в эндопероксид простагландина H2. PGHS являются мишенями для НПВП и ингибиторов PTGS2 (COX-2), называемых коксибами. PGHS-2 представляет собой гомодимер последовательности. Каждый мономер фермента имеет пероксидазу и активный сайт PTGS (COX) . Ферменты PTGS (COX) катализируют превращение арахидоновой кислоты в простагландины в два этапа. Сначала водород отводится от углерода 13 арахидоновой кислоты, а затем две молекулы кислорода добавляются PTGS2 (COX-2), давая PGG2. Во-вторых, PGG2 восстанавливается до PGH2 в активном центре пероксидазы. Синтезированный PGH2 превращается в простагландины (PGD2, PGE2, PGF 2α ), простациклин (PGI2) или тромбоксан A2. тканеспецифическими изомеразами. (Рисунок 2)
При метаболизме арахидоновой кислоты в основном до PGG2, COX-2 также превращает эту жирную кислоту в небольшие количества рацемической смеси 15-гидроксикозатетраеновой кислоты. (т.е. 15-HETE), состоящий из ~ 22% 15 (R) -HETE и ~ 78% 15 (S) -HETE стереоизомеров, а также небольшого количества 11 (R) - HETE. Два стереоизомера 15-HETE обладают внутренней биологической активностью, но, что, возможно, более важно, могут далее метаболизироваться до основного класса агентов, липоксинов. Кроме того, COX-2, обработанный аспирином, метаболизирует арахидоновую кислоту почти исключительно до 15 (R) -HETE, продукт которого может далее метаболизироваться до эпи липоксинов. Липоксины и эпилипоксины являются мощными противовоспалительными агентами и могут вносить вклад в общую активность двух ЦОГ, а также в аспирин.
COX-2 естественным образом ингибируется кальцитриолом (активная форма витамина D).
 арахидоновая кислота, связанная с PTGS2 (COX -2) фермент. полярные взаимодействия между (голубым) и Ser -530 и Tyr -385 остатками показаны желтыми пунктирными линиями. Субстрат стабилизирован гидрофобными взаимодействиями.
арахидоновая кислота, связанная с PTGS2 (COX -2) фермент. полярные взаимодействия между (голубым) и Ser -530 и Tyr -385 остатками показаны желтыми пунктирными линиями. Субстрат стабилизирован гидрофобными взаимодействиями. 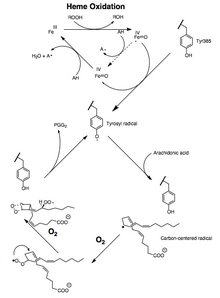 Механизм активации и катализа СОХ. гидропероксид окисляет гем до производного, которое либо восстанавливается на первой стадии цикла пероксидазы, либо окисляет тирозин 385 до. Затем тирозильный радикал может окислять 13-про (S) водород арахидоновой кислоты, чтобы инициировать цикл СОХ.
Механизм активации и катализа СОХ. гидропероксид окисляет гем до производного, которое либо восстанавливается на первой стадии цикла пероксидазы, либо окисляет тирозин 385 до. Затем тирозильный радикал может окислять 13-про (S) водород арахидоновой кислоты, чтобы инициировать цикл СОХ. Активность как пероксидазы, так и PTGS инактивируется во время катализа по механизму первого порядка процессы, что означает, что активность пероксидазы PGHS-2 или PTGS падает до нуля в течение 1-2 минут, даже в присутствии достаточного количества субстратов.
Превращение арахидоновой кислоты в PGG2 можно представить как серию радикальные реакции, аналогичные полиненасыщенной жирной кислоте автоокислению. 13-про (S) -водород отводится, и дикислород улавливает пентадиенил радикал на атоме углерода 11. 11-пероксильный радикал циклизуется у углерода 9, а углерод-центрированный радикал, образующийся в C-8, циклизуется на углероде 12, образуя эндопероксид. Образующийся аллильный радикал захватывается двуокисью углерода у углерода 15 с образованием 15- (S) -пероксильного радикала; затем этот радикал восстанавливается до PGG2. Это подтверждается следующими данными: 1) значительный кинетический изотопный эффект наблюдается для отвода 13-про (S) -водорода; 2) углеродно-центрированные радикалы захватываются во время катализа ; 3) небольшие количества продуктов окисления образуются из-за захвата кислорода промежуточным аллильным радикалом в положениях 13 и 15.
Другой механизм, в котором 13-про (S) -водород депротонирован и карбанион окислен до радикала, что теоретически возможно. Однако оксигенация 10,10-дифторарахидоновой кислоты до 11- (S) -гидроксиэйкоза-5,8,12,14-тетраеновой кислоты не согласуется с образованием промежуточного карбаниона, поскольку это приведет к удалению фторида с образованием сопряженного диена. Считается, что отсутствие эндопероксидсодержащих продуктов, полученных из 10,10-дифторарахидоновой кислоты, указывает на важность карбокатиона C-10 в синтезе PGG2. Однако катионный механизм требует, чтобы образование эндопероксида происходило до удаления 13-про (S) -водорода. Это не согласуется с результатами изотопных экспериментов по оксигенации арахидоновой кислоты.
 Как показано, разные лиганды связывают либо аллостерическую, либо каталитическую субъединицу. Аллостерическая субъединица связывает не-субстрат, активирующий ЖК (например, пальмитиновую кислоту). Аллостерическая субъединица со связанной жирной кислотой активирует каталитическую субъединицу, уменьшая Km для AA.
Как показано, разные лиганды связывают либо аллостерическую, либо каталитическую субъединицу. Аллостерическая субъединица связывает не-субстрат, активирующий ЖК (например, пальмитиновую кислоту). Аллостерическая субъединица со связанной жирной кислотой активирует каталитическую субъединицу, уменьшая Km для AA. PTGS2 (COX-2) существует в виде гомодимера, каждый мономер с молекулярной массой около 70 кДа. Третичная и четвертичная структуры ферментов PTGS1 (COX-1) и PTGS2 (COX-2) практически идентичны. Каждая субъединица имеет три различных структурных домена: короткий N-концевой домен эпидермального фактора роста (EGF ); α-спиральный мембранно-связывающий фрагмент; и С-концевой каталитический домен. Ферменты PTGS (COX, которые можно спутать с «цитохромоксидазой ») представляют собой монотопные мембранные белки; мембранно-связывающий домен состоит из серии амфипатических α-спиралей с несколькими гидрофобными аминокислотами, экспонированными на монослое мембраны. PTGS1 (COX-1) и PTGS2 (COX-2) представляют собой бифункциональные ферменты, которые проводят две последовательные химические реакции в пространственно различных, но механически связанных активных сайтах. Активные центры как циклооксигеназы, так и пероксидазы расположены в каталитическом домене, на который приходится примерно 80% белка. Каталитический домен гомологичен пероксидазам млекопитающих, таким как миелопероксидаза.
. Было обнаружено, что человеческий PTGS2 (COX-2) функционирует как конформационный гетеродимер, имеющий каталитический мономер (E-cat) и аллостерический мономер (Е-алло). Гем связывается только с сайтом пероксидазы E-cat, в то время как субстраты, а также некоторые ингибиторы (например, целекоксиб ) связывают COX сайт E-cat. E-cat регулируется E-allo в зависимости от того, какой лиганд связан с E-allo. Субстрат и не субстрат жирная кислота (FA) и некоторые ингибиторы PTGS (COX) (например, напроксен ) предпочтительно связываются с сайтом PTGS (COX) E -алло. Арахидоновая кислота может связываться с E-cat и E-allo, но сродство AA к E-allo в 25 раз больше, чем к Ecat. Пальмитиновая кислота, эффективный стимулятор, связывает только E-алло в сокристаллах пальмитиновой кислоты / мышиного PGHS-2. Не субстратные ЖК могут усиливать или ослаблять ингибиторы PTGS (COX) в зависимости от жирной кислоты и того, связывает ли ингибитор E-cat или E-allo. Исследования показывают, что концентрация и состав пула свободных жирных кислот в среде, в которой PGHS-2 функционирует в клетках, также называемый тонусом FA, является ключевым фактором, регулирующим активность PGHS-2 и его реакцию на PTGS (
 НПВП (неспецифический ингибитор PTGS2 (COX-2)) флурбипрофен (зеленый), связанный с PTGS2 (COX-2). Флурбипрофен стабилизируется за счет гидрофобных взаимодействий и полярных взаимодействий (Tyr -355 и Arg -120).
НПВП (неспецифический ингибитор PTGS2 (COX-2)) флурбипрофен (зеленый), связанный с PTGS2 (COX-2). Флурбипрофен стабилизируется за счет гидрофобных взаимодействий и полярных взаимодействий (Tyr -355 и Arg -120). PTGS2 (COX-2) не экспрессируется в нормальных условиях в большинстве клеток, но повышенные уровни обнаруживаются во время воспаления. PTGS1 (СОХ-1) конститутивно экспрессируется во многих тканях и является преобладающей формой в слизистой оболочке желудка и в почках. Ингибирование PTGS1 (COX-1) снижает цитопротектор PGE2 и PGI2 в желудке, что может способствовать язве желудка. Поскольку PTGS2 (COX-2) обычно экспрессируется только в клетках, где простагландины активированы (например, во время воспаления), предполагалось, что лекарственные препараты-кандидаты, которые избирательно ингибируют PTGS2 (COX-2), будут демонстрировать меньше побочные эффекты, но доказано, что они значительно увеличивают риск сердечно-сосудистых событий, таких как сердечный приступ и инсульт. Два разных механизма могут объяснить противоречивые эффекты. Аспирин в низких дозах защищает от сердечных приступов и инсультов, блокируя PTGS1 (COX-1) от образования простагландина, называемого тромбоксаном A2. Он склеивает тромбоциты и способствует свертыванию; подавление этого помогает предотвратить сердечные заболевания. С другой стороны, PTGS2 (COX-2) является более важным источником простагландинов, особенно простациклина, который содержится в слизистой оболочке кровеносных сосудов. Простациклин расслабляет или отслаивает тромбоциты, поэтому селективные ингибиторы ЦОГ-2 (коксибы) увеличивают риск сердечно-сосудистых событий из-за свертывания крови.
Нестероидные противовоспалительные препараты (НПВП) подавляют производство простагландина с помощью PTGS1 (COX-1) и PTGS2 (COX-2). НПВП, селективные в отношении ингибирования PTGS2 (ЦОГ-2), с меньшей вероятностью, чем традиционные препараты, вызывают желудочно-кишечные побочные эффекты, но могут вызывать сердечно-сосудистые события, такие как сердечная недостаточность, инфаркт миокарда и инсульт. Исследования фармакологии и генетики, генетических манипуляций грызунов, а также других животных моделей и рандомизированные испытания показывают, что это происходит из-за подавления PTGS2 (COX-2) -зависимые кардиозащитные простагландины, в частности простациклин.
Экспрессия PTGS2 (COX-2) активируется при многих раковых заболеваниях. Сверхэкспрессия PTGS2 (COX-2) наряду с повышенным ангиогенезом и экспрессией SLC2A1 (GLUT-1) в значительной степени связана с карциномами желчного пузыря. Кроме того, продукт PTGS2 (COX-2), PGH 2 превращается простагландин E2-синтазой в PGE 2, что, в свою очередь, может стимулировать прогрессирование рака. Следовательно, ингибирование PTGS2 (COX-2) может иметь преимущество при профилактике и лечении этих типов рака.
Экспрессия COX-2 была обнаружена в идиопатических эпиретинальных мембранах человека. Блокирование циклооксигеназ лорноксикамом в острой стадии воспаления снижает частоту образования мембран на 43% в модели dispase для PVR и на 31% в конканавалин один. Лорноксикам не только нормализовал экспрессию циклооксигеназ в обеих моделях PVR, но также нейтрализовал изменения сетчатки и толщины сосудистой оболочки, вызванные инъекцией про -воспалительные агенты. Эти факты подчеркивают важность циклооксигеназ и простагландинов в развитии PVR.
Активная регуляция гена PTGS2 также связана с множественными стадиями репродукции человека. Наличие гена обнаруживается в хорионической пластинке, в эпителии амниона, синцитиотрофобластах, ворсинчатых фибробластах, хорионических трофобластах, амниотические трофобласты, а также базальная пластинка плаценты, в децидуальных клетках и вневорсинчатых цитотрофобластах. Во время процесса хориоамнионита / децидуита активация PTGS2 в амнионе и хориодецидуите является одним из трех ограниченных эффектов воспаления в матке. Повышенная экспрессия гена PTGS2 в мембранах плода связана с наличием воспаления, вызывающим экспрессию гена простагландина матки и иммунолокализацию белков пути простагландина в клетках хорионического трофобласта и прилегающей децидуальной оболочке, или choriodecidua. PTGS2 связан с воспалительной системой и наблюдается в воспалительных лейкоцитах. Было отмечено, что существует положительная корреляция с экспрессией PTGS2 в амнионе во время спонтанных родов, и было обнаружено, что экспрессия увеличивается с гестационным возрастом после наличия родов, при этом изменений в амнионе и хориодецидуальной оболочке во время преждевременных или срочных родов не наблюдается. Кроме того, окситоцин стимулирует экспрессию PTGS2 в клетках миометрия.
Было показано, что носители мутантного аллеля PTGS2 5939C среди китайской популяции хань имеют более высокий риск рака желудка. Кроме того, была обнаружена связь между инфекцией Helicobacter pylori и наличием аллеля 5939C.
Было показано, что PTGS2 взаимодействует с кавеолином 1.
PTGS2 (COX-2) был обнаружен в 1991 г. лабораторией Дэниела Симмонса в Университете Бригама Янга.