| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC Оксалонитрил | |||
| Систематическое название IUPAC Этандинитрил | |||
| Другие названия Цианоген. Бис (нитридокарбон) (C — C). Дициан. Нитрид углерода. Динитрил щавелевой кислоты. Дицианоген. Нитрилоацетонитрил | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 1732464 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.006.643 | ||
| Номер EC |
| ||
| Справочник Гмелина | 1090 | ||
| MeSH | цианоген | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| номер ООН | 1026 | ||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | (CN) 2 | ||
| Молярная масса | 52,034 г / моль | ||
| Внешний вид | Бесцветный газ | ||
| Запах | резкий, миндалеподобный | ||
| Плотность | 950 мг / мл (при -21 ° C) | ||
| Точка плавления | -28 ° C (-18 ° F; 245 K) | ||
| Температура кипения | -21,1 ° C; -6,1 ° F; 252,0 K | ||
| Растворимость в воде | 45 г / 100 мл (при 20 ° C) | ||
| Растворимость | растворим в этаноле, этиловом эфире | ||
| Давление пара | 5,1 атм (21 ° C) | ||
| закон Генри. постоянная (kH) | 1,9 мкмоль Па кг | ||
| Магнитная восприимчивость (χ) | -21,6 · 10 см / моль | ||
| Преломляющая индекс (nD) | 1,327 (18 ° C) | ||
| Термохимия | |||
| Стандартная молярная. энтропия (S 298) | 241,57 ДжК моль | ||
| Стандартная энтальпия образования. (ΔfH298) | 309,07 кДж моль | ||
| Стандартная энтальпия. горения (ΔcH298) | -1,0978– -1,0942 МДж моль | ||
| Опасности | |||
| Основные опасности | формы цианид в организме; легковоспламеняющийся | ||
| Паспорт безопасности | inchem.org | ||
| Пиктограммы GHS |    | ||
| Сигнальное слово GHS | Опасно | ||
| Предупреждения об опасности GHS | H220, H331, H400, H410 | ||
| Меры предосторожности GHS | P210, P261, P271, P273, P304 + 340, P311, P321, P377, P381, P391, P403, P403 + 233, P405, P501 | ||
| NFPA 704 (огненный алмаз) |  4 4 2 4 4 2 | ||
| Пределы взрываемости | 6,6–32% | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимый) | нет | ||
| REL (рекомендуется) | TWA 10 ppm (20 мг / м) | ||
| IDLH (Непосредственная опасность) | ND | ||
| Родственные соединения | |||
| Родственные алканнитрилы | |||
| Родственный N730 Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в информационном окне | |||
Цианоген - это химическое соединение с формулой (C N )2. Это бесцветный, токсичный газ с резким запахом. Молекула представляет собой псевдогалоген. Молекулы цианогена состоят из двух групп CN - аналогично двухатомным молекулам галогена, таким как Cl 2, но гораздо менее окисляющим. Две циано группы связаны вместе по своим углеродным атомам: N≡C-C≡N, хотя были обнаружены другие изомеры. Это название также используется для радикала CN и, следовательно, используется для таких соединений, как цианогенбромид (NCBr).
Цианоген - это ангидрид из оксамид :
, хотя оксамид получают из цианогена путем гидролиза:
Цианоген обычно получают из цианидных соединений. Один лабораторный метод включает термическое разложение цианида ртути :
В качестве альтернативы можно комбинировать растворы солей меди (II) (таких как сульфат меди (II) ) с цианидами; Образуется нестабильный цианид меди (II), который быстро разлагается на цианид меди (I) и цианоген.
Промышленно он создается путем окисления цианистого водорода, обычно с использованием хлора вместо активированного диоксид кремния катализатор или диоксид азота над солью меди. Он также образуется, когда азот и ацетилен вступают в реакцию с помощью электрической искры или разряда.
Цианоген - это NCCN. Есть менее стабильные изомеры, в которых порядок атомов отличается. Изоцианоген (или цианоизоцианоген) - это NCNC, диизоцианоген - это CNNC, а диазодикарбон - это CCNN.
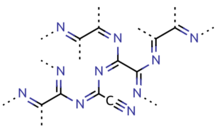
Парацианоген представляет собой полимер цианогена. Лучше всего его можно приготовить путем нагревания цианида ртути. Его также можно получить нагреванием цианида серебра, цианата серебра, иодида цианогена или иодида циануровой кислоты. Его также можно получить путем полимеризации цианогена при температуре от 300 до 500 ° C (от 572 до 932 ° F) в присутствии следов примесей. Парацианоген также можно превратить обратно в цианоген при нагревании до 800 ° C (1470 ° F). Основываясь на экспериментальных данных, структура этого полимерного материала считается довольно неправильной, с большинством атомов углерода sp-типа и локализованными доменами π-конъюгации.
Цианоген был впервые синтезирован в 1815 г. Жозефом Луи Гей-Люссаком, который определил его эмпирическую формулу и назвал ее. Гей-Люссак придумал слово «цианоген» от греческих слов κυανός (кианос, синий) и γεννάω (gennao, я создаю), потому что цианид был впервые выделен шведским химиком Карлом Вильгельмом Шееле из пигмента « берлинская лазурь ". К 1850-м годам фотографы использовали цианоген мыло для удаления серебряных пятен с рук. Он приобрел важное значение с развитием индустрии удобрений в конце 19 века и остается важным промежуточным звеном в производстве многих удобрений. Он также используется в качестве стабилизатора при производстве нитроцеллюлозы.
. В 1910 году спектроскопический анализ кометы Галлея обнаружил цианоген в хвосте кометы, что вызвало опасения общественности. что Земля будет отравлена, когда пройдет через хвост. Из-за чрезвычайно диффузной природы хвоста, когда планета прошла сквозь него, не было никакого эффекта.
Как и другие цианиды, цианоген очень токсичен, так как он легко восстанавливается до цианида, который отравляет комплекс цитохром с-оксидазы, прерывая, таким образом, митохондриальную цепь переноса электрона. Цианоген вызывает раздражение глаз и дыхательной системы. Вдыхание может привести к головной боли, головокружению, учащенному пульсу, тошноте, рвоте, потере сознания, судорогам и смерти, в зависимости от воздействия. Смертельная доза при вдыхании обычно составляет от 100 до 150 миллиграммов (от 1,5 до 2,3 гран ). Вдыхание 900 ppm в течение 10 минут считается смертельным.
Цианоген производит второе по величине естественное пламя (после субнитрида углерода ) с температурой более 4525 ° C ( 8,177 ° F), когда он горит в кислороде.
В 5-м эпизоде 13-го сезона Доктор Кто Мозг Морбиуса доктор синтезирует цианоген, используя цианистый водород в качестве исходного материала, и выпускает его через трубу, чтобы помешать Солону провести операцию на мозге тела Морбиуса, однако он завершает ее, но вскоре после этого умирает от отравления цианогеном.
В Драгнете (1987) Пятница (Дэн Экройд) и Стрибек (Том Хэнкс) выслеживали злодея, укравшего «псевдогаллогенное соединение Цианаген». http://www.subzin.com/quotes/M100518da4/Dragnet/The+trichlornitromethane+and+the+pseudo-halogenic+compound+cyanogen.
| Викискладе есть материалы, связанные с цианогеном. |
| Викисточник содержит текст Британской энциклопедии 1911 года статьи Цианоген. |