 . Безводный . Безводный | |
 . Безводный . Безводный | |
 . Дигидрат . Дигидрат | |
| Имена | |
|---|---|
| Другие названия Хлорид меди | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| Ссылка Beilstein | 8128168 |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.028.373 |
| Номер EC |
|
| Ссылка Gmelin | 9300 |
| PubChem CID | |
| номер RTECS |
|
| UNII |
|
| номер ООН | 2802 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | CuCl 2 |
| Молярный масса | 134,45 г / моль (безводный). 170,48 г / моль (дигидрат) |
| Внешний вид | желто-коричневое твердое вещество (безводное). сине-зеленое твердое вещество (дигидрат) |
| Запах | без запаха |
| Плотность | 3,386 г / см (безводный). 2,51 г / см (дигидрат) |
| Температура плавления | 498 ° C (928 ° F; 771 K) (безводный). 100 ° C (дегидратация дигидрата) |
| Температура кипения | 993 ° C (1819 ° F; 1266 K) (безводный, разлагается) |
| Растворимость в воде | 70,6 г / 100 мл (0 ° C). 75,7 г / 100 мл (25 ° C). 107,9 г / 100 мл (100 ° C) |
| Растворимость | метанол:. 68 г / 100 мл (15 ° C) . этанол:. 53 г / 100 мл (15 ° C). растворим в ацетоне |
| Магнитная восприимчивость (χ) | + 1080 · 10 см / моль |
| Структура | |
| Кристаллическая структура | искаженная CdI 2 структура |
| Координационная геометрия | Октаэдрическая |
| Опасности | |
| Паспорт безопасности | Fisher Scientific |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасно |
| Предупреждения об опасности GHS | H301, H302, H312, H315, H318, H319, H335, H400, H410, H411 |
| Меры предосторожности GHS | P261, P264, P270, P271, P273, P280, P301 + 310, P301 + 312, P302 + 352, P304 + 340, P305 + 351 + 338, P310, P312, P321, P322, P330, P332 + 313, P337 + 313, P362, P363, P391, P403 + 233, P405, P501 |
| NFPA 704 (огненный алмаз) |  0 2 1 0 2 1 |
| Температура вспышки | Нет -воспламеняющийся |
| NIOSH (пределы воздействия на здоровье США): | |
| PEL (допустимо) | TWA 1 мг / м (как Cu) |
| REL (рекомендуется) | TWA 1 мг / м (в виде Cu) |
| IDLH (Непосредственная опасность) | TWA 100 мг / м (в виде Cu) |
| Родственные соединения | |
| Другие анионы | Фторид меди (II). Бромид меди (II) |
| Прочие катионы | Хлорид меди (I). Хлорид серебра. Хлорид золота (III) |
| Если не указано иное отмечено, что данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
Хлорид меди (II) - это химическое соединение с химической формулой CuCl 2. Это светло-коричневое твердое вещество, которое медленно поглощает влагу с образованием сине-зеленого дигидрата.
Безводная и дигидратная формы встречаются в природе в виде очень редких минералов толбахит и эриохальцит. соответственно.
Безводный CuCl 2 имеет искаженную структуру иодида кадмия. В этом мотиве медные центры имеют октаэдрические формы. Большинство соединений меди (II) демонстрируют искажения идеализированной октаэдрической геометрии из-за эффекта Яна-Теллера, который в данном случае описывает локализацию одного d-электрона на молекулярной орбитали, т.е. сильно разрыхлитель по отношению к паре хлоридных лигандов. В CuCl 2 · 2H 2 O медь снова принимает сильно искаженную октаэдрическую геометрию, при этом центры Cu (II) окружены двумя водными лигандами и четырьмя хлоридными лигандами, которые соединяют асимметрично с другими центрами Cu.
Хлорид меди (II) является парамагнитным. Исторический интерес представляет CuCl 2 · 2H 2 O был использован в первых измерениях электронного парамагнитного резонанса, выполненных Евгением Завойским в 1944 году.
Водный раствор, приготовленный из хлорида меди (II), содержит ряд комплексов меди (II) в зависимости от концентрации, температуры и наличия дополнительного хлорида ионы. Эти частицы включают синий цвет [Cu (H 2O)6]] и желтый или красный цвет галогенидных комплексов формулы [CuCl 2 + x ].
осадки гидроксида меди (II) при обработке растворов хлорида меди (II) основанием:
 Хлорид меди (II) дигидрат кристалл
Хлорид меди (II) дигидрат кристалл Частичный гидролиз дает тригидроксид хлорида дигидрата, Cu 2 (OH) 3 Cl, популярный фунгицид.
Хлорид меди (II) является мягким окислителем. Он разлагается до хлорида меди (I) и газообразного хлора около 1000 ° C:
Хлорид меди (II) (CuCl 2) реагирует с несколькими металлами с образованием металлической меди или хлорида меди (I) (CuCl) с окисление другого металла. Чтобы преобразовать хлорид меди (II) в хлорид меди (I), может быть удобно восстановить водный раствор с помощью диоксида серы в качестве восстановителя:
CuCl 2 реагируют с HCl или другими источниками хлорида с образованием комплексных ионов: красный CuCl 3 (на самом деле это димер Cu 2Cl6, пара тетраэдров с общим ребром), а также зеленый или желтый CuCl 4.
Некоторые из этих комплексов можно кристаллизовать из водного раствора, и они принимают широкий спектр структур.
Хлорид меди (II) также образует различные координационные комплексы с лигандами, такими как аммиак, пиридин и оксид трифенилфосфина :
Однако «мягкие» лиганды, такие как фосфины (например, трифенилфосфин ), йодид и цианид, а также некоторые третичные амины вызывают восстановление с образованием комплексов меди (I).
Хлорид меди (II) получают в промышленных масштабах путем хлорирования меди. Медь при красном нагревании (300-400 ° C) непосредственно соединяется с газообразным хлором, давая (расплавленный) хлорид меди (II). Реакция очень экзотермическая.
Это также коммерчески практично сочетать оксид меди (II) с избытком хлорида аммония при аналогичных температурах с получением c хлорид, аммиак и вода:
Хотя сама медь не может окисляться соляной кислотой, могут быть медьсодержащие основания, такие как гидроксид, оксид или карбонат меди (II).
После приготовления раствор CuCl 2 может быть очищен кристаллизацией. При стандартном методе раствор, смешанный с горячей разбавленной соляной кислотой, вызывает образование кристаллов путем охлаждения в бане с хлоридом кальция (CaCl 2) - лед.
Там являются косвенными и редко используемыми средствами использования ионов меди в растворе для образования хлорида меди (II). Электролиз водного раствора хлорида натрия с помощью медных электродов дает (среди прочего) сине-зеленую пену, которую можно собрать и преобразовать в гидрат. Обычно этого не делают из-за выделения токсичного газообразного хлора и преобладания более общего хлорщелочного процесса, при электролизе металлическая медь преобразуется в ионы меди в растворе, образующем соединение. Действительно, любой раствор ионов меди можно смешать с соляной кислотой и превратить в хлорид меди путем удаления любых других ионов.
Хлорид меди (II) встречается в природе как очень редкий безводный минерал толбахит и дигидрат эриохальцита. Оба обнаружены около фумаролы. Более распространены смешанные оксигидроксид-хлориды, такие как атакамит Cu2(OH) 3 Cl, возникающие среди зон окисления Cu рудных пластов в засушливом климате (также известные из некоторых измененных шлаков).
Основным промышленным применением хлорида меди (II) является сокатализатор с хлорид палладия (II) в процессе Ваккера. В этом процессе этен (этилен) превращается в этаналь (ацетальдегид) с использованием воды и воздуха. В ходе реакции PdCl 2 восстанавливается до Pd, а CuCl 2 служит для его повторного окисления до PdCl 2. Затем воздух может окислить образовавшийся CuCl обратно до CuCl 2, завершая цикл.
Общий процесс:
Хлорид меди (II) используется в качестве катализатора в различные процессы, в которых получают хлор путем оксихлорирования. Процесс Дикона происходит при температуре примерно от 400 до 450 ° C в присутствии хлорида меди:
Хлорид меди (II) катализирует хлорирование при производстве винилхлорида и дихлорэтана.
Хлорид меди (II) используется в цикле медь – хлор, в котором он расщепляет пар на кислородсодержащее соединение меди и хлористый водород, а затем восстанавливается в цикле из электролиза хлорида меди (I).
Хлорид меди (II) имеет несколько узкоспециализированных применений в синтезе органических соединений. Он вызывает хлорирование ароматических углеводородов - это часто выполняется в присутствии оксида алюминия. Он способен хлорировать альфа-положение карбонильных соединений:

Эту реакцию проводят в полярном растворителе, таком как диметилформамид (ДМФ), часто в присутствии хлорид лития, ускоряющий реакцию.
CuCl 2 в присутствии кислорода может также окислять фенолы. Основной продукт может быть направлен на получение либо хинона, либо связанного продукта окислительной димеризации. Последний процесс обеспечивает путь с высоким выходом к 1,1-бинафтолу :

Такие соединения являются промежуточными продуктами в синтезе BINAP и его производных
хлорида меди (II) дигидрат способствует гидролизу ацетонидов, то есть для снятия защиты с регенерацией диолов или аминоспиртов, как в этом примере (где TBDPS = трет-бутилдифенилсилил ):
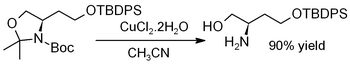
CuCl 2 также катализирует свободный радикал добавление сульфонилхлоридов к алкенам ; затем альфа-хлорсульфон может подвергаться элиминированию основанием с образованием винил сульфона.
Хлорид меди (II) также используется в пиротехнике в качестве сине-зеленого красителя. В испытании пламенем, хлориды меди, как и все соединения меди, излучают зелено-синий цвет.
В картах индикаторов влажности (HIC) от не содержащего кобальта коричневого до лазурного цвета (на основе хлорида меди (II)) HIC могут быть найдено на рынке. В 1998 году Европейское Сообщество (ЕС) классифицировало предметы содержащий хлорид кобальта (II) от 0,01 до 1% по массе в виде T (токсичный), с соответствующей R-фразой R49 (может вызвать рак при вдыхании). Как следствие, были разработаны новые не содержащие кобальта карты индикаторов влажности, содержащие медь.
Хлорид меди (II) может быть токсичным. Агентство по охране окружающей среды США.
| На Викискладе есть материалы, связанные с хлоридом меди (II). |