| Крымско-Конго геморрагическая лихорадка | |
|---|---|
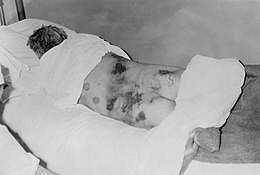 | |
| Мужчина с диагнозом Крымско-Конго геморрагическая лихорадка, 1969 | |
| Специальность | Инфекционное заболевание |
| Симптомы | Лихорадка, боли в мышцах, головная боль, рвота, диарея, кровотечение в кожу |
| Осложнения | Печеночная недостаточность |
| Обычное начало | Быстрое |
| Продолжительность | Две недели |
| Метод диагностики | Обнаружение антител, вирус РНК или сам вирус |
| Дифференциальный диагноз | Лихорадка Денге, Ку-лихорадка, Болезнь, вызванная вирусом Эбола |
| Лечение | Поддерживающая терапия, рибавирин |
| Прогноз | Риск смерти ~ 25% |
Крымско-Конго геморрагическая лихорадка (CCHF ) является вирусным болезнь. Симптомы CCHF могут включать лихорадку, мышечные боли, головную боль, рвоту, диарею и кожное кровотечение <241.>. Симптомы появляются менее чем через две недели после заражения. Осложнения могут включать печеночную недостаточность. У тех, кто выжил, выздоровление обычно происходит примерно через две недели после начала заболевания.
Вирус CCHF обычно распространяется через укусы клещей или контакт с домашним скотом, переносящим болезнь. Группы с высоким риском заражения - это фермеры и те, кто работает на бойнях. Вирус также может передаваться между людьми через биологические жидкости. Диагноз ставится путем обнаружения антител, РНК вируса или самого вируса. Это разновидность вирусной геморрагической лихорадки.
. Профилактика заключается в том, чтобы избегать укусов клещей. Вакцина коммерчески недоступна. Обычно лечение проводится поддерживающей терапией. Также может помочь лекарство рибавирин.
Встречается в Африке, Балканах, на Ближнем Востоке и в Азии. Часто встречается в вспышках. В 2013 г. Иран, Россия, Турция и Узбекистан задокументировали более пятидесяти случаев. Риск смерти среди пострадавших составляет от 10 до 40%. Впервые он был обнаружен в 1940-х годах.
Заболевание человека представляет собой тяжелую форму геморрагической лихорадки. Как правило, через 1–3 дня инкубационного периода после укуса клеща или через 5–6 дней после контакта с инфицированной кровью или тканями появляются симптомы, похожие на грипп, которые могут исчезнуть через один неделя. До 75% случаев признаки кровотечения могут появиться в течение 3-5 дней от начала заболевания в случае плохого сдерживания первых симптомов: нестабильность настроения, возбуждение, спутанность сознания и горло петехии ; и вскоре после носового кровотечения, рвоты и черного стула. печень становится опухшей и болезненной. Может возникнуть диссеминированная внутрисосудистая коагуляция, а также острая почечная недостаточность, шок, а иногда острый респираторный дистресс-синдром. Обычно люди начинают выздоравливать через 9–10 дней после появления первых симптомов. До 30% инфицированных умирают к концу второй недели болезни.
| Ортонаировирус Крымско-Конго геморрагической лихорадки | |
|---|---|
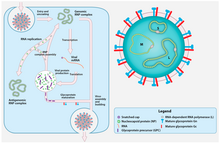 | |
| Вирус Крымско-Конго геморрагической лихорадки (CCHFV) вирион и цикл репликации. | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Орторнавиры |
| Тип: | Негарнавирикота |
| Класс: | Ellioviricetes |
| Отряд: | Bunyavirales |
| Семейство: | Nairoviridae |
| Род: | Orthonairovirus |
| Вид: | Ортонайровирус крымско-конголезской лихорадки |
Крым-Конго Ортонаировирус геморрагической лихорадки (CCHFV) является представителем рода Orthonairovirus, семейства Nairoviridae из РНК-вирусов.
Вирионы имеют размер 80–120 нанометров (нм) в диаметре и плеоморфны. В вирионе нет рибосом-хозяев. Каждый вирион содержит три копии генома. Оболочка является однослойной и сформирована из липидного бислоя толщиной 5 нм. Нет выступов. Белки оболочки образуют небольшие выступы длиной ~ 5–10 нм. Нуклеокапсиды нитевидные, круглые, длиной 200–3000 нм. Вирус может проникнуть в клетку, используя белок клеточной поверхности нуклеолин.
Геном кольцевой, отрицательно-смысловой РНК из трех частей - маленькая (S), средняя (M) и большой (L). Сегмент L имеет длину 11–14,4 килобаз, а сегменты M и S - 4,4–6,3 и 1,7–2,1 килобаз соответственно. Сегмент L кодирует РНК-полимеразу, сегмент M кодирует гликопротеины оболочки (Gc и Gn), а сегмент S кодирует белок нуклеокапсида. Частота мутаций для трех частей генома была оценена как: 1,09 × 10, 1,52 × 10 и 0,58 × 10 замен / сайт / год для сегментов S, M и L. соответственно.
CCHFV является наиболее генетически разнообразным из арбовирусов : его нуклеотидные последовательности часто различаются между разными штаммами, от 20% вариабельности для вирусного S-сегмента до 31% для M-сегмента. Вирусы с разными последовательностями можно найти в одном географическом районе; близкородственные вирусы были изолированы из широко разделенных регионов, что позволяет предположить, что распространение вируса произошло, возможно, от клещей, переносимых перелетными птицами или в результате международной торговли домашним скотом. Повторная сортировка сегментов генома во время коинфекции клещей или позвоночных, по-видимому, сыграла роль в формировании разнообразия этого вируса.
На основании данных о последовательностях было распознано семь генотипов CCHFV: Африка 1 (Сенегал ), Африка 2 (Демократическая Республика Конго и Южная Африка), Африка 3 (южная и западная Африка), Европа 1 (Албания, Болгария, Косово, Россия и Турция ), Европа 2 (Греция ), Азия 1 (Ближний Восток, Иран и Пакистан ) и Азия 2 (Китай, Казахстан, Таджикистан и Узбекистан ).
 Клещ Hyalomma
Клещ Hyalomma Клещи одновременно являются «резервуаром окружающей среды» и переносчиком вируса, переносящего его от диких животных к домашним животным и Виды клещей, идентифицированных как инфицированные этим вирусом, включают Argas reflexus, Hyalomma anatolicum, Hyalomma detritum, Hyalomma marginatum mar ginatum и Rhipicephalus sanguineus. Было обнаружено, что не менее 31 вида клещей из родов Haemaphysalis и Hyalomma на юго-востоке Ирана являются переносчиками вируса.
Дикие животные и мелкие млекопитающие, особенно европейский заяц, Среднеафриканские ежи и многокамерные крысы являются «амплифицирующими хозяевами» вируса. Птицы, как правило, устойчивы к ККГН, за исключением страусов. Домашние животные, такие как овцы, козы и крупный рогатый скот, могут вырабатывать высокие титры вируса в крови, но, как правило, не заболевают.
«Спорадическая инфекция» человека обычно вызывается укусом клеща Hyalomma. Животные могут передавать вирус людям, но обычно это является частью кластера болезней. Когда возникают группы болезней, это обычно происходит после того, как люди лечат, разделывают или съедают зараженный скот, особенно жвачных и страусов. Вспышки произошли на скотобойнях и в других местах, где рабочие подвергались воздействию инфицированной крови человека или животных и фомитов. Люди могут заразить людей, и вспышки также происходят в медицинских учреждениях через зараженную кровь и нечистую медицинскую инструменты.
Там, где инфекция клещами млекопитающих является обычным явлением, сельскохозяйственные правила требуют снимать клещи с сельскохозяйственных животных перед транспортировкой или доставкой на убой. Рекомендуются индивидуальные меры по предотвращению клещей, такие как использование репеллентов от насекомых, соответствующая одежда и осмотр тела на предмет прилипших клещей.
Когда лихорадка пациентам с признаками кровотечения требуется реанимация или интенсивная терапия, изоляция веществ в организме следует соблюдать меры предосторожности.
С 1970-х годов во всем мире было проведено несколько испытаний вакцин против CCHF были прекращены из-за высокой токсичности.
По состоянию на март 2011 г. единственной доступной и, вероятно, в некоторой степени эффективной вакциной CCHF был препарат инактивированного антигена, который затем использовался в Болгарии. В научной литературе не существует публикаций, связанных с этой вакциной, что турецкий вирусолог назвал подозрительным, поскольку для ее производства использовались устаревшие технологии и мозг мыши. В настоящее время разрабатываются новые вакцины, но спорадический характер заболевания даже в эндемичных странах предполагает, что проведение крупных испытаний эффективности вакцины будет затруднено. Поиск добровольцев может оказаться сложной задачей, учитывая растущие настроения против вакцинации и сопротивление населения вакцинации против заразных болезней. Необходимо тщательно определить количество людей, которые будут вакцинированы, и продолжительность наблюдения за ними для подтверждения защиты. С другой стороны, многие ученые, по-видимому, считают, что лечение CCHF с помощью рибавирина более практично, чем профилактика, но некоторые недавно проведенные клинические испытания, похоже, опровергают предположения об эффективности препарата. В 2011 году Турецкая исследовательская группа под руководством Университета Эрджиес успешно разработала первую нетоксичную профилактическую вакцину, которая прошла клинические испытания. По состоянию на 2012 г. вакцина ожидала утверждения FDA США.
После эпидемии Эболы ВОЗ приступила к реализации «Программы готовности к исследованиям и разработкам» по новым патогенам с эпидемическим потенциалом, против которых нет лечения. CCHF был главным приоритетом в первоначальном списке с декабря 2015 года и вторым по состоянию на январь 2017 года.
Лечение в основном поддерживающее. Рибавирин эффективен in vitro и использовался перорально во время вспышек заболеваний, но нет никаких доказательств, подтверждающих его использование.
По состоянию на 2011 год использование препаратов иммуноглобулина остается недоказанным, а разработка антител, которая вселила надежды на терапию моноклональными антителами, все еще находится в зачаточном состоянии.
В вооруженных силах США имеются специальные запасы рибавирина для защищать персонал, направленный в Афганистан и Ирак от CCHF.
CCHD чаще всего возникает среди сельскохозяйственных рабочих после укуса инфицированного клеща, и в меньшей степени среди рабочих бойни, контактировавших с кровью и тканями инфицированного домашнего скота, и медицинского персонала в результате контакта с биологическими жидкостями инфицированных людей.
По состоянию на 2013 год северная граница CCHF была 50 градусов северной широты, к северу от которой отметки Hyalomma не были nd. Согласно карте ВОЗ от 2008 года, клещи Hyalomma встречались к югу от этой широты на всем евразийском континенте и в Африке, за исключением островов Шри-Ланки, Индонезии и Японии. Серологические или вирусологические доказательства CCHF были широко распространены в Азии, Восточной Европе, на Ближнем Востоке (кроме Израиля, Ливана и Иордании), в Центральной Африке, Западной Африке, Южной Африке и на Мадагаскаре.
В 2008 году было зарегистрировано более 50 случаев. в год были зарегистрированы только из 4 стран: Турции, Ирана, России и Узбекистана. 5-49 случаев в год были зарегистрированы в Южной Африке, Центральной Азии, включая Пакистан и Афганистан (но не считая Туркменистана), на Ближнем Востоке только в ОАЭ и балканских странах, ограниченных Румынией, Болгарией, Сербией, Черногорией и Косово-Албанией.
На карте 2014 года, составленной CDC, эндемичные районы (красным цветом) в Африке и на Ближнем Востоке практически не изменились, но разные для Балкан, включая все страны бывшей Югославии, а также Грецию, но уже не Румынию. В северо-западных регионах Индии, Раджастане и Гуджарате, были зарегистрированы первые случаи заболевания.
С 1995 по 2013 год в Республике Косово было зарегистрировано 228 случаев CCHF с уровнем летальности 25,5. %.
В период с 2002 по 2008 год Министерство здравоохранения Турции сообщило о 3 128 случаях CCHF с 5% смертностью. В июле 2005 года власти сообщили о 41 случае CCHF в провинции Йозгат центральной Турции, один из которых погиб. По состоянию на август 2008 г., всего за год в различных городах Турции было зарегистрировано 50 смертей из-за CCHF.
В сентябре 2010 г. была зарегистрирована вспышка заболевания в Хайбер-Пахтунхва Пакистана провинция. Плохая диагностика и ведение записей привели к неопределенности масштабов вспышки, хотя в некоторых отчетах указывалось более 100 случаев с летальным исходом выше 10%.
В январе 2011 г. были зарегистрированы первые случаи заболевания людей CCHF в Индия была зарегистрирована в Сананд, Гуджарат, Индия, с 4 зарегистрированными смертельными случаями, в том числе индексный пациент, лечащий врач и медсестра.
По состоянию на май 2012 года 71 Сообщалось, что люди заразились этой болезнью в Иране, в результате чего погибло 8 человек.
В октябре 2012 года британский мужчина умер от болезни в Королевской свободной больнице в Лондоне. Ранее он был госпитализирован в больницу общего профиля Гартнавел в Глазго после возвращения рейсом из Кабула в Афганистан.
В июле 2013 года семь человек погибли из-за CCHF в деревне Карияна в Бабра талука, район Амрели, Гуджарат, Индия.
В августе 2013 года фермер из Агаго, Уганда лечилась в больнице Калонго по поводу подтвержденной инфекции CCHF. Предполагалось, что смерть трех других людей в северном регионе была вызвана вирусом. В тот же день в госпиталь Мулаго был госпитализирован другой неродственный пациент с CCHF. Министерство здравоохранения 19 объявило, что вспышка находится под контролем, но вторая пациентка, 27-летняя женщина из Нансана, умерла 21-го. Считается, что она заразилась вирусом от своего мужа, который вернулся в Кампалу после лечения от CCHF в Джубе, Южный Судан.
. В июне 2014 года случаи заболевания были диагностированы в Казахстане. Десять человек, включая бригаду скорой помощи, были госпитализированы в больницу на юге Казахстана с подозрением на ЗДН. В июле 2014 года в медицинском комплексе Хаятабад (HMC), Пакистан, был обнаружен 8-й человек, инфицированный CCHF. Восемь пациентов, в том числе медсестра и 6 граждан Афганистана, умерли в период с апреля по июль 2014 года.
По состоянию на 2015 год, спорадические подтвержденные случаи были зарегистрированы в Бхудж, Амрели, Сананд, Идар и Ваднагар в Гуджарате, Индия. В ноябре 2014 года у врача и рабочего в северном Гуджарате результат теста на болезнь оказался положительным. В последующие недели еще три человека умерли от CCHF. В марте 2015 года в Гуджарате от CCHF умер еще один человек. По состоянию на 2015 год среди домашнего скота CCHF был признан «широко распространенным» в Индии, всего через 4 года после того, как был диагностирован первый случай заболевания человека.
В августе 2016 года первый локальный случай CCHF в Западной Европе произошел в Западная Испания. 62-летний мужчина, укушенный клещом в Испании, скончался 25 августа, заразив медсестру. Укус клеща произошел в провинции Авила, в 300 км от провинции Касерес, где вирусная РНК CCHF от клещей была усилена в 2010 году. По состоянию на июль 2017 года было неясно, что специфическая экология привела к случаям заражения в Испании.
В августе 2016 года ряд пакистанских источников новостей выразили обеспокоенность по поводу этого заболевания. В период с января по октябрь 2016 г. в Пакистане зарегистрированы вспышки CCHF с наибольшим числом случаев заболевания и смертей в августе 2016 г., незадолго до праздника Курбан-байрам (проходившего 13–15 сентября 2016 г.). Было высказано предположение, что фестиваль может сыграть важную роль, поскольку люди могут контактировать с домашними или импортированными животными, потенциально инфицированными вирусом CCHF. Национальный институт здравоохранения Пакистана показал, что корреляции нет, и что случаи CCHF совпали с пиком распространения клещей в течение предшествующих 8–10 лет.
5 февраля 2020 г. в центральном регионе Мали произошла вспышка. Зараженные - из регионов Дуэнца и Мопти. На данный момент умерло 7 человек.
Вирус, возможно, возник около 1500–1100 гг. До н.э. Считается, что изменение климата и методов ведения сельского хозяйства примерно в это время могло быть причиной его эволюции.
В XII веке случай геморрагической болезни, зарегистрированный на территории Таджикистана, мог быть причиной первый известный случай крымско-конголезской геморрагической лихорадки. Во время Крымской войны эта болезнь была известна как «Крымская лихорадка» и заразилась многими, в том числе Флоренс Найтингейл.
В 1944 году советские ученые впервые идентифицировали болезнь, которую они назвали Крымской геморрагической лихорадкой, в Крым. Они установили его вирусную этиологию, но в то время не смогли выделить возбудителя.
В феврале 1967 года вирусологи Джон П. Вудал, Дэвид Симпсон, Гислен Куртуа и другие опубликовали первые отчеты о вирусе, который они назвали вирусом Конго. В 1956 году вирус Конго был впервые выделен врачом Гислен Куртуа, главой провинциальной медицинской лаборатории, Стэнливиль, в Бельгийском Конго. Штамм V3010, выделенный Куртуа, был отправлен в вирусную лабораторию Фонда Рокфеллера (RFVL) в Нью-Йорке и оказался идентичным другому штамму из Уганды, но ни одному другому названному
В июне 1967 года советский вирусолог Михаил Чумаков зарегистрировал изолят смертельного случая, произошедшего в Самарканде, в Каталоге вирусов, переносимых членистоногими.. В 1969 г. российский штамм, который Чумаков отправил в РФВЛ, был опубликован как идентичный вирусу Конго.
В 1973 г. Международный комитет по таксономии вирусов принял крымский - Официальное название вируса геморрагической лихорадки Конго.
Эти отчеты включают записи о появлении вируса или антител к вирусу из Греции, Португалии, Южной Африки, Мадагаскар (первая изоляция из там), Магриб, Дубай, Саудовская Аравия, Кувейт и Ирак.
| Классификация | D |
|---|---|
| Внешние ресурсы |