| Синдром Кокейна | |
|---|---|
| Другие названия | Синдром Нейла-Дингуолла |
| Специальность | Медицинская генетика, неврология, дерматология |
синдром Кокейна (CS), также называемый синдром Нейла-Дингуолла, является редким и смертельным аутосомным рецессивное нейродегенеративное расстройство, характеризующееся задержкой роста, нарушением развития нервной системы, аномальной чувствительностью к солнечному свету (светочувствительность ), глазные заболевания и преждевременное старение. Отсутствие нормального развития и неврологические расстройства являются критериями диагностики, в то время как светочувствительность, потеря слуха, аномалии глаз и кариес являются другими очень частыми признаками. Возможны проблемы с некоторыми или всеми внутренними органами. Это связано с группой заболеваний, называемых лейкодистрофиями, которые представляют собой состояния, характеризующиеся деградацией неврологического белого вещества. Основное заболевание - это дефект механизма репарации ДНК. В отличие от других дефектов репарации ДНК, пациенты с CS не предрасположены к раку или инфекции. Синдром Кокейна - редкое, но разрушительное заболевание, обычно приводящее к смерти в течение первого или второго десятилетия жизни. Мутации определенных генов при синдроме Кокейна известны, но широко распространенные эффекты и их связь с репарацией ДНК еще предстоит хорошо понять.
Он назван в честь английского врача Эдварда Альфреда Кокейна ( 1880–1956), который впервые описал его в 1936 году и повторно описал в 1946 году. Синдром Нил-Дингуолл был назван в честь Мэри М. Дингуолл и Кэтрин А. Нил. Эти два ученых описали случай двух братьев с синдромом Кокейна и заявили, что это была та же болезнь, которую описал Кокейн. В своей статье они способствовали появлению признаков болезни, обнаружив кальцификаты в головном мозге. Они также сравнили синдром Кокейна с тем, что сейчас известно как синдром прогерии Хатчинсона-Гилфорда (HGPS), который тогда назывался прогерией из-за позднего старения, характерного для обоих заболеваний.
Если гипероксия или избыток кислорода возникает в нашем организме, наши клеточный метаболизм производит несколько высокореактивных форм кислорода, называемых свободными радикалами. Это может вызвать окислительное повреждение клеточных компонентов, включая ДНК. В нормальных клетках наш организм восстанавливает поврежденные участки. В случае этого заболевания, из-за тонких дефектов в транскрипции, детский генетический механизм для синтеза белков, необходимых организму, не работает в нормальном режиме. То есть ученые полагали, что генетический механизм этих детей для синтеза белков, необходимых организму, не работает в нормальном режиме. Со временем эта теория привела к сбоям в развитии и смерти. Каждую минуту организм перекачивает от 10 до 20 литров кислорода через кровь, доставляя его к миллиардам клеток нашего тела. В своей нормальной молекулярной форме кислород безвреден. Однако клеточный метаболизм с участием кислорода может генерировать несколько высокоактивных свободных радикалов. Эти свободные радикалы могут вызывать окислительное повреждение клеточных компонентов, включая ДНК. В среднем человеческой клетке несколько тысяч повреждений возникают в ДНК каждый день. Многие из этих повреждений возникают в результате окислительного повреждения. Каждое поражение - поврежденный участок ДНК - необходимо вырезать, а ДНК отремонтировать, чтобы сохранить ее нормальную функцию. Необработанная ДНК может потерять способность кодировать белки. Также могут возникнуть мутации. Эти мутации могут активировать онкогены или заглушить гены-супрессоры опухоли. Согласно исследованиям, окислительное повреждение активных генов преимущественно не восстанавливается, а в наиболее тяжелых случаях восстановление замедляется по всему геному. В результате накопление окислительного повреждения может нарушить нормальные функции ДНК и даже может привести к запуску программы гибели клеток (апоптоза). У детей с этим заболеванием не восстанавливаются активные гены, вызывающие окислительное повреждение. Обычно восстановление окислительных повреждений происходит быстрее в активных генах (которые составляют менее пяти процентов генома), чем в неактивных областях ДНК. Возникающее в результате накопление окислительного повреждения может нарушить нормальные функции ДНК и может даже привести к запуску программы гибели клеток (апоптоз ).
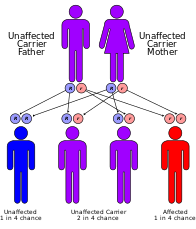
Синдром Кокейна классифицируется генетически следующим образом :
| Тип | OMIM | Ген |
|---|---|---|
| A | 216400 | ERCC8 (также называется CSA) |
| B | 133540 | ERCC6 (также называется CSB) |
| C | 216411 | неизвестно |
В отличие от клеток с нормальной способностью к восстановлению, клетки с дефицитом CSA и CSB неспособны преимущественно восстанавливать циклобутановые димеры пиримидина, вызванные действием ультрафиолетового (УФ) света. на матричной цепи активно транскрибируемых генов. Этот дефицит отражает потерю способности выполнять процесс репарации ДНК, известный как связанная с транскрипцией эксцизионная репарация нуклеотидов (TC-NER).
Внутри поврежденной клетки белок CSA обычно локализуется в сайтах повреждения ДНК, особенно межцепочечных сшивок, двухцепочечных разрывов и некоторых моноаддуктов. Белок CSB также обычно рекрутируется на участки повреждения ДНК, и его рекрутирование происходит наиболее быстро и надежно, а именно: межцепочечные сшивки>двухцепочечные разрывы>моноаддукты>окислительное повреждение. Белок CSB образует комплекс с другим белком репарации ДНК, SNM1A (DCLRE1A ), 5 '- 3' экзонуклеазой, которая локализуется в межцепочечных перекрестных связях в зависимости от транскрипции.. Накопление белка CSB в сайтах двухцепочечных разрывов ДНК происходит транскрипционно-зависимым образом и способствует гомологичной рекомбинационной репарации разрывов. Во время G0 /фазы G1 клеточного цикла повреждение ДНК может запускать CSB-зависимый процесс рекомбинационной репарации, в котором используется матрица РНК (а не ДНК ).
Признаки преждевременного старения CS, вероятно, обусловлены, по крайней мере частично, недостатками в репарации ДНК (см. теория старения повреждений ДНК ).
Люди с этим синдромом имеют меньший, чем обычно, размер головы (микроцефалия ), они невысокого роста (карликовость ), их глаза выглядят запавшими, и они имеют «пожилой» вид. У них часто есть длинные конечности с контрактурами суставов (неспособность расслабить мышцы в суставе), сгорбленная спина (кифоз ), и они могут быть очень тонкими (кахетическими ), из-за потери подкожного жира. Их маленький подбородок, большие уши и острый тонкий нос часто придают стареющий вид. Кожа людей с синдромом Кокейна также часто поражается: гиперпигментация, варикозное расширение или сосудистые звездочки (телеангиэктазии ) и s Повышенная чувствительность к солнечному свету является обычным явлением даже у людей без XP-CS. Часто пациенты с синдромом Кокейна получают сильные ожоги или волдыри при очень небольшом тепловом воздействии. Глаза пациентов могут быть поражены различными способами, и глазные аномалии являются обычным явлением при CS. Катаракта и помутнение роговицы (помутнение роговицы ) - обычное явление. Может произойти потеря или повреждение нервов зрительного нерва, вызывая атрофию зрительного нерва. Нистагм или непроизвольное движение глаз, а зрачки, которые не расширяются, демонстрируют потерю контроля над произвольными и непроизвольными движениями мышц. Пигментация сетчатки глаза солью и перцем также является типичным признаком. Диагноз устанавливается с помощью специального теста на восстановление ДНК, который измеряет восстановление РНК после воздействия УФ-излучения. Несмотря на то, что CS связан с генами, участвующими в эксцизионной репарации нуклеотидов (NER), в отличие от xeroderma pigmentosum, CS не связан с повышенным риском рака.
У пациентов с синдромом Кокейна облученные УФ-излучением клетки показывают снижение синтеза ДНК и РНК. https://emedicine.medscape.com/article/1115866-workup#c5 Лабораторные исследования в основном полезны для устранения других расстройств. Например, рентгенография скелета, эндокринологические тесты и исследования хромосомных разрывов могут помочь исключить нарушения, включенные в дифференциальный диагноз.
КТ головного мозга у пациентов с синдромом Кокейна может выявить кальцификаты и корковые атрофия.
Возможно дородовое обследование. Культивирование клеток амниотической жидкости используется для демонстрации того, что клетки плода испытывают дефицит синтеза РНК после УФ-облучения.
Визуализирующие исследования показывают широко распространенное отсутствие миелиновых оболочек нейронов белого вещества головного мозга и общую атрофию коры. Кальцификации были также обнаружены в скорлупе, области переднего мозга, которая регулирует движения и помогает в некоторых формах обучения, наряду с корой головного мозга. Кроме того, атрофия центральной области мозжечка, обнаруженная у пациентов с синдромом Кокейна, также может приводить к отсутствию мышечного контроля, особенно непроизвольному, и обычно наблюдается плохая осанка.
Постоянного излечения от этого синдрома не существует, хотя пациентов можно лечить симптоматически. Лечение обычно включает физиотерапию и небольшие операции на пораженных органах, например удаление катаракты. Также рекомендуется ношение солнцезащитного крема с высоким фактором и защитной одежды, потому что пациенты с синдромом Кокейна очень чувствительны к УФ-излучению. Также может помочь оптимальное питание. Родителям рекомендуется генетическое консультирование, так как вероятность передачи заболевания любым будущим детям составляет 25%. Также возможно пренатальное тестирование. Другой важный аспект - это предотвращение рецидива CS у других братьев и сестер. Выявление вовлеченных генных дефектов позволяет предложить генетическое консультирование и дородовое диагностическое тестирование родителям, у которых уже есть один больной ребенок.
прогноз для тех, у кого есть Синдром Кокейна плохой, так как смерть обычно наступает к 12 годам. Прогноз синдрома Кокейна зависит от типа заболевания. В зависимости от тяжести и начала симптомов существует три типа синдрома Кокейна. Однако различия между типами не всегда очевидны, и некоторые исследователи полагают, что признаки и симптомы отражают спектр, а не отдельные типы: синдром Кокейна типа A (CSA) характеризуется нормальным развитием, пока ребенку не исполнится 1 или 2 года. старые, в этот момент рост замедляется и отмечаются задержки в развитии. Симптомы не проявляются до 1 года. Ожидаемая продолжительность жизни для типа А составляет примерно от 10 до 20 лет. Эти симптомы наблюдаются у детей типа CS 1. Синдром Кокейна типа B (CSB), также известный как «церебро-окулофасцио-скелетный (COFS) синдром» (или «синдром Пена-Шокейра типа B»), является наиболее тяжелым подтипом. Симптомы присутствуют при рождении, и нормальное развитие мозга прекращается после рождения. Средняя продолжительность жизни детей с типом B - до 7 лет. Эти симптомы наблюдаются у детей 2 типа CS. Синдром Кокейна типа C (CSC) появляется позже в детстве с более легкими симптомами, чем другие типы, и более медленным прогрессированием заболевания. Люди с этим типом синдрома Кокейна доживают до взрослого возраста, средняя продолжительность жизни составляет от 40 до 50 лет. Эти симптомы наблюдаются при CS типа 3.
Синдром Кокейна встречается во всем мире редко. Не сообщается о расовой предрасположенности к синдрому Кокейна. Для синдрома Кокейна не описано сексуальных предпочтений; соотношение мужчин и женщин одинаковое. Синдром Кокейна I (CS-A) проявляется в детстве. Синдром Кокейна II (CS-B) проявляется при рождении или в младенчестве и имеет худший прогноз.
Недавнее исследование, проведенное в январе 2018 года, упоминает различные особенности CS, наблюдаемые во всем мире. со сходствами и различиями: CS имеет частоту 1 случай на 250 000 живорождений и распространенность 2,5 на миллион, что удивительно одинаково для разных регионов мира:
| Затронутые части | Клинические особенности | патология |
|---|---|---|
| Лицо | Морщинистые лица. Запавшие глаза, большие уши, тонкий заостренный нос. Маленький подбородок. Кариес зубов, гипоплазия эмали | |
| Кожа, волосы, ногти | Светочувствительность. Морщинистая и возрастная кожа. Тонкие сухие волосы, преждевременная седина. Плохой венозный доступ. | |
| Центральная нервная система | Микроцефалия обычно начинается в возрасте 2 лет. Умственная отсталость с низким IQ. Отложенные вехи. Тремор, атаксия, судороги, инсульты и субдуральные кровоизлияния. | Демиелинизация - неоднородная и сегментарная - «Метахроматическая лейкодистрофия ». Поражаются как олигодендроглии, так и клетки Шванна. Поражает церебральный белое вещество, мозолистое тело, ствол мозга, спинной мозг и периферические нервы. Нейроны потеря нескольких участков, особенно мозжечка. Потеря клеток переднего рога из-за антероградной и / или ретроградной дегенерации. кальцификации [55–95% ] коры головного мозга (особенно глубины борозд, базальных ганглиев, мозжечка, таламуса ; также артерий, артериолы и капилляры. Сосудистые изменения - особенно в областях метахроматической лейкодистрофии, кальцификации в лептоменингеальных сосудах, ускорение атеросклероз и артериолосклероз. Глиоз присутствует. Астроциты и микроглия могут иметь неправильную цитоплазму, множественные ядра. Может отображаться как белое вещество высокой интенсивности на сигналах последовательностей FLAIR MRI. Нет серьезных дефектов мозга . Наблюдается относительная щадимость коры головного мозга, небольшое истончение корковой ленты. Нормальный гиральный паттерн с расширением бороздок. Ламинирование, размер нейронов и конфигурация неокортекса сохраняются. Может проявляться теменное затылочное доминирование. Тяжелая атрофия мозжечка . Утрата Пуркинье, зернистых нейронов и в некоторых случаях нейронов в зубчатом ядре. Дендриты из клеток Пуркинье могут быть сильно деформированы («цветки кактуса»), железистые дендриты. У дендритов меньше ответвлений высшего порядка. Пуркинье «аксональные торпеды » могут присутствовать. Видны увеличение желудочков, увеличенная цистерна magna. Амилоидные бляшки, нейрофибриллярные клубки, тельца Хирано обычно не наблюдаются, хотя убиквитин реактивность аксонов присутствует |
| слух и вестибулярная система | нейросенсорная система, высокий тон потеря слуха [60–90%]. Смешанная кондуктивная и нейросенсорная тугоухость (44%) Чаще всего двусторонняя, редко односторонняя | Потеря волосковых клеток в улитке, особенно в базальном повороте. Потеря нейронов в спиральном ганглии. Атрофия слуховых путей. Scala communis, утолщенные ножки curare, расширенные prototympanum. Потеря волосковых клеток в верхней части. Потеря нейронов в вестибулярном ганглии. Коллапс эндолимфатического протока нижней части |
| Зрение | Помутнение роговицы. Катаракта [36–86%]. Обычно двусторонний, чаще всего развивается к 4 годам. Пигментная ретинопатия («соль и перец») [43–89%]. Миотическая зрачки, Диск зрительного нерва бледность, Энофтальм, Узкие глазные щели. | Местная потеря меланина пигмент гранулы. Отложение липофусцина, большие нагруженные пигментом клетки в периваскулярном распределении. Сетчатка пигмент эпителиальный атрофия и гиперплазия. Потеря клеток в ганглии и внешних слоях ядерных клеток. Поражаются как внешний, так и внутренний сегменты фоторецепторов . атрофия зрительного нерва с частичной демиелинизацией, потерей аксонов и глиозом |
| костно-мышечной системой | кахектикой карликовостью. Контракты. Кифоз, сколиоз. Сгорбленная поза. Мышечное истощение. | Денервация миопатия, атрофия неиспользования |
| Сердечно-сосудистая система | Ускоренная гипертензия. Расширение корня аорты. Кардиомиопатия. | Повышенное интима утолщение медиальной части. Атеросклероз, артериосклероз. |
| Желудочно-кишечная система | Тяжелый рефлюкс. Аномальная перистальтика желудочно-кишечного тракта. У многих есть подкожные гастростомические трубки. Гепатомегалия, спленомегалия, повышение ферментов печени. Измененный метаболизм лекарственных средств | - |
| Почечная система | Почечная недостаточность | Почечные артерии проявляются изменениями при прогрессирующем атеросклерозе и артериолосклерозе. Односторонние или гипоплазированные почки. |
| Репродуктивная система | - | - |
| Мужчины | Micropenis, меньший тестикулярный размер | - |
| Женщины | Атрофия яичников. Сообщается об успешной беременности. | - |
| Эндокринная система | Нормальные вторичные половые признаки. Нормальный гормон роста, тиреотропный гормон, уровень кальция | Нормальный гипофиз и щитовидная железа |
| Эккринная система | Снижение потоотделения, слез, слюны | - |
| Классификация | D |
|---|---|
| Внешние ресурсы |