 | |
 | |
| Имена | |
|---|---|
| Другие имена Хлорная кислота (V) acid | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.303 |
| Номер ЕС |
|
| PubChem CID | |
| UNII | |
| Номер ООН | 2626 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | HClO 3 |
| Молярная масса | 84,45914 г моль |
| Внешний вид | бесцветный раствор |
| Плотность | 1 г / мл, раствор (приблизительно) |
| Растворимость в воде | >40 г / 100 мл (20 ° C) |
| Кислотность (pK a) | ~ -1 |
| Основание конъюгата | Хлорат |
| Структура | |
| Молекулярная форма | пирамидная |
| Опасности | |
| Основные опасности | Окислитель, коррозионный |
| Паспорт безопасности | См.: страница данных |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H271, H314 |
| Меры предосторожности GHS | P210, P220, P221, P260, P264, P280, P283, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P306 + 360, P310, P321, P363, P370 + 378, P371 + 380 + 375, P405, P501 |
| NFPA 704 (огненный алмаз) |  0 3 2 OX 0 3 2 OX |
| Родственные соединения | |
| Другие анионы | бромная кислота. йодная кислота |
| Другие катионы | хлорат аммония. хлорат натрия. хлорат калия |
| Родственные соединения | соляная кислота. хлорноватистая кислота. хлорноватистая кислота. хлорная кислота |
| Дополнительный страница данных | |
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая постоянная (εr) и т. д. |
| Термодинамические. данные | Фаза поведение. твердое тело – жидкость – газ |
| Спектральные данные | UV, IR, ЯМР, MS |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [ 77 ° F], 100 кПа). | |
| Ссылки в ink | |
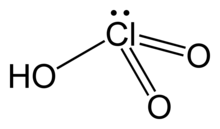
Хлорная кислота, H Cl O 3, является оксокислотой из хлора и формальным предшественником хлората соли. Это сильная кислота (pKa ≈ -2,7) и окислитель.
Хлорная кислота термодинамически нестабильна по отношению к диспропорционированию.
Хлорная кислота стабильна в холодном водном растворе до концентрации примерно 30% и в растворе до 40%. может быть приготовлен осторожным упариванием при пониженном давлении. Выше этих концентраций растворы хлорноватой кислоты разлагаются с образованием различных продуктов, например:
Хлорная кислота - мощный окислитель. Большинство органических и легковоспламеняющихся веществ сгорают при контакте.
Его можно получить реакцией серной кислоты с хлоратом бария, причем нерастворимый сульфат бария удаляется осаждением:
Другим методом является нагревание хлорноватистой кислоты с образованием хлорноватистой кислота и хлористый водород :