 Часть Клеточного цикла
Часть Клеточного цикла Создание сотовой модели было особенно сложной задачей системной биологии и математической биологии. Он включает в себя разработку эффективных алгоритмов, структур данных, визуализации и средств коммуникации для организации интеграции больших объемов биологических данных с целью компьютерного моделирования..
Он также напрямую связан с биоинформатикой, вычислительной биологией и искусственной жизнью.
. Он включает использование компьютерных симуляций многих клеточные подсистемы, такие как сети метаболитов и ферментов, которые включают метаболизм, пути передачи сигнала и сети регуляции генов для анализа и визуализации сложных связей этих клеточных процессов.
Сложная сеть процессов биохимических реакций / переноса и их пространственная организация делают разработку прогнозной модели живой клетки серьезной задачей 21 века.
Эукариотический клеточный цикл очень сложен и является одной из наиболее изучаемых тем, поскольку неправильное его регулирование приводит к раку. Возможно, это хороший пример математической модели, поскольку она имеет дело с простыми вычислениями, но дает достоверные результаты. Две исследовательские группы создали несколько моделей клеточного цикла, имитирующих несколько организмов. Недавно они создали общую модель эукариотического клеточного цикла, которая может представлять конкретного эукариота в зависимости от значений параметров, демонстрируя, что идиосинкразии отдельных клеточных циклов обусловлены разными концентрациями белка и сродством, в то время как лежащие в основе механизмы сохраняются (Csikasz -Nagy et al., 2006).
С помощью системы обыкновенных дифференциальных уравнений эти модели показывают изменение во времени (динамическая система ) белка внутри одной типичной клетки; этот тип модели называется детерминированным процессом (тогда как модель, описывающая статистическое распределение концентраций белка в популяции клеток, называется стохастическим процессом ).
Чтобы получить эти уравнения, необходимо выполнить повторяющуюся серию шагов: сначала несколько моделей и наблюдений объединяются, чтобы сформировать консенсусную диаграмму, и выбираются соответствующие кинетические законы для написания дифференциальных уравнений, например кинетика скорости для стехиометрических реакций, кинетика Михаэлиса-Ментен для реакций с субстратом фермента и кинетика Голдбетера-Кошланда для сверхчувствительных факторов транскрипции, затем параметры уравнений (константы скорости, фермент коэффициенты эффективности и константы Михаэлиса) должны соответствовать наблюдениям; когда они не могут быть установлены, кинетическое уравнение пересматривается, а когда это невозможно, изменяется электрическая схема. Параметры подбираются и проверяются с использованием наблюдений как за диким типом, так и за мутантами, такими как период полужизни белка и размер клеток.
Чтобы подобрать параметры, необходимо изучить дифференциальные уравнения. Это можно сделать либо путем моделирования, либо путем анализа.
При моделировании, учитывая начальный вектор (список значений переменных), прогрессия системы вычисляется путем решения уравнений в каждом временном кадре с небольшими приращениями.
При анализе свойства уравнений используются для исследования поведения системы в зависимости от значений параметров и переменных. Система дифференциальных уравнений может быть представлена как векторное поле , где каждый вектор описывает изменение (в концентрации двух или более белков), определяющее, куда и как быстро движется траектория (моделирование). Векторные поля могут иметь несколько специальных точек: стабильная точка, называемая стоком, которая притягивается во всех направлениях (заставляя концентрации быть на определенном уровне), либо источник, либо седло . точка, которая отталкивает (вынуждая концентрации изменяться от определенного значения), и предельный цикл, замкнутая траектория, к которой несколько траекторий движутся по спирали (заставляя концентрации колебаться).
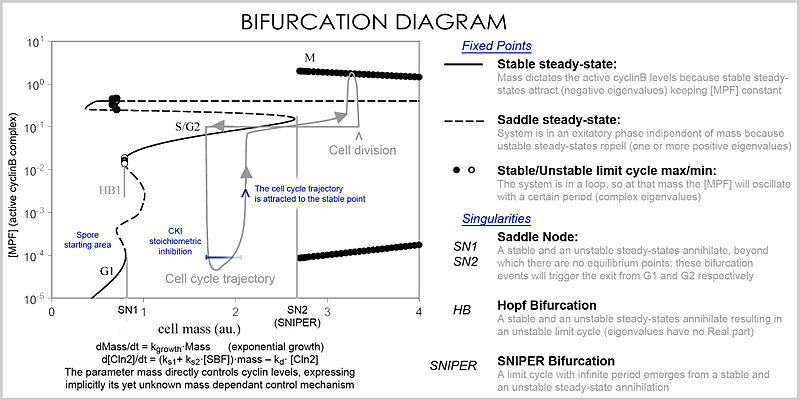
Лучшее представление, которое может обрабатывать большое количество переменных и параметров, называется бифуркационной диаграммой (теория бифуркации ): наличие этих особых точек устойчивого состояния при определенных значениях параметра (например, масса) представлена точкой, и как только параметр переходит определенное значение, происходит качественное изменение, называемое бифуркацией, при которой изменяется природа пространства с глубокими последствиями для концентраций белка: клеточный цикл имеет фазы (частично соответствующие G1 и G2), в которых масса через стабильную точку контролирует уровни циклина, и фазы (фазы S и M), в которых концентрации изменяются независимо, но после того, как фаза изменилась при бифуркации событие (контрольная точка клеточного цикла ), система не может вернуться к предыдущим уровням, так как при текущей массе векторное поле сильно отличается, и масса не может быть обращена обратно через событие бифуркации, что делает контрольную точку необратимой. В частности, контрольные точки S и M регулируются с помощью специальных бифуркаций, называемых бифуркацией Хопфа и бесконечным периодом бифуркации.
Cell Collective - это программное обеспечение для моделирования что позволяет хранить динамические биологические данные, строить вычислительные модели, стимулировать, ломать и воссоздавать модели. Разработкой руководит Томас Геликар, исследователь в области вычислительной биологии. Он предназначен для биологов, студентов, изучающих вычислительную биологию, учителей, специализирующихся на преподавании наук о жизни, и исследователей в области наук о жизни. Сложности математики и информатики встроены в серверную часть, и можно узнать о методах, используемых для моделирования биологических видов, но сложные математические уравнения, алгоритмы, программирование не требуются и, следовательно, не будут препятствовать построению модели.
Математическая структура, лежащая в основе Cell Collective, основана на общем качественном (дискретном) методе моделирования, в котором регуляторный механизм каждого узла описывается логической функцией [для более полной информации о логическом моделировании см.].
Проверка модели Модель была построена с использованием локальной (например, белок-белковое взаимодействие) информации из первичной литературы. Другими словами, на этапе построения модели не было попыток определить локальные взаимодействия на основе каких-либо других более крупных фенотипов или явлений. Однако после того, как модель была завершена, проверка точности модели включала проверку ее способности воспроизводить сложные явления ввода-вывода, которые наблюдались в лаборатории. Для этого модель Т-клеток была смоделирована во множестве клеточных условий и проанализирована с точки зрения кривых «вход-выходная доза-реакция», чтобы определить, ведет ли модель себя так, как ожидалось, включая различные последующие эффекты в результате активации TCR., Пути рецепторов, цитокинов и интегрина, сопряженных с G-белком.
Цель проекта E-Cell Project «сделать возможным точное моделирование целых клеток на молекулярном уровне».
- разработан В. А. Шива Айядурай и К. Форбс Дьюи-младший из отдела биологической инженерии Массачусетского технологического института - предложили метод моделирования всей клетки путем динамической интеграции нескольких моделей молекулярных путей.. "
В июльском выпуске журнала Cell за 2012 год группа под руководством Маркуса Коверта из Стэнфорда опубликовала наиболее полную на сегодняшний день вычислительную модель ячейки. Модель из примерно 500 генов Mycoplasma genitalium содержит 28 алгоритмически независимых компонентов, включающих работу из более чем 900 источников. Он отвечает за взаимодействия полного генома, транскриптома, протеом и метаболом организма, что свидетельствует о значительном прогрессе в данной области.
Большинство попыток моделирования процессов клеточного цикла были сосредоточены на широких и сложных молекулярных взаимодействиях множества различных химических веществ, включая несколько молекул циклин и циклин-зависимых киназ, поскольку они соответствуют фазам S, M, G1 и G2 клеточного цикла . В статье, опубликованной в 2014 году в журнале «Вычислительная биология PLOS», сотрудники Оксфордского университета, Технологического института Вирджинии и Institut de Génétique et Développement де Ренн создал упрощенную модель клеточного цикла, используя только одно взаимодействие циклин / CDK. Эта модель показала способность контролировать полностью функциональное деление клетки посредством регулирования и манипулирования только одним взаимодействием и даже позволила исследователям пропускать фазы за счет изменения концентрации CDK. Эта модель может помочь понять, как относительно простые взаимодействия одного химического вещества переходят в модель клеточного деления на уровне клетки.
Выполняются несколько проектов.