| |||
 | |||
| Имена | |||
|---|---|---|---|
| Другие имена Пероксид мочевины, перкарбамид, UHP | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.275 | ||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | C H 6 N 2 O 3 | ||
| Молярная масса | 94,070 г моль -1 | ||
| Появление | Белое твердое вещество | ||
| Плотность | 1,50 г / см 3 | ||
| Температура плавления | От 75 до 91,5 ° C (от 167,0 до 196,7 ° F; от 348,1 до 364,6 K) (разлагается) | ||
| Фармакология | |||
| Код УВД | D02AE01 ( ВОЗ ) | ||
| Опасности | |||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| Классификация ЕС (DSD) (устаревшая) | | ||
| точка возгорания | 60 ° С (140 ° F, 333 К) | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
Перекись водорода - мочевина (также называемая Hyperol, артизон, перекись водорода мочевины и UHP) представляет собой твердое вещество, состоящее из равных количеств перекиси водорода и мочевины. Это соединение представляет собой белое кристаллическое твердое вещество, которое растворяется в воде с образованием свободной перекиси водорода. Перекись водорода - мочевина содержит твердую и безводную перекись водорода, которая при использовании в качестве окислителя обеспечивает более высокую стабильность и лучшую управляемость, чем жидкая перекись водорода. В стоматологическом кабинете часто называют перекисью карбамида, она используется в качестве источника перекиси водорода для отбеливания, дезинфекции и окисления.
Для приготовления комплекса мочевину растворяют в 30% перекиси водорода (мольное соотношение 2: 3) при температуре ниже 60 ° C. при охлаждении этого раствора перекись водорода - мочевина выпадает в осадок в виде небольших тромбоцитов.
Определение содержания перекиси водорода титрованием раствором перманганата калия дает значение 35,4%, что соответствует 97,8% от теоретического максимального значения. Остальная примесь состоит из мочевины.
Подобно кристаллизационной воде, перекись водорода совместно кристаллизуется с мочевиной со стехиометрией 1: 1. Соединение просто получают (в масштабе нескольких сотен тонн в год) растворением мочевины в избытке концентрированного раствора перекиси водорода с последующей кристаллизацией. Аналогичен лабораторный синтез.
Твердотельная структура этого аддукта была определена методом дифракции нейтронов.
Пероксид водорода-мочевина представляет собой легко растворимое в воде кристаллическое твердое вещество без запаха, которое доступно в виде белого порошка, бесцветных игл или тромбоцитов. При растворении в различных растворителях комплекс 1: 1 диссоциирует обратно на мочевину и перекись водорода. Так же, как и перекись водорода, (ошибочно) так называемый аддукт является окислителем, но высвобождение при комнатной температуре в присутствии катализаторов происходит контролируемым образом, поэтому соединение подходит в качестве безопасной замены нестабильного водного раствора водорода. перекисью. Из-за тенденции к термическому разложению, которое ускоряется при температурах выше 82 ° C, его не следует нагревать выше 60 ° C, особенно в чистом виде.
Растворимость коммерческих образцов варьируется от 0,05 г / мл до более 0,6 г / мл.
Перекись водорода - мочевина в основном используется в качестве дезинфицирующего и отбеливающего средства в косметике и фармацевтике. В качестве лекарственного средства это соединение используется в некоторых препаратах для отбеливания зубов. Он также используется для снятия незначительного воспаления десен, поверхностей слизистой оболочки полости рта и губ, включая язвы и раздражение зубов, а также для эмульгирования и диспергирования ушной серы.
Пероксид карбамида также подходит в качестве дезинфицирующего средства, например, для уменьшения количества микробов на поверхностях контактных линз или в качестве антисептика для полосканий рта, ушных капель или для поверхностных ран и язв.
В лаборатории он используется как более простой в использовании заменитель перекиси водорода. Доказано, что он является стабильным, простым в обращении и эффективным окислителем, которым легко управлять путем подходящего выбора условий реакции. Он доставляет продукты окисления экологически безопасным способом и часто с высокими выходами, особенно в присутствии органических катализаторов, таких как цис- бутендиовый ангидрид, или неорганических катализаторов, таких как вольфрамат натрия.

Он избирательно превращает тиолы в дисульфиды, вторичные спирты в кетоны, сульфиды в сульфоксиды и сульфоны, нитрилы в амиды, N- гетероциклы в оксиды аминов.

Гидроксибензальдегид превращается в дигидроксибензолы ( реакция Дакина ) и дает в подходящих условиях соответствующие бензойные кислоты.
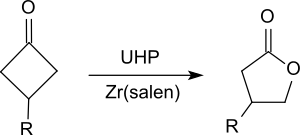
Он окисляет кетоны до сложных эфиров, в частности циклических кетонов, таких как замещенные циклогексаноны или циклобутаноны, с образованием лактонов ( окисление Байера-Виллигера ).
Эпоксидирование различных алкенов в присутствии бензонитрила дает оксираны с выходами от 79 до 96%.
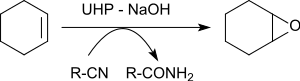
Атом кислорода, перенесенный на алкен, происходит от пероксоимидной кислоты, образующейся промежуточно из бензонитрила. Образовавшаяся имидовая кислота таутомеризуется в бензамид.
Соединение действует как сильный окислитель и может вызвать раздражение кожи и серьезное повреждение глаз.