 . 2D-структура цитрата кальция . 2D-структура цитрата кальция | |
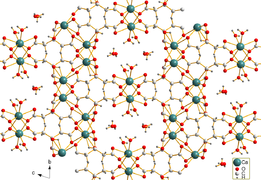 . Тетрагидрат цитрата кальция . Тетрагидрат цитрата кальция | |
| Названия | |
|---|---|
| Название IUPAC Кальциевая соль 2-гидрокси-1,2,3-пропан-трикарбоновой кислоты (2: 3) | |
| Другие названия E333, трикальций дицитрат | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.011.265 |
| Номер EC |
|
| Номер E | E333 (антиоксиданты,...) |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | Ca3(C6H5O7)2 |
| Молярная масса | 498,4334 г / моль (безводный). 570,4945 г / моль (тетрагидрат) |
| Внешний вид | Белый порошок |
| Запах | без запаха |
| Плотность | 1,63 г / см (безводный). 2,00 г / см (тетрагидрат) |
| Точка плавления | Разлагается |
| Кипение точка | Разлагается |
| Растворимость в воде | 0,85 г / л (18 ° C). 0,95 г / л (25 ° C) |
| Растворимость | не растворим в спирте |
| Структура | |
| Кристаллическая структура | Триклин (тетрагидрат) |
| Пространственная группа | P1, № 2 |
| Постоянная решетки | a = 0,59466 (4) нм, b = 1,02247 (8) нм, c = 1,66496 (13) нм α = 72,213 (7) °, β = 79,718 (7) °, γ = 89,791 (6) ° |
| Опасности | |
| Основные га zards | Раздражающий |
| NFPA 704 (огненный алмаз) |  1 1 0 1 1 0 |
| Родственные соединения | |
| Другие катионы | цитрат натрия |
| Если не указано иное, данные приводятся для материалы в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Кальций цитрат представляет собой кальциевую соль лимонной кислоты. Обычно он используется в качестве пищевой добавки (E333 ), обычно в качестве консерванта, но иногда для ароматизатора. В этом смысле он аналогичен цитрату натрия. Цитрат кальция также содержится в некоторых пищевых добавках с кальцием (например, Citracal). Кальций составляет 24,1% цитрата кальция (безводного) и 21,1% цитрата кальция (тетрагидрата) по массе. Тетрагидрат встречается в природе как минерал Эрландит.
Цитрат кальция плохо растворим в воде. Игольчатые кристаллы тетрагидрата дицитрата трикальция [Ca 3(C6H5O7)2(H2O)2] · 2H 2 O были получены гидротермальным синтезом. Кристаллическая структура представляет собой трехмерную сеть, в которой восьмикратно координированные катионы Са связаны цитратными анионами и водородными связями между двумя некоординирующими молекулами кристаллической воды и двумя координирующими молекулами воды.
Цитрат кальция является промежуточным продуктом при выделении лимонной кислоты из процесса ферментации, с помощью которого лимонную кислоту получают промышленным способом. Лимонная кислота в бульонном растворе нейтрализуется гидроксидом кальция, осаждая нерастворимый цитрат кальция. Затем его отфильтровывают от остальной части бульона и промывают, чтобы получить чистый цитрат кальция.
Полученный таким образом цитрат кальция можно продавать как есть или он может быть преобразован в лимонную кислоту с использованием разбавленной серной кислоты.
Установлено, что у многих людей биодоступность цитрата кальция равна биодоступности более дешевого карбоната кальция. Однако изменения в пищеварительном тракте могут изменить способ переваривания и всасывания кальция. В отличие от карбоната кальция, который является основным и нейтрализует желудочную кислоту, цитрат кальция не влияет на желудочную кислоту. Карбонат кальция усваивается труднее, чем цитрат кальция, а карбонат кальция несет в себе риск «отскока кислоты» (желудок чрезмерно компенсирует это за счет производства большего количества кислоты), поэтому люди, чувствительные к антацидам или испытывающие трудности с выработкой адекватной желудочной кислоты, могут выбрать цитрат кальция. над карбонатом кальция для добавок. Согласно недавнему исследованию абсорбции кальция после операции желудочного обходного анастомоза, цитрат кальция может иметь улучшенную биодоступность по сравнению с карбонатом кальция у пациентов с обходным желудочным анастомозом по Ру, которые принимают цитрат кальция в качестве пищевой добавки после операции. В основном это связано с изменениями, связанными с тем, где происходит всасывание кальция в пищеварительном тракте этих людей.