 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.030.331 |
| Номер EC |
|
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
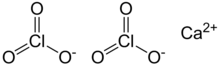
| Химическая формула | Ca (ClO 3)2 |
| Молярная масса | 206,98 г / моль |
| Внешний вид | белое твердое вещество. расплывающееся вещество |
| Запах | без запаха |
| Плотность | 2,71 г / см |
| Температура плавления | 150 ° C (дигидрат, разл.). 325 ° C |
| Растворимость в воде | 209 г / 100 мл (20 ° C). 197 г / 100 мл (25 ° C) |
| Структура | |
| Кристаллическая структура | моноклинная |
| Опасности | |
| NFPA 704 (огненный алмаз) |  0 1 1 OX 0 1 1 OX |
| Родственные соединения | |
| Другое анионы | хлорид кальция. кальций br омат. бромид кальция |
| Другие катионы | хлорат калия. хлорат натрия. хлорат бария. хлорат магния |
| Если не указано иное, данные для материалов приводятся в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Хлорат кальция представляет собой соль кальция хлорноватой кислоты с химической формулой Ca (ClO 3)2. Как и другие хлораты, это сильный окислитель.
Хлорат кальция получают путем пропускания газа хлора через горячую суспензию гидроксида кальция в воде с образованием гипохлорита кальция, который диспропорционирует при нагревании с избытком хлора с образованием хлората кальция и хлорида кальция :
Это также первая стадия производства хлората калия.
Теоретически электролиз горячего раствора хлорида кальция даст хлорат, аналогичный процессу, используемому для производства хлората натрия. На практике электролиз осложняется осаждением гидроксида кальция на катоде, препятствующим прохождению тока.
Когда концентрированные растворы хлората кальция и хлорида калия смешиваются осаждается связанный хлорат калия:
Это вторая стадия процесса Либиха для производства хлората калия.
Растворы хлората кальция реагируют с растворами карбонатов щелочных металлов с образованием осадка карбоната кальция и хлората щелочного металла в растворе:
При сильном нагревании хлорат кальция разлагается с образованием кислорода и хлорида кальция:
Холодные разбавленные растворы хлората кальция и серной кислоты реагируют с образованием осадка сульфата кальция и хлорноватой кислоты в растворе:
Контакт с сильной серной кислотой может привести к взрывам из-за нестабильности концентрированной хлорноватой кислоты. Контакт с соединениями аммония также может вызвать бурное разложение из-за образования нестабильного хлората аммония.
Хлорат кальция использовался в качестве гербицида, например натрия хлорат.
Хлорат кальция иногда используется в пиротехнике в качестве окислителя и красителя розового пламени. Его гигроскопичность и несовместимость с другими распространенными пиротехническими материалами (такими как сера ) ограничивают его применимость в этих приложениях.