 | |
| Названия | |
|---|---|
| Название IUPAC Сульфат кадмия (II) | |
| Другие названия Серный кислота, соль кадмия (1: 1),. | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChEBI |
|
| ChemSpider | |
| ECHA InfoCard | 100.030.288 |
| Номер EC |
|
| Ссылка Gmelin | 8295 |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| номер ООН | 2570 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | CdSO 4. CdSO 4·H2O (моногидрат). 3CdSO 4 · 8H 2 O (октагидрат) |
| Молярная масса | 208,47 г / моль (безводный). 226,490 г / моль (моногидрат). 769,546 г / моль (октагидрат) |
| Внешний вид | Белый гигроскопичный твердый |
| Запах | без запаха |
| Плотность | 4,691 г / см (безводный). 3,79 г / см (моногидрат). 3,08 г / см (октагидрат) |
| Температура плавления | 1000 ° C (1830 ° F; 1270 K) (безводный). 105 ° C (моногидрат). 40 ° C (октагидрат) |
| Температура кипения | (разлагается до основного сульфата, а затем оксида) |
| Растворимость в воде | безводный:. 75 г / 100 мл (0 ° C). 76,4 г / 100 мл (25 ° C). 58,4 г / 100 мл (99 ° C) моногидрат:. 76,7 г / 100 мл (25 ° C) октагидрата:. очень растворим |
| Растворимость | мало растворим в метаноле, этилацетат. нерастворим в этанол |
| Магнитная восприимчивость (χ) | -59,2 · 10 см / моль |
| Показатель преломления (nD) | 1,565 |
| Структура | |
| Кристаллическая структура | орторомбическая (безводная). моноклинная (гепта- и октагидрат) |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 123 Дж · моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −935 кДж · моль |
| Опасности | |
| Паспорт безопасности | [1] |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H301, H330, H340, H350, H360, H372, H400, H41 0 |
| Меры предосторожности GHS | P201, P202, P260, P264, P270, P271, P273, P281, P284, P301 + 310, P304 + 340, P308 + 313, P310, P314, P320, P321, P330, P391, P403 + 233, P405, P501 |
| NFPA 704 (огненный алмаз) |  1 3 0 1 3 0 |
| Летальная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 280 мг / кг (перорально, крыса) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимая) | [1910,1027] TWA 0,005 мг / м (в виде Cd) |
| REL (рекомендуется) | Ca |
| IDLH (непосредственная опасность) | Ca [9 мг / м (в виде Cd) ] |
| Родственные соединения | |
| Другие анионы | Ацетат кадмия,. Хлорид кадмия,. Нитрат кадмия |
| Другие катионы | Сульфат цинка,. Сульфат кальция,. Сульфат магния |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобокс | |
Сульфат кадмия - это название серии родственных неорганических соединений с формулой CdSO 4 · xH 2 O. Наиболее распространенной формой является моногидрат CdSO 4·H2O, но известны две другие формы CdSO 4 · ⁄ 3H2O и безводная соль (CdSO 4). Все соли бесцветны и хорошо растворяются в воде.
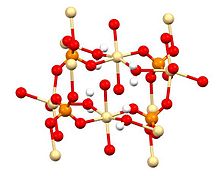
Рентгеновская кристаллография показывает, что CdSO 4·H2O является типичным координационным полимером. Каждый центр Cd имеет октаэдрическую координационную геометрию, будучи окруженным четырьмя кислородными центрами, обеспечиваемыми четырьмя сульфатными лигандами и двумя кислородными центрами из мостикового водного лиганда.
октогидрат сульфата кадмия может может быть получен реакцией металлического кадмия, его оксида или гидроксида с разбавленной серной кислотой:
Безводный материал получают с использованием персульфата натрия :
Чистый сульфат кадмия имеет вид очень редкие минералы дробецит (CdSO 4 · 4H 2 O), воудуризит (моногидрат) и лазаридизит (8/3-гидрат).
Сульфат кадмия широко используется для гальваники кадмия в электронных схемах. Он также является предшественником пигмента на основе кадмия, такого как сульфид кадмия. Он также используется для электролита в стандартной ячейке Weston, а также в качестве пигмента в флуоресцентных экранах.