 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название IUPAC Пентафторид брома | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.029.234 | ||
| Номер EC |
| ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| номер ООН | 1745 | ||
| CompTox Dashboard (EPA ) | |||
InChI
| |||
SMILES
| |||
| Свойства | |||
| Химическая формула | BrF 5 | ||
| Молярный масса | 174,894 г · моль | ||
| Внешний вид | Бледно-желтая жидкость | ||
| Плотность | 2,466 г / см | ||
| Температура плавления | -61,30 ° C (-78,34 ° F; 211,85 K) | ||
| Температура кипения | 40,25 ° C (104,45 ° F; 313,40 K) | ||
| Растворимость в воде | Реагирует с водой | ||
| Структура | |||
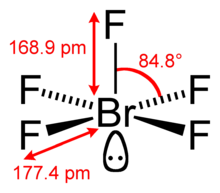
| Молекулярная форма | Квадратная пирамидальная | ||
| Опасности | |||
| Главная опасности | Бурно реагирует с водой, сильным окислителем | ||
| Паспорт безопасности | См.: страница данных. Внешний паспорт безопасности материала | ||
| Пиктограммы GHS |     | ||
| Сигнальное слово GHS | Опасно | ||
| Краткая характеристика опасности GHS | H271, H305, H314, H318, H330, H370, H371, H373 | ||
| Меры предосторожности GHS | P210, P220, P221, P260, P264, P270, P271, P280, P283, P284, P301 + 310, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P306 + 360, P307 + 311, P309 + 311, P310, P314, P320, P321, P331, P363, P370 + 378 | ||
| NFPA 704 (огненный алмаз) |  0 4 3 0 4 3 | ||
| Температура вспышки | Невоспламеняющийся | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (Допустимо) | нет | ||
| REL (рекомендуется) | TWA 0,1 ppm (0,7 мг / м) | ||
| IDLH (немедленно опасность) | ND | ||
| Родственные соединения | |||
| Другие анионы | Монохлорид брома | ||
| Прочие катионы | Пентафторид хлора. Пентафторид йода | ||
| Родственные соединения | Монофторид брома. Трифторид брома | ||
| Страница дополнительных данных | |||
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr), и т.д. | ||
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ | ||
| Спектральные данные | UV, IR, ЯМР, MS | ||
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Пентафторид брома, Br F5, представляет собой межгалогенное соединение и фторид брома. Это сильный реагент фторирования.
BrF 5 находит применение в кислородном изотопном анализе. Лазерная абляция твердых силикатов в присутствии пентафторида брома высвобождает O2 для последующего анализа. Он также был испытан как окислитель в жидких ракетных топливах и используется в качестве фторирующего агента при переработке урана.
Пентафторид брома впервые был получен в 1931 году путем прямой реакции брома с фтором.. Эта реакция подходит для получения больших количеств и проводится при температуре выше 150 ° C (302 ° F) с избытком фтора:
Для получения меньших количеств используется бромид калия :
Этот способ дает пентафторид брома, почти полностью свободный от трифторидов. и другие примеси.
Пентафторид брома бурно реагирует с водой, но с образованием бромной кислоты и плавиковой кислоты (особенно при замедлении разбавление ацетонитрилом ), продукты простого гидролиза:
Это чрезвычайно эффективный фторирующий агент, способный превращать большинство соединений урана в гексафторид урана при комнатной температуре.
Пентафторид брома сильно разъедает кожу, а его пары раздражают глаза, кожу и слизистые оболочки. Во влажном воздухе он фактически выделяет «дым», содержащий пары фтористоводородной кислоты, возникающий в результате реакции с водой в воздухе. Кроме того, воздействие 100 ppm или более в течение более одной минуты смертельно для большинства экспериментальных животных. Хроническое воздействие может вызвать повреждение почек и печеночную недостаточность.
Оно может самопроизвольно воспламениться или взорваться при контакте с органическими материалами или металлической пылью.