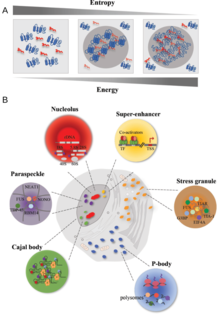
 Образование и примеры безмембранных органелл
Образование и примеры безмембранных органелл Биомолекулярные конденсаты относятся к классу не мембранных связанные органеллы и субдомены органелл. Как и другие органеллы, биомолекулярные конденсаты представляют собой специализированные субъединицы клетки. Однако, в отличие от многих органелл, состав биомолекулярного конденсата не контролируется связывающей мембраной. Вместо этого они могут образовываться с помощью ряда различных процессов, наиболее известным из которых является разделение фаз белков, РНК и других биополимеров в коллоидные эмульсии, жидкие кристаллы, твердые кристаллы или агрегаты внутри клеток.
 Гранулы крахмала кукурузы
Гранулы крахмала кукурузы Мицеллярная теория Карла Нэгели была разработана на основе его подробного исследования крахмала гранул в 1858 году. Были предложены аморфные вещества, такие как крахмал и целлюлоза состоит из строительных блоков, упакованных в рыхлую кристаллическую решетку с образованием, которое он позже назвал «мицеллами». Вода может проникать между мицеллами, и новые мицеллы могут образовываться в промежутках между старыми мицеллами. Набухание крахмальных зерен и их рост был описан с помощью молекулярно-агрегатной модели, которую он также применил к целлюлозе клеточной стенки растений. Современное использование «мицеллы » относится строго к липидам, но его первоначальное использование явно распространилось на другие типы биомолекул, и это наследие до сих пор отражается в описании молока как состоит из «казеина мицелл».
Термин «коллоид » был введен Вольфгангом Оствальдом и определен Томасом Грэмом в 1861, чтобы описать поведение определенных биологических макромолекул (крахмал, альбумин, желатин и т. Д.) И неорганических молекул как медленно диффундирующих компонентов мутного жидкий раствор - суспензии, которые были заблокированы полупроницаемыми мембранами, в то время как физика разделения фаз была описана Джозайей Уиллардом Гиббсом в его знаменательной статье под названием О равновесии гетерогенных веществ, опубликованной частями между 1875 и 1878 годами. Под влиянием Уилларда Гиббса важный вклад также внес Йоханнес Дидерик ван дер Ваальс, который в 1890 г. опубликовал трактат по теории бинарных растворов.
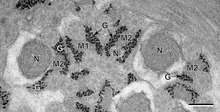 Гранулы гликогена в спермиогенезе у Pleurogenidae (Digenea)
Гранулы гликогена в спермиогенезе у Pleurogenidae (Digenea) Концепция внутриклеточных коллоидов как организующего принципа для Компартментализация живых клеток восходит к концу 19 века, начиная с Уильяма Бэйта Харди и Эдмунда Бичера Уилсона, которые описали цитоплазму (тогда называемую 'протоплазма ') как коллоид. Примерно в то же время Томас Харрисон Монтгомери-младший описал морфологию ядрышка, органеллы в ядре, которая, как впоследствии было показано, образуется в результате внутриклеточного разделения фаз . У. Б. Харди связал образование биологических коллоидов с разделением фаз в своем исследовании глобулинов, заявив, что: «Глобулин диспергирован в растворителе в виде частиц, которые являются коллоидными частицами и которые настолько велики, что образуют внутреннюю фазу ", а также внесли свой вклад в базовое физическое описание разделения фаз нефть-вода.
Коллоидное разделение фаз как движущая сила в клеточной организации привлекло решительно Стефану Ледюку, который написал в своей влиятельной книге 1911 года «Механизм жизни»: «Следовательно, изучение жизни может быть лучше всего начато с изучения тех физико-химических явлений, которые возникают в результате контакта двух различных жидкости Таким образом, биология - это всего лишь раздел физико-химии жидкостей; она включает изучение электролитических и коллоидных растворов, а также молекулярных сил, задействованных в растворе, осмосе, диффузии, когезии и кристаллизации ».
Первобытный суп теория происхождения жизни, предложенная Александром Опариным на русском языке в 1924 году (опубликована на английском языке в 1936 году) и Дж. Б.С. Холдейн в 1929 году предположил, что жизни предшествовало образование того, что Холдейн называл «горячим разбавленным супом» из «коллоидных органических веществ», и которые Опарин называл «коацерватами '(по де Йонгу) - частицы, состоящие из двух или более коллоидов, которые могут быть белком, липидом или нуклеиновой кислотой. Эти идеи сильно повлияли на последующую работу Сидни В. Фокса над протеиноидными микросферами.
В 1922 году Герман Штаудингер усовершенствовал теорию коллоидной ассоциации из Томаса Грэма, предложив, что определенные коллоиды состоят из высокомолекулярных полимеров (цепи, соединенные ковалентными связями ), которые он назвал «макромолекулами », чтобы отличить их от коллоидные кластеры молекул с более низкой молекулярной массой. коллоидная теория ассоциации была настолько сильной, что даже Эмиль Фишер, который пришел к выводу, что белки представляют собой полипептиды, образующиеся с помощью ковалентных связей между аминокислотными единицами в 1906 г., поначалу отказывались верить в существование высокомолекулярных полимеров. Штаудингер в конечном итоге получил Нобелевскую премию в 1953 году. Важно отметить, что открытие высокомолекулярных макромолекулярных полимеров ставит под сомнение универсальность разделения коллоидных фаз в биологии, несмотря на тот факт, что отдельные полимеры все еще могут связываться с помощью кластеризация и разделение фаз с образованием коллоидов, жидких кристаллов, твердых кристаллов или агрегатов.
Произошло гораздо большее влияние когда Фредерик Сэнджер определил аминокислотную последовательность инсулина и Линуса Полинга, Роберта Кори и Герман Брэнсон правильно предложил альфа-спираль и бета-лист в качестве первичных структурных мотивов во вторичной структуре белка , в то время как Макс Перуц и Джон Кендрю проанализировал трехмерную структуру миоглобина, а затем гемоглобина. Эти достижения в определении структуры белка привели к тому, что биологи в целом сосредоточили свое внимание на аминокислотной последовательности и трехмерных конформационно-специфических взаимодействиях белок-белок модель замка и ключа тип, обычно между определенным количеством взаимодействующих субъединиц в пределах стехиометрического комплекса. Вместе с Нобелевской премией Штаудингера в 1953 году этот новый подход привел к снижению интереса к биополимерам как к коллоидам в биологии, помимо их склонности к образованию твердых кристаллы для определения структуры с помощью рентгеновской кристаллографии. Тем не менее, области коллоидной химии и физики полимеров не ослабевали, чтобы охарактеризовать нестехиометрические взаимодействия, происходящие во время коллоидных, жидких кристаллов и другое фазовое поведение макромолекулярных полимеров, в частности синтетических полимеров, разработанных для промышленного применения.
 Казеин мицелл
Казеин мицелл Когда клеточные биологи в значительной степени отказались от коллоидного разделения фаз, дальнейший прогресс в этой области был предоставлен относительным посторонним - ученым-агрономам и физикам. изучение фазоразделительных биомолекул в клетках.
Начиная с начала 1970-х, Гарольд М. Фаррелл-младший из Министерства сельского хозяйства США разработал коллоидную модель разделения фаз для молока казеина. мицеллы, которые образуются в клетках молочной железы перед секрецией в виде молока.
Также в 1970-х годах физики Танака и Бенедек из Массачусетского технологического института определили поведение фазового разделения белков гамма-кристаллина из эпителиальных клеток хрусталика и катаракта в растворе, которую Бенедек назвал «конденсацией белка» .
 эпителий хрусталика, содержащий кристаллин. Справочник по физиологии (1892)
эпителий хрусталика, содержащий кристаллин. Справочник по физиологии (1892) В 1980-х и 1990-х годах Лаборатория физики полимеров Афин Дональд в Кембридже подробно описала фазовые переходы / фазовое разделение крахмала гранул из цитоплазмы растительных клеток, которые ведут себя как жидкие кристаллы.
В 1991 году Пьер-Жиль де Жен получил Нобелевскую премию по физике за разработку обобщенной теории фазовых переходов с конкретными приложениями к описанию упорядочения и фазовых переходов в полимерах. К сожалению, де Жен написал в Nature, что полимеры следует отличать от других типов коллоидов, даже если они могут демонстрировать аналогичную кластеризацию и разделение фаз поведение, позиция, которая нашла свое отражение в сокращении использования термина коллоид для описания поведения ассоциации более высокого порядка биополимеров в современной клеточной биологии и молекулярной самости. -сборка.
Достижения в конфокальной микроскопии в конце 20-го века идентифицировали белки, РНК или углеводы, локализующиеся во многих немембранно-связанных клеточных компартментах в цитоплазме или ядре, которые по-разному назывались «точки / точки», «сигналосомы ',' гранулы ',' тела ',' сборки ',' параспеклы ',' пуриносомы ',' включения ',' агрегаты 'или' фабрики '. В течение этого периода времени (1995-2008 гг.) Концепция разделения фаз была повторно заимствована из коллоидной химии физики полимеров и предложена в качестве основы для обеих цитоплазматическая и ядерная компартментализация.
С 2009 года наблюдались новые доказательства того, что биомакромолекулы претерпевают внутриклеточные фазовые переходы (разделение фаз ) во многих различных контекстах, как внутри клеток, так и в реконструированных экспериментах in vitro.
Новый термин «биомолекулярный конденсат » относится к биологическим полимерам (в отличие от синтетических полимеров ), которые подвергаются самосборке посредством кластеризации для увеличения локальной концентрации собираемых компонентов, и аналогичны физическому определению конденсации.
В физике, конденсации обычно относится к фазовому переходу газ-жидкость .
В биологии термин «конденсация» используется гораздо шире и может также относиться к жидкости-жидкости разделение фаз с образованием коллоидных эмульсий или жидких кристаллов внутри ячеек и разделение фаз жидкость-твердое с образованием гели, золи или суспензии внутри клеток, а также фазовые переходы из жидкого состояния в твердое , такие как конденсация ДНК во время профазы клеточного цикла или белковой конденсации кристаллинов в катаракте. Имея это в виду, термин «биомолекулярные конденсаты» был специально введен, чтобы отразить эту широту (см. Ниже). Поскольку биомолекулярная конденсация обычно включает олигомерные или полимерные взаимодействия между неопределенным числом компонентов, ее обычно считают отличной от образования более мелких стехиометрических белковых комплексов с определенным числом субъединиц, таких как вирусные капсиды или протеасома, хотя оба являются примерами спонтанных молекулярная самосборка или самоорганизация.
С механической точки зрения оказывается, что поливалентные взаимодействия между внутренне неупорядоченными белками (включая кросс-бета-полимеризацию) и / или белковые домены, которые индуцируют олигомерные или полимерные кластеры, могут играть роль в фазовом разделении белков.
 Формирование и примеры ядерных безмембранных компартментов
Формирование и примеры ядерных безмембранных компартментов  Динамика стрессовых гранул
Динамика стрессовых гранул Многие примеры биомолекулярных конденсатов были охарактеризованы в цитоплазме и ядре, которые, как считается, возникают в результате разделения фаз жидкость-жидкость или жидкость-твердое тело.
Другие ядерные структуры, включая гетерохроматин и конденсацию ДНК в конденсированном митозе, хромосомы образуются по аналогичным механизмам. к фазовому разделению, поэтому их также можно отнести к биомолекулярным конденсатам.
Типичные органеллы или эндосомы, заключенные в липидный бислой, не считаются биомолекулярными конденсатами. Кроме того, липидные капли окружены липидным монослоем в цитоплазме, или в молоке, или в слезах, поэтому, по-видимому, они подпадают под категорию «мембраносвязанных». Наконец, частицы секретируемого LDL и HDL липопротеина также заключены в липидный монослой. Формирование этих структур включает разделение фаз на от коллоидных мицелл или жидких кристаллов бислоев, но они не классифицируются как биомолекулярные конденсаты, поскольку этот термин зарезервирован для органелл, не связанных с мембраной.
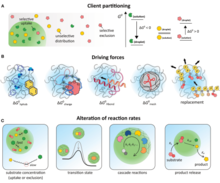 Биомолекулярное разделение
Биомолекулярное разделение Жидкость-жидкость разделение фаз (LLPS) порождает подтип коллоида, известного как эмульсия, которая может объединяться в большие капли в жидкости. Упорядочение молекул во время разделения фаз жидкость-жидкость может генерировать жидкие кристаллы, а не эмульсии. В клетках LLPS производит жидкий подкласс биомолекулярного конденсата, который может вести себя как эмульсия или жидкий кристалл.
Термин биомолекулярные конденсаты был введен в контексте внутриклеточного сборки как удобный и неисключающий термин для описания нестехиометрических сборок биомолекул. Выбор языка здесь конкретен и важен. Было высказано предположение, что многие биомолекулярные конденсаты образуются в результате разделения фаз жидкость-жидкость (LLPS) с образованием коллоидных эмульсий или жидких кристаллов в живые организмы, в отличие от жидко-твердого разделения фаз с образованием кристаллов / агрегатов в гелях, золях или суспензии внутри клеток или внеклеточных секретов. Однако однозначно продемонстрировать, что клеточное тело формируется посредством разделения фаз жидкость-жидкость, является сложной задачей, потому что в живых клетках не всегда легко различить различные состояния материала (жидкость против геля против твердого). Термин «биомолекулярный конденсат» напрямую решает эту проблему, не делая никаких предположений ни о физическом механизме, посредством которого достигается сборка, ни о материальном состоянии полученной сборки. Следовательно, клеточные тела, которые образуются в результате разделения фаз жидкость-жидкость, представляют собой подмножество биомолекулярных конденсатов, как и те, у которых физическое происхождение сборки неизвестно. Исторически сложилось так, что многие клеточные не связанные с мембраной компартменты, идентифицированные под микроскопом, подпадают под широкий круг биомолекулярных конденсатов.
В физике разделение фаз можно разделить на следующие типы коллоидов, одним из примеров которых являются биомолекулярные конденсаты:
| Среда / фаза | Дисперсная фаза | |||
|---|---|---|---|---|
| Газ | Жидкость | Твердое тело | ||
| Дисперсия. среда | Газ | Такие коллоиды не известны.. Гелий и ксенон известны как несмешивающиеся при определенных условиях. | Жидкость аэрозоль. Примеры: туман, облака, конденсация, туман, лаки для волос | Твердый аэрозоль . Примеры: дым, ледяное облако, атмосферные частицы вещество |
| Жидкость | Пена. Пример: взбитые сливки, крем для бритья, Газовые пузырьки | Эмульсия или Жидкие кристаллы. Примеры: молоко, майонез, крем для рук, латекс, биологические мембраны, мицеллы, липопротеины, шелк, жидкие биомолекулярные конденсаты | Sol или суспензия. Примеры: пигментированные чернила, осадок, осадки, агрегаты, волокна / фибриллы / нити, кристаллы, твердые биомолекулярные конденсаты | |
| твердые | твердые пены . Примеры: аэрогель, пенополистирол, пемза | гель. Примеры: агар, желатин, желе, гелеобразные биомолекулярные конденсаты | твердый золь . Пример: клюквенное стекло | |
. В биологии наиболее подходящими формами разделения фаз являются либо жидкость-жидкость, либо жидкость-твердое тело, хотя были сообщения о газовых пузырьках, окруженных фазой. разделенная белковая оболочка в цитоплазме некоторых микроорганизмов.
Одним из первых обнаруженных примеров высокодинамичного внутриклеточного жидкого биомолекулярного конденсата с четкой физиологической функцией были супрамолекулярные комплексы (Wnt сигналосомы ), образованные компонентами Wnt сигнального пути. Белок Disheveled (Dsh или Dvl) подвергается кластеризации в цитоплазме через свой домен DIX, который опосредует кластеризацию белка (полимеризацию) и фазовое разделение и важен для передачи сигнала. Белок Dsh функционирует как в плоской полярности, так и в передаче сигналов Wnt, где он рекрутирует другой супрамолекулярный комплекс (комплекс Axin) к рецепторам Wnt на плазматической мембране. Образование этих Disheveled и содержащих аксин капель законсервировано для многоклеточных животных, в том числе в клетках Drosophila, Xenopus и человека.
Другим примером жидких капель в клетках являются гранулы P зародышевой линии в Caenorhabditis elegans. Эти гранулы отделяются от цитоплазмы и образуют капли, как масло из воды. И гранулы, и окружающая цитоплазма являются жидкими в том смысле, что они текут в ответ на силы, и две гранулы могут слиться при контакте. Когда (некоторые из) молекул в гранулах исследуются (посредством восстановления флуоресценции после фотообесцвечивания ), обнаруживается, что они быстро оборачиваются в каплях, что означает, что молекулы диффундируют в гранулы и из них, как и ожидалось. в капле жидкости. Капли также могут вырастать до множества молекул в диаметре (микрометры). Исследования капель белка Caenorhabditis elegans LAF-1 in vitro также показывают поведение, подобное жидкости, с кажущейся вязкостью 