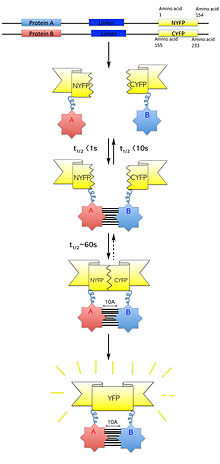
 Образование белкового комплекса с использованием BiFC. Сначала происходит взаимодействие между белком А и белком В, за которым следует повторное образование и флуоресценция флуоресцентного репортерного белка
Образование белкового комплекса с использованием BiFC. Сначала происходит взаимодействие между белком А и белком В, за которым следует повторное образование и флуоресценция флуоресцентного репортерного белка Комплементация бимолекной флуоресценции (известная как BiFC ) - это технология, обычно используемая для проверки белок взаимодействия. Он основан на ассоциации фрагментов флуоресцентного белка, которые присоединены к компонентам одного и того же макромолекулярного комплекса . Белки, предположительно взаимодействуют, сливаются снутыми комплементарными фрагментами флуоресцентного репортерного белка и экспрессируются в живых клетках. Взаимодействие этих механизмов приводит к сближению флуоресцентных фрагментов, позволяя репортерному преобразовать в свою нативную трехмерную способность и испускать свой флуоресцентный сигнал. Этот флуоресцентный сигнал может быть обнаружен и локализован в клетке с помощью инвертированного флуоресцентного микроскопа, который позволяет визуализировать флуоресценцию в клетках. Указание на более высокие уровни флуоресценции на тесные или прямые взаимодействия, а более низкие уровни флуоресценции указывают на взаимодействие внутри комплекса. Таким образом, посредством визуализации и анализа распределения флуоресценции в этих клетках можно идентифицировать местоположение, так и по взаимодействию интересующих белков.
Биохимическая комплементация впервые была описана в расщепленной субтилизином бычьей панкреатической рибонуклеазе, затем увеличена с использованием β- мутанты галактозидазы, которые позволяют клеткам расти на лактозе.
Признание способности многих белков спонтанно собираться в функциональные комплексы, а также способности фрагментов белка собираться как следствие спонтанной сборки функционального комплекса партнеров по взаимодействию, они сливаются, было позже сообщено о фрагменты убиквитина во взаимодействиях с дрожжевыми белками.
В 2000 году Ghosh et al разработали систему, позволяющую получить зеленый флуоресцентный белок (GFP ) для повторной сборки с использованием антипараллельной лейциновой молнии в клетках E. coli. Это было достигнуто путем разделения GFP на C- и N-концевые фрагменты GFP. Временной фрагмент GFP был прикреплен к каждой лейциновой застежке с помощью линкера, гетеродимеризация антипараллельной лейциновой застежки приводила к восстановленному или реформированному белку GFP, который можно было визуализировать. Успешный флуоресцентный сигнал показал, что отдельные фрагменты пептида GFP были правильно собираться и достигать третичного сворачивания. Следовательно, было постулировано, что с помощью техники фрагментированный GFP может быть использован для изучения взаимодействия пар белок-белок, когда N-C-концы находятся в непосредственной близости.
После демонстрации успешного восстановления фрагментов флуоресцентного белка в клетках млекопитающих Hu et al. описали использование фрагментированного желтого флуоресцентного белка (YFP ) в исследовании взаимодействия bZIP и семейства Rel транскрипционного фактора. Это было первое сообщение о регуляции взаимодействия с белком bZIP регионами за пределами домена bZIP, регуляции субядерной локализации доменов bZIP Fos и июнь за счет их различного взаимодействия. партнеров и модуляция активации транскрипции белковZIP и Rel посредством взаимных взаимодействий. Кроме того, это исследование было первым отчетом о методе in vivo, теперь известном как анализ комплементации бимолекулярной флуоресценции (BiFC), чтобы обеспечить понимание структурной основы образования белковых комплексов путем обнаружения флуоресценции, вызванной сборкой фрагментов флуоресцентного репортерного белка, привязанной к взаимодействующим белкам.
Активация флуорофора происходит реакция автокатали той циклизации, которая происходит после, как белок был правильно свернут. Это было продвинуто с успешным восстановлением флуорофора YFP из фрагментов белка, которые были слиты с взаимодействующими белками в течение 8 часов после трансфекции, о чем сообщалось в 2002 году.
 Рабочий процесс для BiFC
Рабочий процесс для BiFC Существуют различные системы продуцирования, которые можно использовать для полученного слитого белка. Временная экспрессия генов используется для идентификации белок-белковых взаимодействий in vivo, а также при субклеточной локализации комплекса BiFC. Однако следует проявлять осторожность во избежание чрезмерной экспрессии белка, поскольку это может исказить как предпочтительную локализацию, так и преобладающие образующиеся белковые комплексы. Вместо этого следует использовать слабые промоторы, использование низких уровней плазмидной ДНК при трансфекции и плазмидные уровни, которые не реплицируются в клетках млекопитающих, для экспрессии белков на своих эндогенных уровнях или около них, чтобы имитировать физиологические клеточные уровни. Окружающая среда. Также важен тщательный выбор флуоресцентного белка, поскольку для разных флуоресцентных белков требуется разная клеточная среда. Например, GFP можно использовать в клетках E. coli, а YFP - в клетках млекопитающих.
Стабильные клеточные линии с вектором экспрессии, интегрированным в его геном, обеспечивает более стабильные экспрессия гена в клеточной популяции, что приводит к более согласованным результатам.
При выборе места слияния линкера на поверхности необходимо выполнить три момента. Во-первых, фрагменты флуоресцентных белков имеют возможность связываться друг с другом при взаимодействии их связанных белков. Как можно отсеивать несколько комбинаций и перестановок, эта информация не является необходимой. Во-второе, создание слитого протеина не было тестом локализацию, стабильность или экспрессию белков, с помощью протеинов, связанных фрагменты, по сравнению с эндогенными белками дикого типа. Наконец, добавление слияния флуоресцентных фрагментов не должно влиять на биологическую функцию белка, что проверяется с помощью анализов, оценивающих все известные функции белков.
Линкер - это короткая аминокислотная последовательность, которая связывает фрагмент флуоресцентного репортерного белка, представляющего интересный белком, образуя гибридный белок. При разработке линкерной системы необходимо убедиться, что линкер достаточно растворим и увеличенная длина, чтобы обеспечить флуоресцентным белковым фрагментам гибкость и свободу передвижения, так что этот фрагмент и его партнерский фрагмент будут сталкиваться достаточно часто для восстановления во время взаимодействия их соответствующих слитых белков. Хотя это не задокументировано, возможно, что последовательность линкера включена на комплементацию некоторых белков. Сообщенные линкерные последовательности RSIAT и RPACKIPNDLKQKVMNH (код одиночной аминокислоты) и AAANSSIDLISVPVDSR (Sigma) были успешно использованы в экспериментах BiFC.
При разработке плазмидных векторов для экспрессии представляющих интерес белков конструкции должна обладать способностью экспрессировать белки, которые способны образовывать слитые белки с флуоресцентными фрагментами белка без нарушения функции белка. Кроме того, ожидаемый белковый комплекс должен быть в состоянии достижения стабилизации флуоресцентных белковых фрагментов, не влияя на функцию белкового комплекса или исследуемую клетку. В BiFC можно использовать многие фрагменты флуоресцентного белка, которые объединены через территорию. Как правило, рекомендуется использовать YFP в качестве репортерного белка, расщепляемого по остатку 155 (N-конец, из остатков 1–154, и C-конец, состоящий из остатков 155–238) или остаток 173, в особенно, как эти наборы фрагментов очень эффективны в их комплементации, когда они сливаются вместе с использованием белками, и они производят низкую флуоресценцию при слиянии с невзаимодействующими белками. Предполагается, что каждый белок сливается как с N-, так и с С-концевыми фрагментами флуоресцентного репортерного белка по очереди, и что эти фрагменты сливаются в каждом из N- и С-концевых концов белков-мишеней. Это позволит получить в общей сложности восемь различных перестановок с тестируемыми взаимодействми:
N-концевой фрагмент, слитый с N-концевым белком, 1 + C-концевой фрагмент, слитый с N-концевым белком 2,. N-концевой фрагмент слитый с N-концевым белком 1 + С-концевой фрагмент слит с С-концевым белком 2. N-концевой фрагмент слит с С-концевым белком 1 + С-концевой фрагмент слит с С-концевым белком 2. N- концевой фрагмент, слитый с С-концевым белком, 1 + С-концевой фрагмент, слитый с С-концевым белком 2. С-концевой фрагмент, слитый с N-концевым белком 1 + N-концевой фрагмент, слитый с N-концевой белок 2. С-концевой фрагмент, слитый с N-концевым белком 1 + N-концевой фрагмент, слитый с С-концевым белком 2. С-концевой фрагмент, слитый с С-концевым белком 1 + N -концевой фрагмент, слитый с N-концевым белком 2. С-концевой фрагмент, слитый с С-концевым белком 1 + N-концевой фрагмент, слитый с С-концевым белком 2
Как указывалось ранее, важно убедиться, что флуоресцентный репортерный белок, используемый в BiFC, является подходящим и может быть экспрессирован в системе культуры клеток по выбору, поскольку все репортерные белки могут флуоресцировать или визуализироваться во всех модельных систем.
Фрагменты флуоресцентного белка могут связываться и флуоресцировать с низкой эффективностью в отсутствие специфического взаимодействия. Следовательно, важно включить контроли, чтобы убедиться, что флуоресценция от восстановления флуоресцентного репортерного белка не вызвана неспецифическим контактом.
Некоторые контроли включают фрагменты флуорофоров, связанные с невзаимодействующими белками, присутствие этих слияний имеет тенденцию к снижению неспецифической комплементации и ложноположительных результатов.
Другой контроль посредством пути связывания фрагментаоресцентного белка с белками с мутированными гранями взаимодействия. Пока флуоресцентный фрагмент слит с мутировавшими белками таким же образом, как и белок дикого типа, и мутация не влияет на уровни экспрессии и локализацию гена, это служит сильным отрицательным фактором, поскольку мутантные белки и, следовательно, флуоресцентные фрагменты не влияют на уровни экспрессии и локализацию гена. должны взаимодействовать друг с другом.
Внутренний контроль также необходим для соблюдения различий в эффективности трансфекции и экспрессии генов в разных клетках. Это достигается путем котрансфекции клеток плазмидами, кодирующими интересующие слитые белки, а также целым (нефрагментированным) белком, который флуоресцирует на длине волны, отличной от длины волны флуоресцентного репортерного белка. Во время визуализации определения интенсивности флуоресценции комплекса BiFC и контроля, который после вычитания фонового сигнала становится новым. Это соотношение представляет эффективность BiFC и может сравниваться с другими соотношениями для определения относительной эффективности образования различных комплексов.
Разработаны и созданы системы доставки плазмиды трансфицированные в исследуемые клетки. После трансфекции необходимо подождать, как правило, около восьми часов, чтобы слитые белки использовали и их фрагменты флуоресцентного репортерного белка ассоциировались и флуоресцируют.
После достаточного когда слитые белки и связанные с ними флуоресцентные фрагменты взаимодействуют и флуоресцируют, клетки можно наблюдать под инвертированным флуоресцентным микроскопом, который может визуализировать флуоресценцию в клетках. Интенсивность флуоресценции комплексов BiFC обычно составляет <10% of that produced by expression of intact fluorescent proteins, the extremely low аутофлуоресценцию в видимом диапазоне, большая часть клеток часто делает сигнал BiFC на порядки выше, чем фоновая флуоресценция.
Если флуоресценция обнаруживается, когда слитые белки экспрессируются, но отсутствуют или значительно снижены после экспрессии мутировавшего отрицательного контроля, вероятно, что специфическое взаимодействие происходит между двумя интересующими белками-мишенями. Однако, вероятно, вызвана неспецифическими взаимодействми белков, поэтому следует протестировать другую комбинацию конформаций гибридного белка.
Если флуоресценция не обнаружена, то взаимодействие между интересующими белками все еще может существовать, поскольку создание гибридного белка может изменить или поверхность взаимодействия целевого белка, или фрагменты флуоресценции могут быть связаны с физически неспособны ассоциировать. Чтобы этот результат не являлся ложноотрицательным, что нет взаимодействия, взаимодействие белков должно быть проверено в ситуации, когда для комплементации и активации флуоресценции требуется внешний сигнал. В этом случае, если внешний сигнал не может вызвать ассоциацииоресцентных фрагментов, вероятно, что белки не связаны или существует физическое препятствие для комплементации флуоресценции.
Белки взаимодействуют с различными белками-связками и другими макромолекулами для достижения функций, которые включают различные функции в клетках, которые включают выживание организма. Идентификация этих взаимодействий может дать ключ к разгадке их влияния на клеточные процессы. Исследование этих физиий in vivo и на эндогенных уровнях, рекомендуется в BiFC, обеспечивает релевантный контекст, из которого можно сделать выводы о взаимодействиях белков.
BiFC позволяет напрямую визуализировать белковые взаимодействия в живых клетках с ограниченным клеточным возмущением, вместо того, чтобы полагаться на вторичные эффекты или окрашивание экзогенным молекулы, которые могут не распределяться равномерно. Это, а также возможность наблюдать за живыми клетками в течение длительных периодов времени, стали возможными благодаря сильной собственной флуоресценции восстановленного репортерного белка, что снижает вероятность неправильного считывания, связанного с процессом выделения белка.
В отличие от многих анализов взаимодействия белков in vivo, BiFC не требует, чтобы белковые комплексы были образованы большой долей белков или в стехиометрических пропорциях. Вместо этого BiFC может обнаруживать взаимодействия между белками субпопуляциями, слабые взаимодействия и белки с низкой экспрессией из-за стабильной комплементации флуоресцентного репортерного белка. Кроме того, сообщалось об успешном восстановлении флуоресцентного белка для белков-партнеров, находящихся на расстоянии более 7 нм друг от друга, при условии, что линкеры, связывающие фрагмент флуорофора с представляющим интерес белком, обладают гибкостью, необходимой для связывания с его соответствующим фрагментом. Кроме того, сила белкового взаимодействия может быть количественно определена по изменению силы флуоресцентного сигнала.
BiFC позволяет измерять пространственные и временные изменения в белковых комплексах, даже в ответ на активацию и ингибирование лекарств и субклеточно, обеспечивая наивысшее пространственное разрешение анализов белок-белкового взаимодействия in vivo.
BiFC не требует специального оборудования, поскольку визуализация возможно с инвертированным флуоресцентным микроскопом, который может обнаруживать флуоресценцию в клетках. Кроме того, анализ не требует сложной обработки данных или корректировки других источников флуоресценции.
BiFC может быть выполнен без структурной информации о партнерах по взаимодействию, если Фрагменты флуоресцентного репортерного белка могут ассоциироваться внутри комплекса, так как можно проводить скрининг множественных комбинаций слитых белков. Это связано с предположением, что, поскольку функции белка повторяются в контексте in vivo, сложная структура будет напоминать структуру интактных белков, видимых физиологически.
Технология BiFC был усовершенствован и расширен, чтобы включить возможности одновременно визуализировать множественные белковые комплексы в одной и той же клетке, взаимодействия РНК / белок, чтобы быстро обнаруживать изменения в путях трансдукции генов, демонстрировать скрытые фенотипы лекарственных препаратов, при которых прогнозируемый результат лечения (т.е. гибель клеток, дифференцировка, морфологические изменения) не наблюдается in vivo, изучить образование комплексов в различных клеточных отсеков и для отображения поверхностей взаимодействия с белками
Флуоресцентный сигнал вырабатывается только после взаимодействия белков, что обычно порядок часов. Следовательно, BiFC не может обеспечить обнаружение белковых взаимодействий в реальном времени. Задержка химических реакций с образованием флуорофора может также влиять на динамику диссоциации комплекса и обмена партнерами.
Образование комплекса BiFC является только обратимым на начальном этапе повторной сборки флуоресцентного репортерного белка, как правило, порядка миллисекунд. После воссоздания флуорохрома in vitro он становится практически необратимым. Это предотвращает взаимодействие белков с другими и может нарушить ассоциацию / диссоциацию белковых комплексов в динамическом равновесии.
Флуоресцентныефрагменты белка имеют ограниченную способность связываться независимо от белков. к которому они сливаются. Независимо от того, что независимая ассоциация считает, что независимые протеины и уровни их экспрессии. Как правило, это ограничивается смягчающими, гарантирующими, что интересующие слитые белки экспресс в эндогенных условиях.
Связывание флуоресцентных фрагментов может изменить укладку или протеину. Представляет интерес, что приводит к удалению сайта связывания взаимодействующего белка на поверхности. Кроме расположения флуоресцентных фрагментов, может быть уменьшена гибкость для связывания флуоресцентных фрагментов, препятствующих восстановлению флуорофора посредством стерического препятствия. Следовательно, отсутствие комплементации флуоресценции может быть ложноотрицательным и не обязательно доказывает, что рассматриваемое взаимодействие не происходит.
Из-за потребности в молекулярном кислороде для образования флуорофора BiFC нельзя использовать для облигатных анаэробов, которые не могут выжить в присутствии кислорода. Это ограничивает использование BiFC аэробными организмами.
Автофлуоресценция обычно не является проблемой, поскольку сигнал BiFC будет намного выше фонового. Однако некоторые организмы, особенно apicomplexa, имеют более высокую автофлуоресценцию, что затрудняет нанесение на них BiFC. Некоторые грибы, такие как Candida albicans, также имеют высокий автофлуоресцентный фон, но BiFC часто все же можно проводить при использовании надлежащих контролей и штаммов.
типа эндогенные белки дикого типа невозможно визуализировать in vivo, необходимо создать гибридные белки и трансфицировать их плазмиды в исследуемые клетки. Эти слитые белки могут не повторять функции, локализацию и взаимодействие, общие для их аналогов дикого типа, некие картину рассматриваемых белков. Эту проблему можно облегчить, используя структурную информацию и расположение сайтов для определения уровня знаний сайтов с использованием соответствующих контроли и уровни экспрессии и функции слитых белков и белков дикого типа с помощью вестерн-блоттинга и функционального анализа.
Хотя низкие температуры способствуют восстановлению флуоресценции, когда фрагменты находятся в пределах близости, это может влиять на поведение целевых белков, приводя к неточным выводам природы взаимодействия белков и их взаимодействующие партнеры.
«Временное восстановление флуорофора» может происходить на расстоянии 7 нм или более, комплементация флуоресценции может указывать на прямую или косвенную (т.е. в пределах одного комплекса) взаимодействие между слитыми белками флуоресцентных фрагментов.
В дополнение к валидации белка - pr При описанных выше взаимодействиях белков BiFC был расширен и адаптирован для других приложений:
Система BiFC применлась для регистрации событий биогенеза рибосом в E.coli. Процесс сборки рибосом включает зарождение рибосомных белков в правильном порядке и ориентации. Нарушения сборки приводят к структурным дефектам в субъединицах рибосом, которые в результате не могут соединяться в правильной ориентации с образованием полностью функциональных рибосом. Таким образом, события присоединения субъединиц, сигнализируемое создание BiFC, единый способ мониторинга биогенеза рибосом в отличие от трудоемких методов профилирования полисом.
Флуоресцентные белковые фрагменты, используемые в BiFC, были расширены, чтобы включить цвета: синий, голубой, зеленый, желтый, красный, вишневый и Венеры. Эта цветовая гамма сделала возможной комплемент анализа многоцветной флуоресценции. Этот метод позволяет одновременно визуализировать несколько белковых комплексов в одной и той же клетке. Кроме того, белки обычно имеют большое количество альтернативных партнеров по взаимодействию. Таким образом, путем слияния фрагментов различных флуоресцентных белков с белками-кандидатами можно изучить конкуренцию между другими группами по взаимодействию за образование комплекса посредством комплементации различных флуоресцентных цветных фрагментов.
BiFC был расширен, чтобы включить взаимодействие РНК-связывающих белков в методе Рэкхема и Брауна, описанных как комплементация тримолекулярной флуоресценции (TriFC). В этом методе фрагмент флуоресцентного белка Венеры сливается с мРНК, представляющей интерес, и комплементарный участок Венеры сливается с РНК-связывающим белком, представляющим интерес. Подобно BiFC, если мРНК и белок взаимодействуют, Венеры восстанавливает и флуоресцирует. Это позволяет легко обнаруживать и локализовать взаимодействия РНК-белок в живой клетке и обеспечивает простой метод обнаружения прямая или непрямая ассоциация РНК-белок (т. е. внутри комплекса), которая может быть проверена с помощью анализа очищенных соединений in vitro или РНКи нокдауна мостиковой молекулы (молекулы).
BiFC можно использовать для связывания генов друг с другом и их функциями измерения взаимодействий между белками, которые кодируют гены. Это приложение идеально подходит для новых генов, поскольку известно их мало что об их восходящих и нижестоящих эффекторах, поскольку установлены новые связи путей. Кроме того, влияние лекарств, гормонов или делеции или нокдауна интересующего гена, а также последующие эффекты как на силу межбелковых взаимодействий, так и на взаимодействие можно наблюдать в течение нескольких секунд.
BiFC был использован для изучения ядерной транслокации через комплексную локализацию, а также взаимодействий, включающих интегральные мембранные белки. Таким образом, BiFC является важным инструментом для понимания локализации транскрипционного фактора в субклеточных компартментах.
BiFC сочетается с проточной цитометрией (BiFC-FC). Это позволяет реализовать модель взаимодействия посредством введения сайт-направленных или случайных мутаций, влияющих на совокупность.
Используется другие методы для изучения межбелковых полагий на методы in vitro. К сожалению, изучение белков в искусственной системе за пределами клеточного окружения сопряжено рядом трудностей. Например, для этого может потребоваться удаление белков из их нормального клеточного окружения. Обработка, необходимая для выделения белка, может повлиять на его взаимодействие с другими белками. Кроме того, выделение белка из внутриклеточной передачи сигналов и механизмов, которые происходят в нормальной клетке, может дать неверную картину внутриклеточных и физиологических явлений. Кроме того, белки, изученные in vitro, могут быть изучены при помощи клеток, отличных от их нормального уровня содержания, которые могут быть недостаточно эффективными для функционирования в геноме хозяина. Наконец, изучая белки in vitro, определить влияние специфических белок-белковых взаимодействий в клетке функциональные или физиологические последствия.
Другие анализы in vivo, наиболее часто используемых для изучения межбел взаимодействий, включая резонансный перенос энергии флуоресценции (FRET ) и дрожжевой двугибридный (Y2H ) анализ. Каждый из этих анализов имеет свои преимущества по сравнению с BiFC:
резонансный перенос энергии флуоресценции (FRET ), также известный как резонансный перенос энергии Фёрстера, резонансный перенос энергии (RET ) или электронный перенос энергии (EET ) - это на основе передачи энергии от возбужденного (донора ) хромофора или флуорофора (если хромофоры флуоресцентные) к ближайшему акцептору. В методе флуорофоры химически связаны или генетически слиты с двумя белками, предположительно связаны. Это приводит к тому, что флуорофоры взаимодействуют в непосредственной близости друг от друга. Когда флуорофоры ориентированы таким образом, чтобы они открывали друг другу флуорофоры, это обычно обеспечивается при проектировании и конструировании связи / слияния флуорофор-белок, то передача энергии от возбужденного донорного флуорофора приводит к изменению в силе флуоресценции или времени жизни флуорофоров.
дрожжевой двугибридный (Y2H ) представляет собой метод генетического скрининга, который можно использовать для обнаружения физических (связывающих) взаимодействий белок-белок или белок-ДНК. Обычно он применяется в модельном дрожжевом организме Saccharomyces cerevisiae. Он использует функцию белок-приманку с (неизвестной) функцией, которая слит, например, с доменом связывания фактора транскрипции GAL4 против сдерживающих белков или библиотеки кДНК, которые экспрессируют, например, Домен активации GAL4 («жертва»).
| Технология сравнения | Сходство с BiFC | Преимущества | Недостатки | |
|---|---|---|---|---|
| FRET | Способность обнаруживать и определять местонахождение сайтов взаимодействия в живых клетках | Мгновенный мониторинг белковых взаимодействий в реальном времени
Обратное взаимодействие флуорофора
| Близкое пространственное соседство
Пониженная чувствительность
Необратимое фотообесцвечивание
|  FRET: взаимодействие между белком A и белком B сводит два флуоресцентных белка вместе, и происходит передача энергии между двумя флуоресцентными белками. FRET: взаимодействие между белком A и белком B сводит два флуоресцентных белка вместе, и происходит передача энергии между двумя флуоресцентными белками. |
| Y2H | Метод in vivo, используемый для скрининга взаимодействий | Генетический скрининг взаимодействий
| Предполагаемая связь между приманкой и добычей
Ошибочная активация транскрипции
Генетическая комплементация
Дрожжи как модельный организм
Сверхэкспрессия белков
Ядерная локализация
|  Дрожжевой-2-гибрид: взаимодействие между белком А и белком B активирует транскрипцию Дрожжевой-2-гибрид: взаимодействие между белком А и белком B активирует транскрипцию |