В органической химии деформация кольца - это тип нестабильности, которая существует в молекуле образуют аномальные углы. Деформация чаще всего обсуждается для небольших колец, таких как циклопропаны и циклобутаны, внутренние углы которых существенно меньше идеализированного значения приблизительно 109 °. Из-за их высокой деформации теплота сгорания для этих небольших колец повышена.
Деформация кольца возникает в результате комбинации угловой деформации, конформационной деформации или Штамм Питцера (торсионное затмевающее взаимодействие) и трансаннулярный штамм, также известный как штамм Ван-дер-Ваальса или штамм Прелога. Простейшими примерами угловой деформации являются небольшие циклоалканы, такие как циклопропан и циклобутан.
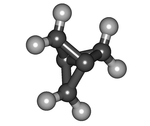 1.1.1-Пропеллан (C2(CH 2)3) - одна из наиболее напряженных известных молекул.
1.1.1-Пропеллан (C2(CH 2)3) - одна из наиболее напряженных известных молекул. В алканах, оптимум перекрытие атомных орбиталей достигается при 109,5 °. Наиболее распространенные циклические соединения имеют пять или шесть атомов углерода в своем кольце. Адольф фон Байер получил Нобелевскую премию в 1905 году за открытие теории деформации Байера, которая была объяснением относительная стабильность циклических молекул в 1885 году.
Угловая деформация возникает, когда валентные углы отклоняются от идеальных валентных углов для достижения максимальной прочности связи в конкретной химической конформации. Угловая деформация обычно влияет на циклические молекулы, которым не хватает гибкости ациклических молекул.
Угловая деформация дестабилизирует молекулу, что проявляется в более высокой реакционной способности и повышенной теплоте сгорания. Максимальная прочность связи достигается за счет эффективного перекрытия атомных орбиталей в химической связи. Количественным показателем угловой деформации является энергия деформации. Угловая деформация и скручивающая деформация вместе создают кольцевую деформацию, которая влияет на циклические молекулы.
Нормализованные значения энергии, которые позволяют сравнивать деформации кольца, получают путем измерения на метиленовую группу (CH 2) молярной теплоты сгорания. в циклоалканах.
Значение 658,6 кДж на моль получается из недеформированного длинноцепочечного алкана.
| Размер кольца | Энергия деформации (ккал / моль) | Размер кольца | Энергия деформации (ккал / моль) | |
|---|---|---|---|---|
| 3 | 27,5 | 10 | 12,4 | |
| 4 | 26,3 | 11 | 11,3 | |
| 5 | 6,2 | 12 | 4,1 | |
| 6 | 0,1 | 13 | 5,2 | |
| 7 | 6,2 | 14 | 1,9 | |
| 8 | 9,7 | 15 | 1,9 | |
| 9 | 12,6 | 16 | 2,0 |
Циклические алкены подвержены деформации, возникающей в результате деформации sp -гибридизированный углеродный цент ters. Иллюстративным является C60, где углеродные центры пирамидализированы. Это искажение увеличивает реакционную способность этой молекулы. Угловая деформация также является основой правила Бредта, которое диктует, что углеродные центры-мосты не включаются в алкены, поскольку образующийся алкен будет подвергаться экстремальной угловой деформации.
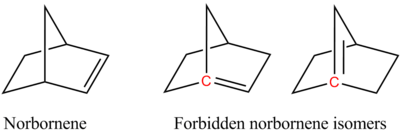 Правило Бредта, которое указывает, что алкены редко включают углеродные центры плацдарма. Это правило является следствием угловой деформации.
Правило Бредта, которое указывает, что алкены редко включают углеродные центры плацдарма. Это правило является следствием угловой деформации. В циклоалканах каждый углерод неполярно ковалентно связан с двумя атомами углерода и двумя водородом. Углероды имеют sp-гибризацию и должны иметь идеальные валентные углы 109,5 °. Однако из-за ограничений циклической структуры идеальный угол достигается только в шестиуглеродном кольце - циклогексан в конформации кресло. Для других циклоалканов валентные углы отклоняются от идеальных.
Молекулы с высокой степенью кольцевой деформации состоят из трех, четырех и некоторых пятичленных циклов, включая: циклопропаны, циклопропены, циклобутаны, циклобутены, [1,1,1] пропелланы, [2,2,2] пропелланы, эпоксиды, азиридины, циклопентены и норборнены. Эти молекулы имеют валентные углы между кольцевыми атомами, которые являются более острыми, чем оптимальные тетраэдрические (109,5 °) и тригональные плоские (120 °) валентные углы, требуемые их соответствующими sp- и sp-связями. Из-за меньших углов связи связи имеют более высокую энергию и принимают более p-характер, чтобы уменьшить энергию связей. Кроме того, кольцевые структуры циклопропанов / енов и циклобутанов / енов обладают очень небольшой конформационной гибкостью. Таким образом, заместители в кольцевых атомах существуют в закрытой конформации в циклопропанах и между гош и закрытой в циклобутанах, способствуя более высокой энергии деформации кольца в форме ван-дер-ваальсова отталкивания.
кольцевая деформация может быть значительно выше в бициклических системах. Например, бициклобутан, C 4H6, известен как одно из наиболее напряженных соединений, которые можно выделить в больших количествах; его энергия деформации оценивается в 63,9 ккал · моль (267 кДж · моль).
Потенциальная энергия и уникальная структура связи, содержащаяся в связях молекул с кольцевой деформацией, может использоваться для запуска реакций в органическом синтезе. Примерами таких реакций являются метатезис-полимеризация с раскрытием кольца, фотоиндуцированное раскрытие цикла циклобутенов и нуклеофильное раскрытие цикла эпоксидов и азиридины.