 S-аденозилметионин, источник метильных групп во многих биогенных соединениях мышьяка
S-аденозилметионин, источник метильных групп во многих биогенных соединениях мышьяка Биохимия мышьяка относится к биохимические процессы, в которых можно использовать мышьяк или его соединения, такие как арсенат. Мышьяк является элементом с умеренным содержанием в земной коре, и хотя многие соединения мышьяка часто считаются высокотоксичными для большинства живых организмов, производится большое количество мышьяковоорганических соединений биологически и различные органические и неорганические соединения мышьяка метаболизируются многочисленными организмами. Этот шаблон является общим для других связанных элементов, включая селен, который может проявлять как положительные, так и вредные эффекты. Биохимия мышьяка стала актуальной, поскольку многие токсичные соединения мышьяка обнаружены в некоторых водоносных горизонтах, потенциально влияя на многие миллионы людей посредством биохимических процессов.
 Отравление мышьяком является глобальной проблемой, возникающей из-за встречающегося в природе мышьяка в грунтовые воды.
Отравление мышьяком является глобальной проблемой, возникающей из-за встречающегося в природе мышьяка в грунтовые воды. Доказательства того, что мышьяк может быть полезным питательным веществом при t уровень расы ниже фона, которому обычно подвергаются живые организмы. Некоторые органические соединения мышьяка, встречающиеся в природе, - это арсенобетаин и арсенохолин, которые содержатся во многих морских организмах. Также известны некоторые As-содержащие нуклеозиды (производные сахаров). Некоторые из этих мышьякоорганических соединений возникают в результате процессов метилирования. Например, плесень Scopulariopsis brevicaulis вырабатывает значительные количества триметиларсина, если присутствует неорганический мышьяк. Органическое соединение арсенобетаин содержится в некоторых морских продуктах, таких как рыба и водоросли, а также в грибах в больших концентрациях. В чистой окружающей среде съедобные виды грибов Cyanoboletus pulverulentus гипераккумулируют мышьяк в концентрациях, достигающих даже 1300 мг / кг в сухом весе; какодиловая кислота является основным соединением As. Очень необычный состав мышьяковоорганических соединений был обнаружен в оленьих трюфелях (Elaphomyces spp.). В среднем человек получает около 10–50 мкг / день. Значения около 1000 мкг не являются необычными после употребления в пищу рыбы или грибов; однако есть небольшая опасность в употреблении в пищу рыбы, поскольку это соединение мышьяка почти нетоксично.
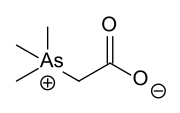
Арсенобетаин, одно из наиболее распространенных соединений мышьяка в природе. Также обычным является арсенохолин, который имеет CH 2 OH вместо CO 2 H).

Триметиларсин, продуцируемый микробным действием на арсенат пигменты

содержащие мышьяк производные рибозы (R = несколько групп)
Местный источник мышьяк - зеленые пигменты, когда-то популярные в обоях, например Парижский зеленый. Это соединение обвиняют в различных заболеваниях, хотя его токсичность преувеличена.
Триметиларсин, когда-то известный как газ Гозио, представляет собой мышьякорганическое соединение с сильным зловонным запахом, которое обычно вырабатывается микробами на неорганических субстратах мышьяка. 184>
Соединения мышьяка (V) легко восстанавливаются до мышьяка (III) и могли служить акцептором электронов на исконной Земле. Озера, содержащие значительное количество растворенного неорганического мышьяка, содержат толерантную к мышьяку биоту.
Хотя фосфат и арсенат структурно схожи, нет доказательства того, что мышьяк заменяет фосфор в ДНК или РНК. Эксперимент 2010 года с участием бактерий GFAJ-1, который сделал это заявление, был опровергнут к 2012 году.
Антропогенные (искусственные) источники мышьяка, такие как Естественными источниками являются в основном оксиды мышьяка и связанные с ними анионы. Искусственные источники мышьяка включают отходы переработки полезных ископаемых, свиноводческих и птицеводческих хозяйств. Например, многие руды, особенно сульфидные минералы, загрязнены мышьяком, который выделяется при обжиге (горении на воздухе). При такой обработке арсенид превращается в триоксид мышьяка, который является летучим при высоких температурах и выбрасывается в атмосферу. Птицефабрики и свиноводства широко используют мышьякорганическое соединение роксарсон в качестве антибиотика в кормах. Некоторая древесина обрабатывается арсенатом меди в качестве консерванта. Механизмы воздействия этих источников на живые организмы «ниже по течению» остаются неопределенными, но, вероятно, разнообразны. Один из часто упоминаемых путей включает метилирование.
Монометилированная кислота, метаноарзоновая кислота (CH 3 AsO (OH) 2), является предшественником фунгицидов (торговое название Неоазозин) в выращивание риса и хлопка. Производные фениларсоновой кислоты (C6H5AsO (OH) 2) используются в качестве кормовых добавок для скота, в том числе 4-гидрокси-3-нитробензоларсоновая кислота (3-NHPAA или Роксарсон), уреидофениларсоновую кислоту и п-арсаниловую кислоту. Эти приложения вызывают споры, поскольку они вводят растворимые формы мышьяка в окружающую среду.
Несмотря на или, возможно, из-за своей давно известной токсичности, зелья и лекарства, содержащие мышьяк, имеют историю медицины и шарлатанство, которое продолжается в 21 веке. Начиная с начала 19 века и вплоть до 20 века, продавался раствор Фаулера, токсичная смесь арсенита натрия. Мышьякоорганическое соединение сальварсан было первым синтетическим химиотерапевтическим средством, открытым Полем Эрлихом. Однако лечение привело ко многим проблемам, вызывающим длительные осложнения для здоровья. Примерно в 1943 году его окончательно вытеснили пенициллин. Родственный препарат Меларсопрол все еще используется против позднего состояния африканского трипаносомоза (сонная болезнь), несмотря на его высокую токсичность и, возможно, смертельные побочные эффекты.
Триоксид мышьяка (As 2O3) подавляет рост клеток и вызывает апоптоз (запрограммированную гибель клеток) в некоторых типах раковых клеток, которые обычно бессмертны и могут неограниченно размножаться. В сочетании с полностью транс-ретиноевой кислотой он одобрен FDA в качестве лечения первой линии для промиелоцитарной лейкемии.
Неорганический мышьяк и его соединения, при попадая в пищевую цепь, постепенно метаболизируются (детоксифицируются) в процессе метилирования. Метилирование происходит через чередующиеся реакции восстановительного и окислительного метилирования, то есть восстановление пятивалентного мышьяка до трехвалентного с последующим добавлением метильной группы (CH 3).
 Какодиловая кислота, образующаяся в печени после приема внутрь мышьяка.
Какодиловая кислота, образующаяся в печени после приема внутрь мышьяка. У млекопитающих метилирование происходит в печени с помощью метилтрансфераз, причем продуктами являются (CH 3)2AsOH () и (CH 3)2As (O) OH () диметиларсиновая кислота ), которые имеют степени окисления As (III) и As (V), соответственно. Хотя механизм метилирования мышьяка у человека не выяснен, источником метил является метионин, что предполагает роль S-аденозилметионина. Воздействие токсичных доз начинается, когда способность печени к метилированию превышена или подавлена.
Существуют две основные формы мышьяк, который может попадать в организм, мышьяк (III) и мышьяк (V). Мышьяк (III) проникает в клетки через аквапорины 7 и 9, которые являются разновидностью акваглицеропорина. Ars Соединения enic (V) используют переносчики фосфата для проникновения в клетки. Мышьяк (V) может быть превращен в мышьяк (III) ферментом пуриновой нуклеозидфосфорилазой. Это классифицируется как стадия биоактивации, поскольку, хотя мышьяк (III) более токсичен, он более легко метилируется.
Существует два пути метилирования неорганических соединений мышьяка. Первый способ использует метилтрансферазу мышьяка Cyt19 для метилирования мышьяка (III) до монометилированного соединения мышьяка (V). Затем это соединение превращают в монометилированное соединение мышьяка (III) с использованием глутатион-S-трансферазы омега-1 (GSTO1 ). Монометилированное соединение мышьяка (V) затем может быть снова метилировано метилтрансферазой мышьяка Cyt19, которая образует соединение диметил мышьяка (V), которое может быть преобразовано в соединение диметил мышьяка (III) с помощью глутатион S-трансферазы Омега-1 ( GTSO1). Другой путь использует глутатион (GSH) для конъюгирования с мышьяком (III) с образованием комплекса мышьяка (GS) 3. Этот комплекс может образовывать монометилированный комплекс GS мышьяка (III) с использованием Cyt19 метилтрансферазы мышьяка, и этот монометилированный комплекс GS находится в равновесии с монометилированным мышьяком (III). Cyt19 метилтрансфераза мышьяка может метилировать комплекс еще раз, и это образует диметилированный комплекс GS мышьяка, который находится в равновесии с комплексом диметил мышьяка (III). И монометилированные, и диметилированные соединения мышьяка легко выводятся с мочой. Однако было показано, что монометилированное соединение более реактивно и более токсично, чем неорганические соединения мышьяка, для гепатоцитов человека (печень), кератиноцитов в коже и эпителиальных клеток бронхов (легкие).
Исследования на экспериментальных животных и людях показывают, что как неорганический мышьяк, так и метилированные метаболиты проникают через плаценту к плоду, однако есть свидетельства того, что метилирование усиливается во время беременности и может быть очень защищает развивающийся организм.
Ферментативное метилирование мышьяка - это процесс детоксикации; он может быть метилирован до метиларсенита, диметиларсенита или триметиларсенита, все из которых являются трехвалентными. Метилирование у млекопитающих катализируется метилтрансферазой мышьяка (AS3MT), которая переносит метильную группу на кофакторе S-аденометионин (SAM) в мышьяк (III). Ортолог AS3MT обнаружен у бактерий и называется CmArsM. Этот фермент был протестирован в трех состояниях (без лиганда, связанный мышьяк (III) и связанный с SAM). В сайтах связывания мышьяка (III) обычно используются тиоловые группы остатков цистеина. В катализе участвуют тиолаты Cys72, Cys174 и Cys224. В реакции SN2 положительный заряд на атоме серы SAM оттягивает связывающий электрон от углерода метильной группы, который взаимодействует с неподеленной парой мышьяка с образованием связи As-C, оставляя SAH.
У людей основной путь выведения большинства соединений мышьяка - через мочу. Биологический период полураспада неорганического мышьяка составляет около 4 дней, но после воздействия арсената он немного короче, чем после воздействия арсенита. Основные метаболиты, выделяемые с мочой людей, подвергшихся воздействию неорганического мышьяка, - это моно- и диметилированная мышьяковая кислота, а также некоторое количество неметаболизированного неорганического мышьяка.
Биотрансформация мышьяка для выведения из организма в основном осуществляется посредством ядерный фактор, связанный с эритроидом 2, фактор 2 (Nrf2 ) путь. В нормальных условиях Nrf2 связан с Kelch-подобным ECH ассоциированным белком 1 (Keap1 ) в его неактивной форме. По мере поглощения мышьяка клетками и последующих реакций, которые приводят к производству активных форм кислорода (ROS), Nrf2 расщепляется и становится активным. Keap1 имеет реактивные тиоловые фрагменты, которые связывают ROS или электрофильные формы мышьяка, такие как монометиллированный мышьяк (III), и индуцирует высвобождение Nrf2, который затем перемещается через цитоплазму к ядру. Затем Nrf2 активирует антиоксидантный чувствительный элемент (ARE), а также электрофильный чувствительный элемент (EpRE), оба из которых способствуют увеличению антиоксидантных белков. Особо следует отметить в этих антиоксидантных белках гемоксигеназу 1 ([HO-1]), NAD (P) H-хинон оксидоредуктазу 1 (NQO1) и γ-глутамилцистеинсинтазу (γGCS), которые работают вместе для уменьшения окислительных форм, таких как как перекись водорода для уменьшения окислительного стресса клетки. Повышение γGCS вызывает повышенное производство арсенит-триглутатионина (As (SG) 3), важного аддукта, который поглощается либо множественным лекарственным белком 1 или 2 (MRP1 или MRP2 ), который выводит мышьяк из клетки в желчь для выведения. Этот аддукт также может разлагаться обратно на неорганический мышьяк.
Особо следует отметить при экскреции мышьяка многочисленные этапы метилирования, которые могут увеличить токсичность мышьяка, поскольку MMeAsIII является мощным ингибитором глутатионпероксидазы, глутатионредуктазы, пирувата. дегидрогеназа и тиоредоксинредуктаза.
Мышьяк является причиной смертности во всем мире; сопутствующие проблемы включают болезни сердца, дыхательных путей, желудочно-кишечного тракта, печени, нервной системы и почек.
Мышьяк влияет на долголетие клеток за счет аллостерического ингибирования важного метаболического фермента пируватдегидрогеназы ( PDH), который катализирует окисление пирувата до ацетил-CoA с помощью NAD. При ингибировании фермента энергетическая система клетки нарушается, что приводит к эпизоду клеточного апоптоза. Биохимически мышьяк препятствует использованию тиамина, что приводит к клинической картине, напоминающей дефицит тиамина. Отравление мышьяком может повысить уровень лактата и привести к лактоацидозу.
Генотоксичность включает ингибирование репарации ДНК и метилирования ДНК. канцерогенный эффект мышьяка возникает в результате окислительного стресса, вызванного мышьяком. Высокая токсичность мышьяка естественным образом привела к разработке различных соединений мышьяка в качестве химического оружия, например диметиларшьяк хлорид. Некоторые из них использовались как боевые отравляющие вещества, особенно в Первой мировой войне. Эта угроза привела к многочисленным исследованиям противоядий и к расширению знаний о взаимодействии соединений мышьяка с живыми организмами. Одним из результатов была разработка таких антидотов, как британский анти-люизит. Многие из таких антидотов используют сродство As (III) к тиолатным лигандам, которые превращают высокотоксичные органо-мышьяковые соединения в менее токсичные производные. Обычно предполагается, что арсенаты связываются с остатками цистеина в белках.
Напротив, оксид мышьяка является одобренным и эффективным химиотерапевтическим препаратом для лечения острого промиелоцитарного лейкоза (APL).
Благодаря схожей структуре и свойствам пятивалентные метаболиты мышьяка способны заменять фосфатную группу многих метаболических путей. Замена фосфата арсенатом начинается, когда арсенат вступает в реакцию с глюкозой и глюконатом in vitro. Эта реакция генерирует глюкозо-6-арсенат и 6-арсеноглюконат, которые действуют как аналоги глюкозо-6-фосфата и 6-фосфоглюконата. На уровне субстрата во время гликолиза глюкозо-6-арсенат связывается в качестве субстрата с глюкозо-6-фосфатдегидрогеназой, а также ингибирует гексокиназу посредством отрицательной обратной связи. В отличие от важности фосфата в гликолизе, присутствие арсената ограничивает образование АТФ за счет образования нестабильного ангидридного продукта в результате реакции с D-глицеральдегид-3-фосфатом. Образовавшийся ангидрид 1-арсенато-3-фосфо-D-глицерат легко гидролизуется из-за большей длины связи As-O по сравнению с P-O. На митохондриальном уровне арсенат разъединяет синтез АТФ за счет связывания с АДФ в присутствии сукцината, таким образом образуя нестабильное соединение, что в конечном итоге приводит к снижению чистого прироста АТФ. С другой стороны, метаболиты арсенита (III) имеют ограниченное влияние на производство АТФ в красных кровяных тельцах.
Ферменты и рецепторы, содержащие тиол или сульфгидрил функциональные группы активно нацелены на метаболиты арсенита (III). Эти серосодержащие соединения обычно представляют собой глутатион и аминокислоту цистеин. Производные арсенита обычно имеют более высокое сродство к связыванию по сравнению с метаболитами арсената. Эти связывания ограничивают активность определенных метаболических путей. Например, пируватдегидрогеназа (ПДГ) ингибируется, когда монометиларсоновая кислота (ММА) нацелена на тиольную группу кофактора липоевой кислоты. ПДГ является предшественником ацетил-КоА, поэтому ингибирование ПДГ в конечном итоге ограничивает производство АТФ в цепи переноса электронов, а также производство глюконеогенеза
Мышьяк может вызывать окислительный стресс за счет образования активных форм кислорода (ROS) и активных форм азота (RNS). Активные формы кислорода продуцируются ферментом НАДФН-оксидазой, который переносит электроны от НАДФН к кислороду, синтезируя супероксид, который является реактивным свободным радикалом. Этот супероксид может реагировать с образованием пероксида водорода и активных форм кислорода. Фермент НАДФН-оксидаза способен генерировать больше активных форм кислорода в присутствии мышьяка за счет субъединицы p22phax, которая отвечает за перенос электронов и регулируется мышьяком. Активные формы кислорода способны воздействовать на эндоплазматический ретикулум, что увеличивает количество сигналов ответа развернутого белка. Это приводит к воспалению, пролиферации клеток и, в конечном итоге, к их гибели. Другой механизм, при котором активные формы кислорода вызывают гибель клеток, связан с перестройкой цитоскелета, которая влияет на сократительные белки.
Активные формы азота возникают, когда активные формы кислорода разрушают митохондрии. Это приводит к образованию активных форм азота, которые ответственны за повреждение ДНК при отравлении мышьяком. Известно, что повреждение митохондрий вызывает высвобождение активных форм азота из-за реакции между супероксидами и оксидом азота (NO). Оксид азота (NO) является частью регуляции клеток, включая клеточный метаболизм, рост, деление и смерть. Оксид азота (NO) реагирует с активными формами кислорода с образованием пероксинитрита. В случаях хронического воздействия мышьяка уровни оксида азота истощаются из-за супероксидных реакций. Фермент NO-синтаза (NOS) использует L-аргинин для образования оксида азота, но этот фермент ингибируется монометилированными соединениями мышьяка (III).
Сообщается, что мышьяк вызывает Модификации ДНК, такие как анеуплоидия, образование микроядер, хромосомная аномалия, делеционные мутации, обмен сестринских хроматид и сшивание ДНК белками. Было продемонстрировано, что мышьяк не взаимодействует напрямую с ДНК и считается плохим мутагеном, но вместо этого он способствует мутагенности других канцерогенов. Например, синергетическое увеличение мутагенной активности мышьяка с УФ-светом наблюдалось в клетках человека и других млекопитающих после воздействия мышьяка на УФ-обработанные клетки. Серия экспериментальных наблюдений предполагает, что генотоксичность мышьяка в первую очередь связана с образованием активных форм кислорода (ROS) во время его биотрансформации. Продукция ROS способна генерировать аддукты ДНК, разрывы цепей ДНК, сшивки и хромосомные аберрации. Окислительное повреждение вызывается модификацией ДНК азотистых оснований, в частности, 8-оксогуанина (8-OHdG), что приводит к мутациям G: C в T: A. Неорганический мышьяк также может вызывать разрыв цепи ДНК даже при низких концентрациях.
Ингибирование процессов репарации ДНК считается одним из основных механизмов генотоксичности неорганического мышьяка. эксцизионная репарация нуклеотидов (NER) и эксцизионная репарация оснований (BER) - это процессы, участвующие в репарации повреждений оснований ДНК, вызванных ROS после воздействия мышьяка. В частности, механизм NER является основным путем восстановления объемных искажений в двойной спирали ДНК, в то время как механизм BER в основном участвует в восстановлении однонитевых разрывов, вызванных ROS, но неорганический мышьяк также может подавлять механизм BER.
Мышьяк очень вреден для врожденной и адаптивной иммунной системы организма. Когда количество развернутых и неправильно свернутых белков в эндоплазматическом ретикулуме стрессе чрезмерно, развернутый белковый ответ (UPR) активируется, чтобы увеличить активность нескольких рецепторов, которые отвечают за восстановление гомеостаза. Инозит-требующий фермент-1 (IRE1) и протеинкиназа РНК-подобная киназа эндоплазматического ретикулума (PERK) являются двумя рецепторами, ограничивающими скорость трансляции. С другой стороны, развернутые белки корректируются за счет продукции шаперонов, которые индуцируются активирующим фактором транскрипции 6 (ATF6). Если количество ошибочных белков увеличивается, срабатывает дополнительный механизм, запускающий апоптоз. Доказано, что мышьяк увеличивает активность этих белковых сенсоров.
Воздействие мышьяка у маленьких детей искажает соотношение Т-хелперных клеток (CD4 ) в цитотоксические Т-клетки (CD8 ), которые ответственны за иммунодепрессию. Кроме того, мышьяк также увеличивает количество воспалительных молекул, секретируемых через макрофаги. Избыточное количество гранулоцитов и моноцитов приводит к хроническому состоянию воспаления, которое может привести к развитию рака.
Есть три молекулы, которые служат хелатирующими агентами, связывающимися с мышьяком. Этими тремя являются британский анти-люизит (BAL, димеркапрол), сукцимер (DMSA ) и унитиол (DMPS ).
, когда эти агенты хелатируют неорганические мышьяк, он превращается в органическую форму мышьяка, потому что он связан с органическим хелатирующим агентом. Атомы серы групп тиол являются местом взаимодействия с мышьяком. поскольку тиоловые группы нуклеофильны, а атомы мышьяка электрофильны. После связывания с хелатирующим агентом молекулы могут выводиться из организма, и, следовательно, свободные неорганические атомы мышьяка удаляются из организма.
Могут использоваться и другие хелатирующие агенты, но они могут вызывать больше побочных эффектов, чем британский антилевизит (BAL, димеркапрол), сукцимер (DMSA ) и (DMPS ). DMPS и DMSA также имеют более высокий терапевтический индекс, чем BAL.
Эти препараты эффективны при остром отравлении мышьяком, которое относится к мгновенным эффектам, вызванным отравлением мышьяком. Например, h Головные боли, рвота или потливость - некоторые из распространенных примеров мгновенного эффекта. Для сравнения, хронические ядовитые эффекты возникают позже, причем неожиданно, например, повреждение органов. Обычно предотвратить их появление уже поздно. Поэтому следует принимать меры сразу же при возникновении острых ядовитых эффектов.