 Фенилаланин
Фенилаланин 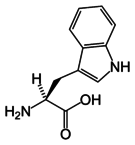 Триптофан
Триптофан  Тирозин
Тирозин ароматическая аминокислота (AAA ) - это аминокислота, которая включает ароматическое кольцо. Среди 20 стандартных аминокислот следующие являются ароматическими: фенилаланин, триптофан и тирозин. Однако, помимо того, что тирозин является ароматическим, его можно классифицировать как полярную аминокислоту. Кроме того, хотя гистидин содержит ароматическое кольцо, его основные свойства позволяют классифицировать его преимущественно как полярную аминокислоту; однако соединение по-прежнему ароматическое.
Ароматические аминокислоты поглощают ультрафиолетовый свет при длине волны более 250 нм и производят флуоресценцию. Эта характеристика используется в количественном анализе, особенно при определении концентраций этих аминокислот в растворе. Это достигается за счет использования УФ-спектрофотометра и уравнения закона Бера-Ламберта. Большинство белков будет иметь максимум поглощения при 280 нм из-за присутствия ароматических аминокислот в их первичной структуре. Однако, поскольку существует несколько ароматических аминокислот, этот метод имеет низкую точность; для смягчения этой проблемы желаемый белок должен быть чистым, и его молярная поглощающая способность известна. Кроме того, белок без ароматических аминокислот не будет иметь максимум поглощения примерно при 280 нм. Присутствие нуклеиновых кислот в белке может дополнительно снизить точность метода из-за присутствия пуриновых и пиримидиновых колец, которые имеют максимум поглощения примерно при 260 нм. Фенилаланин имеет относительно низкую абсорбцию по сравнению с другими стандартными ароматическими аминокислотами; его присутствие в белке может быть обнаружено только в отсутствие триптофана и тирозина. Его максимум поглощения приходится на 257 нм. Следовательно, он имеет относительно слабую флуоресценцию. Триптофан имеет самую высокую относительную абсорбцию по сравнению с другими стандартными ароматическими аминокислотами; его максимум поглощения приходится на 280 нм. Боковая цепь триптофана не титруется. Максимум поглощения тирозина приходится на 274 нм. В химических реакциях тирозин может действовать как нуклеофил. Ароматические аминокислоты также играют решающую роль во гликановых взаимодействиях.
 Гистидин
Гистидин .
У растений путь шикимата сначала приводит к образованию хоризмата, который является предшественником фенилаланина, тирозина и триптофана. Эти ароматические аминокислоты являются производными многих вторичных метаболитов, все они необходимы для биологических функций растения, таких как гормоны салицилат и ауксин. Этот путь содержит ферменты, которые могут регулироваться ингибиторами, которые могут прекращать выработку хоризмата и, в конечном итоге, биологические функции организма. Гербициды и антибиотики действуют путем ингибирования этих ферментов, участвующих в биосинтезе ароматических аминокислот, тем самым делая их токсичными для растений. Глифосат, тип гербицида, используется для контроля накопления избыточной зелени. Помимо уничтожения зелени, глифосат может легко влиять на поддержание микробиоты кишечника в организме-хозяине, специфически ингибируя 5-енолпирувилшикинат-3-фосфатсинтазу, которая предотвращает биосинтез незаменимых ароматических аминокислот. Ингибирование этого фермента приводит к расстройствам, таким как желудочно-кишечные заболевания и нарушения обмена веществ.
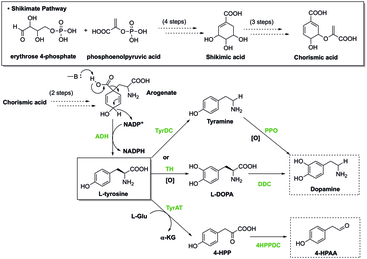 Схема пути шикимата и примеры аминокислот, выступающих в качестве предшественников.
Схема пути шикимата и примеры аминокислот, выступающих в качестве предшественников. Ароматические аминокислоты часто служат предшественниками других молекул. Например, при производстве адреналина фенилаланин является исходной молекулой. Реакция указана ниже:
Фенилаланин → Тирозин → L-ДОФА → Дофамин → Норэпинефрин → Адреналин
Тирозин также является прекурсором для синтеза октопамина и меланина во многих организмах. При производстве тироксина фенилаланин также служит исходным предшественником:
Фенилаланин → Тирозин → Тироксин
При производстве серотонина триптофан является исходной молекулой, поскольку указано ниже:
Триптофан → 5-гидрокситриптофан → Серотонин
Кроме того, гистидин является предшественником гистамина. Триптофан является исходной молекулой для синтеза триптамина, серотонина, ауксина, кинуренинов и мелатонина.
Животные получают ароматические аминокислоты из своего рациона, но все растения и микроорганизмы должны синтезировать свои ароматические аминокислоты через метаболически затратный путь шикимата, чтобы произвести их. Фенилаланин, триптофан и гистидин являются незаменимыми аминокислотами для животных. Поскольку они не синтезируются в организме человека, их необходимо получать с пищей. Тирозин является частично незаменимым; следовательно, он может быть синтезирован животными, но только из фенилаланина. Фенилкетонурия, генетическое заболевание, которое возникает в результате неспособности расщеплять фенилаланин, вызвано нехваткой фермента фенилаланингидроксилазы. Недостаток триптофана в рационе может вызвать задержку развития скелета. Имеются данные, позволяющие предположить, что высокое потребление ароматических аминокислот с пищей может увеличить уровень гипертонии, хотя требуются дополнительные исследования. Синдром голубых подгузников - аутосомно-рецессивное заболевание, вызываемое из-за плохого усвоения триптофана в организме.
.