 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Гидроксид алюминия | |
| Систематическое название IUPAC Алюминий (3+) триоксиданид | |
| Другие названия Алюминиевая кислота. Гидроксид алюминия. Гидроксид алюминия (III). Гидроксид алюминия. Тригидроксид алюминия. Гидратированный оксид алюминия. Ортоалюминовая кислота | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.040.433 |
| KEGG | |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
| InChI | |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | Al (OH) 3 |
| Молярный масса | 78,00 г / моль |
| Внешний вид | Белый аморфный порошок |
| Плотность | 2,42 г / см, твердый |
| Точка плавления | 300 ° С (572 ° F; 573 K) |
| Растворимость в воде | 0,0001 г / 100 мл |
| Произведение растворимости (Ksp) | 3 × 10 |
| Растворимость | растворим в кислотах и щелочах |
| Кислотность (pK a) | >7 |
| Изоэлектрическая точка | 7,7 |
| Термохимия | |
| Стандартная энтальпия. образования (ΔfH298) | −1277 кДж · моль |
| Фармакология | |
| Код АТС | A02AB01 (ВОЗ ) |
| Беременность. категория |
|
| Опасности | |
| Паспорт безопасности | Внешний паспорт безопасности материала |
| Пиктограммы GHS |  |
| Предупреждения об опасности GHS | H319, H335 |
| Меры предосторожности GHS | P264, P261, P280, P271, P312, P304 + 340, P305 + 351 + 338, P337 +313 |
| NFPA 704 (огненный алмаз) |  0 1 0 0 1 0 |
| Температура вспышки | Невоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | >5000 мг / кг (крыса, перорально) |
| Родственные соединения | |
| Другие анионы | Нет |
| Родственные соединения | Оксид натрия,. гидроксид алюминия |
| За исключением случаев, когда в противном случае данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на ink | |
Гидроксид алюминия, Al (OH) 3, встречается в природе как минерал гиббсит (также известный как гидраргиллит), а его три гораздо реже полиморфы : байерит, дойлит и нордстрандит. Гидроксид алюминия является амфотерным по природе, то есть он имеет как основные, так и кислотные свойства. Близкими родственниками являются гидроксид алюминия, AlO (OH) и оксид алюминия или оксид алюминия (Al 2O3), последний из которых также является амфотерным. Эти соединения вместе являются основными компонентами алюминиевого ore боксита.
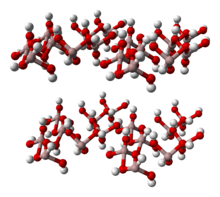
Al (OH) 3 состоит из двойных слоев гидроксильных групп с ионами алюминия, занимающими две трети октаэдрических отверстий между двумя слоями. Распознаются четыре полиморфа. Все характерные слои состоят из октаэдрических единиц гидроксида алюминия с водородными связями между слоями. Полиморфы различаются по наложению слоев. Все формы кристаллов Al (OH) 3 являются гексагональными:
гидрагиллит, который когда-то считался быть гидроксидом алюминия, представляет собой фосфат алюминия. Тем не менее, и гиббсит, и гидраргиллит относятся к одному и тому же полиморфизму гидроксида алюминия, причем гиббсит чаще всего используется в Соединенных Штатах, а гидраргиллит чаще используется в Европе. Гидрагиллит назван в честь греческих слов, обозначающих воду (гидра) и глина (аргиллы).
Гидроксид алюминия амфотерный. В кислоте она действует как основание Бренстеда – Лоури. Он нейтрализует кислоту, образуя соль:
В основаниях он действует как Кислота Льюиса путем связывания гидроксид-ионов:
 Красный шлам коллекторы (этот в Stade, Германия) содержат коррозионные остатки от производства гидроксида алюминия.
Красный шлам коллекторы (этот в Stade, Германия) содержат коррозионные остатки от производства гидроксида алюминия. Практически весь гидроксид алюминия, используемый на рынке, производится по процессу Байера, который включает растворение боксита в гидроксиде натрия при температуре до 270 ° C (518 ° F). Твердые отходы, бокситовые хвосты, удаляют, и гидроксид алюминия осаждают из оставшегося раствора алюмината натрия. Этот гидроксид алюминия можно превратить в оксид алюминия или оксид алюминия путем прокаливания.
Остаток или бокситовые хвосты, которые в основном представляют собой оксид железа, очень едкие из-за остаточного натрия. гидроксид. Исторически хранился в лагунах; это привело к аварии на глиноземном заводе в Айке в 2010 году в Венгрии, где прорыв дамбы привел к гибели девяти человек. Еще 122 человека обратились за лечением по поводу химических ожогов. Грязь залила 40 квадратных километров (15 квадратных миль) земли и достигла Дуная. Хотя грязь считалась нетоксичной из-за низкого уровня тяжелых металлов, связанная с ней суспензия имела pH 13.
Также гидроксид алюминия находит применение в качестве огнезащитного наполнителя для полимеров. Он выбран для этих целей, потому что он бесцветен (как и большинство полимеров), дешев и обладает хорошими огнезащитными свойствами. Гидроксид магния и смеси хантита и гидромагнезита используются аналогичным образом. Он разлагается при температуре около 180 ° C (356 ° F), поглощая при этом значительное количество тепла и выделяя водяной пар. Помимо того, что он ведет себя как антипирен, он очень эффективен в качестве подавителя дыма в широком диапазоне полимеров, особенно в полиэфирах, акрилах, этиленвинилацетате, эпоксидных смолах, ПВХ и резине.
Гидроксид алюминия является сырьем для производства других соединений алюминия: специального кальцинированного оксида алюминия, сульфата алюминия, хлорида полиалюминия, хлорид алюминия, цеолиты, алюминат натрия, активированный оксид алюминия и нитрат алюминия.
Свежеосажденный гидроксид алюминия образует гели, которые являются основой для применения солей алюминия в качестве флокулянтов при очистке воды. Этот гель со временем кристаллизуется. Гели гидроксида алюминия могут быть дегидратированы (например, с использованием смешивающихся с водой неводных растворителей, таких как этанол ) с образованием порошка аморфного гидроксида алюминия, который легко растворяется в кислотах. Нагревание превращает его в активированный оксид алюминия, который используется в качестве осушителей, адсорбента при газоочистке и носителей катализатора.
под общим названием «альгельдрат», гидроксид алюминия, используется в качестве антацида у людей и животных (в основном кошек и собак). Он предпочтительнее других альтернатив, таких как бикарбонат натрия, потому что Al (OH) 3, будучи нерастворимым, не увеличивает pH желудка выше 7 и, следовательно, не вызывает секрецию избытка. кислота желудком. Торговые марки включают Alu-Cap, Aludrox, Gaviscon или Pepsamar. Он вступает в реакцию с избытком кислоты в желудке, снижая кислотность содержимого желудка, что может облегчить симптомы язвы, изжоги или диспепсии. Такие продукты могут вызывать запор, потому что ионы алюминия подавляют сокращения гладкомышечных клеток в желудочно-кишечном тракте, замедляя перистальтику и удлиняя время, необходимое для стула. пройти через двоеточие. Некоторые такие продукты созданы для минимизации таких эффектов за счет включения в равных концентрациях гидроксида магния или карбоната магния, которые обладают уравновешивающим слабительным действием.
Это соединение также используется для контроля гиперфосфатемии (повышенных уровней фосфата или фосфора в крови) у людей и животных, страдающих почечной недостаточностью. Обычно почки отфильтровывают избыток фосфата из крови, но почечная недостаточность может привести к накоплению фосфата. Соль алюминия при проглатывании связывается с фосфатом в кишечнике и снижает количество фосфора, которое может абсорбироваться.
Осажденный гидроксид алюминия включен в качестве адъюванта в некоторых вакцинах (например, вакцина против сибирской язвы ). Одной из хорошо известных марок адъюванта гидроксида алюминия является Alhydrogel, производимый Brenntag Biosector. Поскольку он хорошо абсорбирует белок, он также действует для стабилизации вакцин, предотвращая осаждение белков в вакцине или прилипание к стенкам контейнера во время хранения. Гидроксид алюминия иногда называют «квасцами », термин, обычно зарезервированный для одного из нескольких сульфатов.
Составы вакцин, содержащие гидроксид алюминия, стимулируют иммунную систему, вызывая высвобождение мочевой кислоты, иммунологический сигнал опасности. Это сильно привлекает определенные типы моноцитов, которые дифференцируются в дендритные клетки. Дендритные клетки захватывают антиген, переносят его в лимфатические узлы и стимулируют Т-клетки и В-клетки. По-видимому, он способствует индукции хорошего ответа Tdiv class="ht", поэтому его можно использовать для иммунизации против патогенов, которые блокируются антителами. Однако он имеет небольшую способность стимулировать клеточный (Th1) иммунный ответ, важный для защиты от многих патогенов, и он бесполезен, когда антиген основан на пептиде.
Гидроксид алюминия, как и большинство соединений алюминия, малотоксичен.
В 1960-х и 1970-х годах предполагалось, что алюминий связан с различными неврологическими расстройствами, включая болезнь Альцгеймера. С тех пор многочисленные эпидемиологические исследования не обнаружили связи между воздействием алюминия или проглоченного алюминия и неврологическими расстройствами, хотя вводимый алюминий в этих исследованиях не рассматривался.