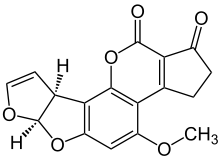
 . Химическая структура (-) - афлатоксина B 1 . Химическая структура (-) - афлатоксина B 1 | |
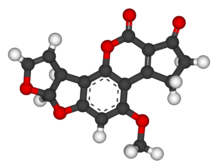 . Трехмерная структура афлатоксина B 1 . Трехмерная структура афлатоксина B 1 | |
| Имена | |
|---|---|
| Название ИЮПАК (6aR, 9aS) -2,3,6a, 9a-Тетрагидро-4-метокси-1H, 11H-циклопента [c] фуро [3 ', 2': 4,5] фуро [2,3-h] [1] бензопиран-1,11-дион | |
| Другие названия NSC 529592 | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChEMBL |
|
| ChemSpider | |
| ECHA InfoCard | 100.013.276 |
| PubChem CID | |
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | C17H12O6 |
| Молярная масса | 312,277 г · моль |
| Опасности | |
| Основные опасности | Канцероген - Мутаген - Острая токсичность / Яд |
| Пиктограммы GHS |   |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H300 , H310 , H330 , H340 , H350 |
| Меры предосторожности GHS | P201 , P202 , P260 , P262 , P264 , P270 , P271 , P280 , P281 , P284 , P301 + 330 + 331 , P310 , P302 + 350 , P304 + 340 , P311 , P308 + 313 , P320 , P321 , P322 , P330 , P361 , P363 , P403 + 233 , P405 , P501 |
| Если не указано иное, данные приводятся для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационное окно | |
Афлатоксин B 1представляет собой афлатоксин, продуцируемый Aspergillus flavus и A. parasiticus. Это очень мощный канцероген с TD50 3,2 мкг / кг / день у крыс. Эта канцерогенная активность варьируется в зависимости от вида, причем некоторые, например крысы и обезьяны, кажутся гораздо более восприимчивыми, чем другие. Афлатоксин B 1 является обычным загрязнителем различных пищевых продуктов, включая арахис, хлопковую муку, кукурузу и другие зерновые; а также корма для животных. Афлатоксин B 1 считается наиболее токсичным афлатоксином, и он сильно вовлечен в гепатоцеллюлярную карциному (ГЦК) у людей. У животных афлатоксин B 1 также оказался мутагенным, тератогенным и вызывает иммуносупрессию. Несколько методов отбора проб и анализа, включая тонкослойную хроматографию (ТСХ), высокоэффективную жидкостную хроматографию (ВЭЖХ), масс-спектрометрию и ферментативную хроматографию. Связанный иммуносорбентный анализ (ELISA), среди прочего, использовался для тестирования пищевых продуктов на загрязнение афлатоксином B 1. По данным Продовольственной и сельскохозяйственной организации (ФАО), максимальные переносимые уровни афлатоксина B 1 в мире находятся в диапазоне 1–20 мкг / кг в продуктах питания, и 5–50 мкг / кг в диетическом корме КРС в 2003 году.
Афлатоксин B 1 в основном обнаруживается в зараженной пище, и люди практически полностью подвергаются воздействию афлатоксина B 1 через свой рацион. Также сообщалось о профессиональном воздействии афлатоксина B 1 на свиноводство и птицеводство. Хотя контаминация афлатоксином B 1 часто встречается во многих основных продуктах питания, его производство максимально увеличивается в продуктах, хранящихся в жарком влажном климате. Следовательно, воздействие наиболее распространено в Юго-Восточной Азии, Южной Америке и Африке к югу от Сахары.
Афлатоксин B 1 может проникать через кожу. Воздействие этого афлатоксина на кожу в определенных условиях окружающей среды может привести к серьезным рискам для здоровья. Печень является наиболее чувствительным органом к токсичности афлатоксина B 1. В исследованиях на животных патологические поражения, связанные с интоксикацией афлатоксином B 1, включают уменьшение веса печени, вакуолизацию гепатоцитов и карциному печени. Другие поражения печени включают увеличение печеночных клеток, жировую инфильтрацию, некроз, кровоизлияние, фиброз, регенерацию узелков и пролиферацию желчных протоков / гиперплазию.
Aspergillus flavus - это гриб семейства Trichocomaceae, распространенный во всем мире. Плесень живет в почве, выживая за счет мертвых растений и животных, но распространяется по воздуху через воздушные конидии. Этот гриб растет в длинных разветвленных гифах и способен питаться множеством источников пищи, включая кукурузу и арахис. Грибок и его продукты патогенны для ряда видов, включая человека. В то время как токсичность его продуктов, афлатоксинов, исследуется в этой статье, сам Aspergillus flavus также оказывает патогенное действие через аспергиллез или заражение плесенью. Эта инфекция в основном возникает в легких пациентов с ослабленным иммунитетом, но инфекция может также возникать на коже или других органах. В отличие от многих видов плесени, Aspergillus flavus предпочитает жаркие и сухие условия. Его оптимальный рост при 37 ° C (99 ° F) способствует его патогенности для людей.
Афлатоксин B 1 происходит от обоих выделенных синтаза жирных кислот (FAS) и поликетидсинтаза (PKS), вместе известные как синтаза норсолориновой кислоты. Биосинтез начинается с синтеза гексаноата с помощью FAS, который затем становится стартовой единицей для итеративного PKS типа I. PKS добавляет семь наполнителей малонил-CoA к гексаноату с образованием поликетидного соединения C20. PKS сворачивает поликетид особым образом, чтобы вызвать циклизацию с образованием антрахинон-норсолориновой кислоты. Затем редуктаза катализирует восстановление кетона в боковой цепи с образованием аверантина. Аверантин превращается в аверуфин с помощью двух разных ферментов, гидроксилазы и алкогольдегидрогеназы. Это будет насыщать кислородом и циклизовать боковую цепь аверантина с образованием кеталя в аверуфине.
С этого момента биосинтетический путь афлатоксина B 1 становится намного более сложным, с несколькими серьезными изменениями скелета. Большинство ферментов не охарактеризовано, и может быть еще несколько промежуточных продуктов, которые все еще неизвестны. Однако известно, что аверуфин окисляется P450 -оксидазой, AvfA, при окислении Байера-Виллигера. Это открывает эфирные кольца и при перегруппировке образуется версикональный ацетат. Теперь эстераза, EstA, катализирует гидролиз ацетила, образуя первичный спирт в версиконале. Ацеталь в версиколорине A образуется в результате циклизации боковой цепи версиконала, которая катализируется VERB-синтазой, а затем VerB, десатураза, восстанавливает версиколорин B с образованием дигидробисфурана.
Есть еще два ферменты, которые катализируют превращение версиколорина А в деметилстеригматоцистин: AflN, оксидаза, и AflM, редуктаза. Эти ферменты используют молекулярный кислород и два НАДФН для дегидратации одной из гидроксильных групп антрахинона и открытия хинина с помощью молекулярного кислорода. При образовании альдегида на стадии раскрытия цикла он окисляется с образованием карбоновой кислоты, и впоследствии происходит декарбоксилирование, чтобы замкнуть кольцо, образуя шестичленную кольцевую систему простого эфира, наблюдаемую в деметилстеригматоцистине. Следующими двумя этапами биосинтетического пути является метилирование S-аденозилметионином (SAM) двух гидроксильных групп ксантоновой части деметистеригматоцистина двумя разными метилтрансферазами, OmtB и OmtA. Это дает O-метилстеригматоцистин. На последних стадиях происходит окислительное расщепление ароматического кольца и потеря одного углерода в O-метилстеригматоцистине, что катализируется OrdA, оксидоредуктазой. Затем происходит окончательная рециклизация с образованием афлатоксина B 1.
Афлатоксин B 1 - мощный генотоксичный гепатоканцероген, воздействие которого сильно связано с развитием гепатоцеллюлярной карциномы, опухолей печени, особенно учитывая коинфекцию вирусом гепатита В. Эти эффекты, по-видимому, в значительной степени опосредованы мутациями гуанина в кодоне 249 гена p53, гена подавления опухоли, и нескольких остатков гуанина в 12-м и 13-м кодонах гена ras, гена, продукт которого контролирует сигналы клеточной пролиферации. Афлатоксин B 1 должен сначала метаболизироваться в его реактивную электрофильную форму, афлатоксин B 1 -8,9-экзоэпоксид с помощью цитохрома p450. Эта активная форма затем интеркалирует между остатками оснований ДНК и образует аддукты с остатками гуанина, чаще всего афлатоксином B 1 -N7-Gua. Эти аддукты могут затем перестроиться или полностью удаляться из основной цепи, образуя апуриновый сайт. Эти аддукты и изменения представляют собой повреждения, которые после репликации ДНК вызывают вставку несоответствующего основания в противоположную цепь. До 44% гепатоцеллюлярных карцином в регионах с высокой экспозицией афлатоксина несут трансверсию GC → TA в кодоне 249 р53, характерную мутацию, наблюдаемую для этого токсина.
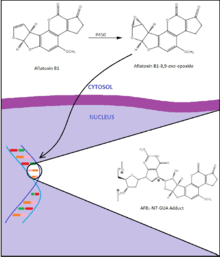 Адаптировано из Semela et al. 2001
Адаптировано из Semela et al. 2001 Распространенность гепатоцеллюлярной карциномы у лиц, подвергшихся воздействию афлатоксина, возрастает при одновременном инфицировании вирусом гепатита В. Одно исследование показало, что, хотя у людей с биомаркерами афлатоксина в моче риск гепатоцеллюлярной карциномы в три раза выше, чем у нормальной популяции; инфицированные вирусом гепатита B подвергались четырехкратному риску; и те, у кого были биомаркеры афлатоксина и инфицированы вирусом гепатита B, имели в 60 раз больший риск гепатоцеллюлярной карциномы, чем нормальная популяция.
Несколько афлатоксинов B 1 исследований токсичности было проведено на различных видах животных.
Воздействие афлатоксина B 1 лучше всего контролировать с помощью мер, направленных на предотвращение заражения сельскохозяйственных культур на поле, послеуборочную обработку и хранение или с помощью мер, направленных на обнаружение и обеззараживание зараженных товаров или материалов, используемых в кормах для животных. Например, биологическая дезинфекция с использованием одного вида бактерий, Flavobacterium aurantiacum, была использована для удаления афлатоксина B 1 из арахиса и кукурузы.
В нескольких странах мира действуют правила и нормы. регулирующие содержание афлатоксина B 1 в пищевых продуктах, включая максимально разрешенные или рекомендуемые уровни афлатоксина B 1 для определенных пищевых продуктов.
Открытие афлатоксина B 1 произошло следы массовой гибели индеек в Англии летом 1960 года от какой-то неизвестной болезни, в то время называемой «Болезнь Х». В течение 500 вспышек болезнь унесла жизни более 100 000 индеек, которые оказались здоровыми. Позднее было установлено, что массовая смерть была вызвана заражением арахисовой муки Aspergillus flavus.
Двенадцать пациентов умерли от острого отравления афлатоксином в нескольких больницах района Мачакос в Кении в 1981 году после употребления зараженной кукурузы. Все пациенты также страдали гепатитом.
После вспышек заражения кукурузы афлатоксином, достигшей 4 400 частей на миллиард весной 2004 года, 125 человек в Кении умерли от острой печеночной недостаточности, а всего было зарегистрировано 317 случаев. На сегодняшний день это была самая крупная из известных вспышек афлатоксоза с точки зрения зарегистрированных смертей.