 Туман и туман являются аэрозолями
Туман и туман являются аэрозолями . аэрозоль (аббревиатура от «аэро-раствор») представляет собой суспензию мелких твердых частиц или жидкости капли в воздухе или другом газе. Аэрозоли могут быть естественными или антропогенными. Примеры природных аэрозолей: туман, туман, пыль, лес экссудаты и гейзер пар. Примерами антропогенных аэрозолей являются частицы загрязнители воздуха и дым. Жидкие или твердые частицы обычно имеют диаметр менее 1 мкм ; более крупные частицы со значительной скоростью оседания делают смесь суспензией, но различие не является четким. В общем, аэрозоль обычно относится к аэрозольному спрею, который доставляет потребительский продукт из баллончика или аналогичного контейнера. Другие технологические применения аэрозолей включают распыление пестицидов, лечение респираторных заболеваний и технологию сжигания. Заболевания также могут распространяться с помощью небольших капель в дыхании , также называемых аэрозолями (или иногда биоаэрозоли ).
Аэрозольная наука охватывает образование и удаление аэрозолей, технологическое применение аэрозолей, воздействие аэрозолей на окружающую среду и людей и другие темы.
 Микрофотография, сделанная с помощью сканирующего электронного микроскопа (SEM): Летучая зола частицы при 2,000-кратном увеличении. Большинство частиц в этом аэрозоле имеют почти сферическую форму.
Микрофотография, сделанная с помощью сканирующего электронного микроскопа (SEM): Летучая зола частицы при 2,000-кратном увеличении. Большинство частиц в этом аэрозоле имеют почти сферическую форму. Аэрозоль определяется как система суспензии твердых или жидких частиц в газе. Аэрозоль включает в себя как частицы, так и взвешенный газ, которым обычно является воздух. Фредерик Г. Доннан предположительно впервые использовал термин аэрозоль во время Первой мировой войны для описания аэро- раствор, облака микроскопических частиц в воздухе. Этот термин возник аналогично термину гидрозоль, коллоидной системе с водой в качестве дисперсной среды. Первичные аэрозоли содержат частицы, введенные непосредственно в газ; вторичные аэрозоли образуются в результате преобразования газа в частицы.
Различные типы аэрозолей, классифицируемые по физической форме и способу их образования, включают пыль, дым, туман, дым и туман.
Есть несколько способов измерения концентрации аэрозоля. Экология и гигиена окружающей среды часто используют массовую концентрацию (M), определяемую как масса твердых частиц на единицу объема в таких единицах, как мкг / м. Также обычно используется числовая концентрация (N), количество частиц на единицу объема, в таких единицах, как количество на м или количество на см.
Размер частиц имеет большое влияние на свойства частиц, а радиус или диаметр аэрозольной частицы (d p) является ключевым свойством, используемым для характеристики аэрозолей.
Аэрозоли различаются по своей дисперсности. Монодисперсный аэрозоль, производимый в лаборатории, содержит частицы одинакового размера. Однако большинство аэрозолей в виде полидисперсных коллоидных систем имеют частицы различного размера. Капли жидкости почти всегда имеют почти сферическую форму, но ученые используют эквивалентный диаметр, чтобы охарактеризовать свойства твердых частиц различной формы, некоторые из которых имеют очень неправильную форму. Эквивалентный диаметр - это диаметр сферической частицы с тем же значением некоторого физического свойства, что и у частицы неправильной формы. Эквивалентный объемный диаметр (d e) определяется как диаметр сферы того же объема, что и у частицы неправильной формы. Также обычно используется аэродинамический диаметр, d a.
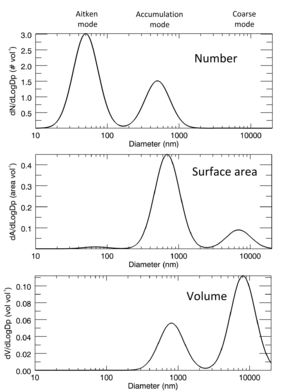 Такое же гипотетическое логнормальное распределение аэрозоля, нанесенное сверху вниз в виде числа в зависимости от распределения диаметра, площади поверхности в зависимости от..распределение диаметра и распределение объема по диаметру. Типичные названия режимов показаны вверху. Каждое распределение нормализовано так, что общая площадь равна 1000.
Такое же гипотетическое логнормальное распределение аэрозоля, нанесенное сверху вниз в виде числа в зависимости от распределения диаметра, площади поверхности в зависимости от..распределение диаметра и распределение объема по диаметру. Типичные названия режимов показаны вверху. Каждое распределение нормализовано так, что общая площадь равна 1000. Для монодисперсного аэрозоля одного числа - диаметра частиц - достаточно, чтобы описать размер частиц. Однако более сложные распределения частиц по размерам описывают размеры частиц в полидисперсном аэрозоле. Это распределение определяет относительное количество частиц, отсортированных по размеру. Один из подходов к определению гранулометрического состава использует список размеров каждой частицы в образце. Однако этот подход оказывается утомительным для проверки в аэрозолях с миллионами частиц и неудобен в использовании. Другой подход разбивает весь диапазон размеров на интервалы и определяет количество (или пропорцию) частиц в каждом интервале. Затем можно визуализировать эти данные в виде гистограммы с площадью каждой полосы, представляющей долю частиц в ячейке этого размера, обычно нормализованную путем деления количества частиц в ячейке на ширину интервала так, чтобы Площадь каждого столбца пропорциональна количеству частиц в диапазоне размеров, который он представляет. Если ширина интервалов стремится к нулю, получается частотная функция:

где
 - диаметр частиц
- диаметр частиц - доля частиц, имеющих диаметр от
- доля частиц, имеющих диаметр от  до
до  +
+ 
 - частотная функция
- частотная функцияСледовательно, область под кривой частоты между двумя размерами a и b представляет собой общую долю частиц в этом диапазоне размеров:

Его также можно сформулировать в терминах общей числовой плотности N:

Предполагая, что аэрозольные частицы имеют сферическую форму, поверхность аэрозоля a rea на единицу объема (S) задается вторым моментом :

И третий момент дает общую объемную концентрацию (V) частиц:

Также полезно аппроксимировать распределение частиц по размерам, используя математическую функцию. нормальное распределение обычно не описывает должным образом распределение частиц по размерам в аэрозолях из-за асимметрии, связанной с длинным хвостом более крупных частиц. Также для количества, которое варьируется в большом диапазоне, как и многие размеры аэрозолей, ширина распределения подразумевает отрицательные размеры частиц, что явно физически нереально. Однако нормальное распределение может быть подходящим для некоторых аэрозолей, таких как тестовые аэрозоли, определенные пыльцевые зерна и споры.
Более широко выбранное логнормальное распределение дает частота как:

где:
 - стандартное отклонение распределения размеров и
- стандартное отклонение распределения размеров и - среднее арифметическое диаметр.
- среднее арифметическое диаметр.Логнормальное распределение не имеет отрицательных значений, может охватывать широкий диапазон значений и достаточно хорошо подходит для многих наблюдаемых распределений по размерам.
Другие распределения, иногда используемые для характеристики размера частиц, включают: распределение Розина-Раммлера, применяемое к крупнодисперсным пыль и аэрозоли; для распылителей чрезвычайно широкого диапазона размеров; распределение степенной функции, иногда применяемое к атмосферным аэрозолям; экспоненциальное распределение, применяемое к порошковым материалам; и для облачных капель.
Для низких значений числа Рейнольдса (<1), true for most aerosol motion, Закон Стокса описывает силу сопротивления, действующую на твердую сферическую частицу в жидкости. Однако закон Стокса справедлив только тогда, когда скорость газа у поверхности частицы равна нулю. Для мелких частиц (< 1 μm) that characterize aerosols, however, this assumption fails. To account for this failure, one can introduce the Поправочный коэффициент Каннингема, всегда больше 1. Включая этот коэффициент, можно найти связь между силой сопротивления, действующей на частицу, и ее скоростью:

где
 - сила сопротивления на сферическом частица
- сила сопротивления на сферическом частица - динамическая вязкость газа
- динамическая вязкость газа - скорость частицы
- скорость частицы - поправочный коэффициент Каннингема.
- поправочный коэффициент Каннингема.Это позволяет нам вычислить предельную скорость o f частица, подвергающаяся гравитационному осаждению в неподвижном воздухе. Пренебрегая эффектом плавучести, мы находим:

где
 - конечная скорость оседания частицы.
- конечная скорость оседания частицы.Конечная скорость также может быть выведенным для других видов сил. Если закон Стокса выполняется, то сопротивление движению прямо пропорционально скорости. Константа пропорциональности - это механическая подвижность (B) частицы:

Частица, движущаяся с любой разумной начальной скоростью, приближается к своей конечной скорости экспоненциально с временем электронного сворачивания, равным времени релаксации:

где:
 - скорость частицы в момент времени t
- скорость частицы в момент времени t - конечная скорость частицы
- конечная скорость частицы - начальная скорость частицы
- начальная скорость частицыДля учета Эффект формы несферических частиц, поправочный коэффициент, известный как коэффициент динамической формы, применяется к закону Стокса. Он определяется как отношение силы сопротивления частицы неправильной формы к силе сопротивления сферической частицы с таким же объемом и скоростью:

где:
 - коэффициент динамической формы
- коэффициент динамической формыАэродинамический диаметр частицы неправильной формы определяется как диаметр сферической частицы с плотностью 1000 кг / м и такой же скоростью осаждения, как и у частицы неправильной формы.
Если пренебречь поправкой на скольжение, частица устанавливается на конечной скорости, пропорциональной квадрату аэродинамического диаметра, d a:

где
 = стандартная плотность частиц (1000 кг / м).
= стандартная плотность частиц (1000 кг / м).Это уравнение дает аэродинамический диаметр:

Можно применить аэродинамический диаметр к твердым загрязнителям или вдыхаемым лекарствам, чтобы предсказать, где в дыхательных путях осаждаются такие частицы. Фармацевтические компании обычно используют аэродинамический диаметр, а не геометрический диаметр для характеристики частиц во вдыхаемых лекарствах.
Предыдущее обсуждение было сосредоточено на отдельных аэрозольных частицах. Напротив, динамика аэрозолей объясняет эволюцию полных популяций аэрозолей. Концентрация частиц будет меняться со временем в результате многих процессов. Внешние процессы, которые перемещают частицы за пределы исследуемого объема газа, включают диффузию, гравитационное осаждение и электрические заряды и другие внешние силы, которые вызывают миграцию частиц. Второй набор процессов, внутренних по отношению к данному объему газа, включает образование частиц (зародышеобразование), испарение, химическую реакцию и коагуляцию.
A дифференциальное уравнение, называемое общим динамическим уравнением аэрозолей (GDE), характеризует эволюцию числа плотность частиц в аэрозоле из-за этих процессов.

Изменение во времени = Конвективный перенос + броуновская диффузия + взаимодействие газ-частицы + коагуляция + миграция под действием внешних сил
Где:
 - числовая плотность частиц размерной категории
- числовая плотность частиц размерной категории 
 - скорость частицы;
- скорость частицы; - это частица Стокс-Эйнштейн коэффициент диффузии
- это частица Стокс-Эйнштейн коэффициент диффузии  - скорость частицы, связанная с внешней силой
- скорость частицы, связанная с внешней силойПоскольку частицы и капли в аэрозоле сталкиваются друг с другом, они могут подвергаться слиянию или агрегации. Этот процесс приводит к изменению гранулометрического состава аэрозольных частиц, причем диаметр моды увеличивается по мере уменьшения общего количества частиц. Иногда частицы могут распадаться на множество более мелких частиц; однако этот процесс обычно происходит в основном с частицами, слишком большими для рассмотрения как аэрозоли.
Число Кнудсена частицы определяет три различных динамических режима, которые управляют поведением аэрозоля:

где 


где a - радиус частицы, P ∞ и P A - давления вдали от капли и на поверхности капли соответственно, k b - постоянная Больцмана, T - температура, C A - средняя тепловая скорость, а α - коэффициент аккомодации. Вывод этого уравнения предполагает постоянное давление и постоянный коэффициент диффузии.
Частицы находятся в режиме континуума, когда K n<< 1. In this regime, the particles are big compared to the mean free path of the suspending gas, meaning that the suspending gas acts as a continuous fluid flowing round the particle. The molecular flux in this regime is:

где a - радиус частицы A, M A - молекулярная масса частицы A, D AB - коэффициент диффузии между частицами A и B, R - постоянная идеального газа, T - температура (в абсолютных единицах, таких как кельвин), а P A ∞ и P AS - давления на бесконечности и на поверхности соответственно.
Переходный режим содержит все частицы между свободномолекулярным и континуальным режимами или K n ≈ 1. Силы, действующие на частицу, представляют собой сложную комбинацию взаимодействий с отдельными молекулами газа и макроскопических взаимодействий. Полуэмпирическое уравнение, описывающее поток массы:

где I cont - поток массы в режиме континуума. Эта формула называется интерполяционной формулой Фукса-Сутугина. Эти уравнения не учитывают эффект тепловыделения.
 Конденсация и испарение
Конденсация и испарение Теория разделения аэрозолей регулирует конденсацию и испарение с поверхности аэрозоля соответственно. Конденсация массы вызывает усиление режима гранулометрического состава аэрозоля; наоборот, испарение вызывает уменьшение режима. Зарождение ядра - это процесс образования аэрозольной массы в результате конденсации газообразного предшественника, в частности пара. Чистая конденсация пара требует перенасыщения, парциальное давление больше, чем его давление пара. Это может происходить по трем причинам:
Существует два типа процессов зародышеобразования. Газы предпочтительно конденсируются на поверхностях уже существующих аэрозольных частиц, что известно как гетерогенное зародышеобразование . Этот процесс приводит к увеличению диаметра в режиме гранулометрического состава при постоянной числовой концентрации. При достаточно высоком пересыщении и отсутствии подходящих поверхностей частицы могут конденсироваться в отсутствие ранее существовавшей поверхности, что известно как гомогенное зародышеобразование . Это приводит к добавлению очень маленьких, быстрорастущих частиц к гранулометрическому составу.
Вода покрывает частицы в аэрозолях, делая их активированными, обычно в контексте образования облачная капля. Согласно уравнению Кельвина (основанному на кривизне жидких капель), более мелким частицам требуется более высокая относительная влажность окружающей среды для поддержания равновесия, чем более крупным частицам. Следующая формула дает относительную влажность в состоянии равновесия:

где 
Уравнение Кельвина для давления насыщенного пара над изогнутой поверхностью:

где r p радиус капли, σ поверхностное натяжение капли, ρ плотность жидкости, М молярные масса, температура T и молярная газовая постоянная R.
Не существует общих решений для общего динамического уравнения (GDE); общие методы, используемые для решения общего динамического уравнения, включают:
Люди создают аэрозоли для различных целей, в том числе:
Некоторые устройства для генерации аэрозолей:
Стабильность агломератов наночастиц имеет решающее значение для оценки распределения размеров аэрозольные частицы из нанопорошков или других источников. На рабочих местах нанотехнологий рабочие могут подвергаться вдыханию потенциально токсичных веществ во время работы с наноматериалами и их обработки. Наночастицы в воздухе часто образуют агломераты из-за сил притяжения между частицами, таких как сила Ван-дер-Ваальса или электростатическая сила, если частицы заряжены. В результате аэрозольные частицы обычно наблюдаются в виде агломератов, а не отдельных частиц. Для оценки воздействия и оценки риска переносимых по воздуху наночастиц важно знать о распределении аэрозолей по размерам. При вдыхании людьми частицы разного диаметра откладываются в различных местах центральной и периферийной дыхательной системы. Было показано, что наноразмерные частицы проникают через воздушный барьер в легких и перемещаются во вторичные органы человеческого тела, такие как мозг, сердце и печень. Следовательно, знание стабильности агломератов наночастиц важно для прогнозирования размера аэрозольных частиц, что помогает оценить их потенциальный риск для человеческого тела.
Были созданы различные экспериментальные системы для проверки стабильности частиц в воздухе и их способности дезагломерироваться в различных условиях. Недавно описанная комплексная система способна поддерживать устойчивый процесс аэрозолизации и генерировать аэрозоли со стабильной числовой концентрацией и средним размером из нанопорошков. Потенциал деагломерации различных переносимых по воздуху наноматериалов также можно изучить с помощью критических отверстий. Кроме того, было разработано устройство ударной фрагментации для исследования энергий связи между частицами.
Стандартная процедура испытания на деагломерацию может быть предусмотрена с развитием различных типов существующих систем. Вероятность деагломерации аэрозольных частиц в производственных условиях может быть оценена для различных наноматериалов, если доступен эталонный метод. С этой целью может быть запущено межлабораторное сравнение результатов испытаний на различных установках, чтобы изучить влияние характеристик системы на свойства создаваемых аэрозолей из наноматериалов.
Аэрозоль можно измерять на месте или с помощью методов дистанционного зондирования.
Некоторые доступные методы измерения на месте включают:
Подходы дистанционного зондирования включают:
Частицы могут откладываться в носу, рот, глотка и гортань (область головных дыхательных путей), глубже в дыхательных путях (от трахеи до терминала bronchioles ) или в альвеолярной области. Местоположение осаждения аэрозольных частиц в дыхательной системе во многом определяет последствия воздействия таких аэрозолей на здоровье. Это явление побудило людей изобрести пробоотборники аэрозоля, которые отбирают подмножество частиц аэрозоля, которые достигают определенных частей дыхательной системы. Примеры этих подмножеств гранулометрического состава аэрозоля, важного для профессиональной гигиены, включают вдыхаемые, торакальные и вдыхаемые фракции. Фракция, которая может попасть в каждую часть дыхательной системы, зависит от отложения частиц в верхних отделах дыхательных путей. Вдыхаемая фракция частиц, определяемая как доля частиц, изначально находящихся в воздухе, которые могут попасть в нос или рот, зависит от скорости и направления внешнего ветра, а также от гранулометрического состава по аэродинамическому диаметру. Торакальная фракция - это доля частиц в атмосферном аэрозоле, которые могут достигать грудной клетки или грудной клетки. Вдыхаемая фракция - это доля частиц в воздухе, которые могут достичь альвеолярной области. Для измерения вдыхаемой фракции частиц в воздухе используется предварительный коллектор с фильтром для отбора проб. Предварительный коллектор удаляет частицы, поскольку дыхательные пути удаляют частицы из вдыхаемого воздуха. Фильтр для отбора проб собирает частицы для измерения. Обычно для предварительного коллектора используют циклонное разделение, но другие методы включают ударные, горизонтальные и большие пористые мембранные фильтры.
Два альтернативных критерия отбора по размеру, часто используемых при атмосферном мониторинге, равны PM 10 и PM 2,5. PM 10 определяется в ISO как частицы, которые проходят через входное отверстие с избирательным размером с 50% эффективностью отсечки при аэродинамическом диаметре 10 мкм и PM 2,5 в виде частиц, которые проходят через входное отверстие с избирательным размером с 50% эффективностью отсечки при аэродинамическом диаметре 2,5 мкм. PM 10 соответствует «грудному условию», как определено в ISO 7708: 1995, раздел 6; PM 2,5 соответствует «условию респирабельности высокого риска», как определено в ISO 7708: 1995, 7.1. Агентство по охране окружающей среды США заменило старые стандарты для твердых частиц, основанные на общем количестве взвешенных частиц, другим стандартом, основанным на PM 10 в 1987 году, а затем ввело стандарты для PM 2,5 (также известный как мелкие твердые частицы) в 1997 г.
 Загрязнение аэрозолями над северной Индией и Бангладеш
Загрязнение аэрозолями над северной Индией и Бангладеш Некоторые типы атмосферных аэрозолей имеют значительную влияние на климат Земли: вулканические, пустынная пыль, морская соль, происходящие из биогенных источников и созданные человеком. Вулканический аэрозоль образуется в стратосфере после извержения в виде капель серной кислоты, которые могут преобладать до двух лет и отражать солнечный свет, понижая температуру. Пустынная пыль и минеральные частицы, уносимые на большие высоты, поглощают тепло и могут быть причиной предотвращения образования грозовых облаков. Созданные человеком сульфатные аэрозоли, в основном из-за сжигания нефти и угля, влияют на поведение облаков.
Хотя все гидрометеоры, твердые и жидкие, можно охарактеризовать как аэрозоли, обычно проводится различие между такими дисперсиями (т.е. облаками), содержащими активированные капли и кристаллы, и аэрозольными частицами. атмосфера Земли содержит аэрозоли различных типов и концентраций, включая количества:
Аэрозоли можно найти в городских экосистемах в различных формах, например:
Наличие аэрозолей в атмосфере Земли может повлиять на ее климат, а также на здоровье человека.
| На Wikimedia Commons есть материалы, связанные с Аэрозолями. |